解题方法
1 . 如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容。某同学从该试剂瓶中取出24.0 g固体,配成1 L溶液,请计算:
(1)所得氢氧化钠溶液的物质的量浓度为___________ 。
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为___________ 。(写出解答步骤)
| 氢氧化钠 化学纯(CP) 500 g 品名:氢氧化钠 化学式:NaOH 相对分子质量:40 |
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为
您最近一年使用:0次
2 . 根据所学知识,回答下列问题:
(1)常温常压下,HCl气体溶于水形成的盐酸溶液,其溶质质量分数为
 ,密度为
,密度为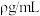 ,该溶液浓度为
,该溶液浓度为 。
。(2)“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物.
 “可燃冰”(
“可燃冰”( )的物质的量与
)的物质的量与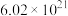 个水分子的物质的量相等,则该“可燃冰”的摩尔质量为
个水分子的物质的量相等,则该“可燃冰”的摩尔质量为(3)过氧化钠可用作呼吸面罩供氧剂,其原理可用方程式
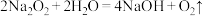 ,
,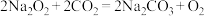 表示。若生成标况下
表示。若生成标况下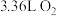 ,转移电子的数目为
,转移电子的数目为(4)现有
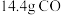 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为
。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为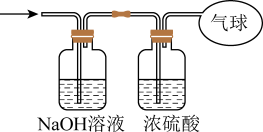
您最近一年使用:0次
解题方法
3 . 将某质量的镁铝合金溶解在500 mL盐酸中,向反应后的溶液中逐滴加入2 mol/L NaOH溶液,产生沉淀质量与碱溶液体积的关系如图所示。请填写下列空白:
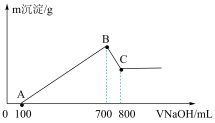
(1)写出BC段发生反应的化学方程式:_______ 。
(2)合金中铝的质量为_______ 。
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是_______ 。

(1)写出BC段发生反应的化学方程式:
(2)合金中铝的质量为
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是
您最近一年使用:0次
4 . 实验室通常利用质量分数36.5%盐酸(密度为1.14g/mL)与二氧化锰通过反应制取Cl2。通过计算回答下列问题:
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为_______ 。
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为_______ 克。
(3)此时,被氧化HCl的物质的量为_______ 。
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为
(3)此时,被氧化HCl的物质的量为
您最近一年使用:0次
5 . 物质的量是高中化学常用的物理量,请完成以下有关计算(设阿伏加德罗常数的值为NA):
(1)在标准状况下,0.5molO2的体积为_______ L。
(2)将0.2moLMgCl2固体溶于水配成400mL溶液,MgCl2溶液的物质的量浓度为_______ 。
(3)0.2molCH4含有_______ NA个氢原子。
(4)49g 的物质的量是
的物质的量是_______ mol。
(5)标准状况下,2gH2的体积是_______ L。
(6)等物质的量的 和
和 的质量之比为
的质量之比为_______ 。
(7)标准状况下6.72L某气体质量13.2g,该物质的摩尔质量为_______ 。
(1)在标准状况下,0.5molO2的体积为
(2)将0.2moLMgCl2固体溶于水配成400mL溶液,MgCl2溶液的物质的量浓度为
(3)0.2molCH4含有
(4)49g
 的物质的量是
的物质的量是(5)标准状况下,2gH2的体积是
(6)等物质的量的
 和
和 的质量之比为
的质量之比为(7)标准状况下6.72L某气体质量13.2g,该物质的摩尔质量为
您最近一年使用:0次
6 . 按要求填写下列空格。
(1)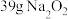 中阴离子的数目为
中阴离子的数目为________
(2) 个水分子的质量为
个水分子的质量为________
(3)现有标准状况下 和
和 混合气体6.72L,其质量为10g,则此混合气体中,
混合气体6.72L,其质量为10g,则此混合气体中, 和
和 的物质的量之比是
的物质的量之比是________
(4)9.2g氮的氧化物 中N原子的物质的量为
中N原子的物质的量为 ,则x的数值为
,则x的数值为________ 。
(5)某盐混合溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则 =
=________
(6)取 钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是
钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是________
(7)使用胆矾配制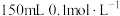 的
的 溶液,需要用托盘天平称取胆矾的质量为
溶液,需要用托盘天平称取胆矾的质量为________
(1)
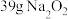 中阴离子的数目为
中阴离子的数目为(2)
 个水分子的质量为
个水分子的质量为(3)现有标准状况下
 和
和 混合气体6.72L,其质量为10g,则此混合气体中,
混合气体6.72L,其质量为10g,则此混合气体中, 和
和 的物质的量之比是
的物质的量之比是(4)9.2g氮的氧化物
 中N原子的物质的量为
中N原子的物质的量为 ,则x的数值为
,则x的数值为(5)某盐混合溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则 =
=(6)取
 钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是
钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是(7)使用胆矾配制
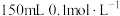 的
的 溶液,需要用托盘天平称取胆矾的质量为
溶液,需要用托盘天平称取胆矾的质量为
您最近一年使用:0次
名校
解题方法
7 . 计算题
(1)一定量的质量分数为10%的氢氧化钠溶液,若将其蒸发掉100g水,其质量分数恰好变为20%,溶液体积变为80mL,则浓缩后的氢氧化钠溶液物质的量浓度为___________ mol/L。
(2)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是___________ L。(用含字母的式子表示,NA表示阿伏伽德罗常数)
(3)有8gNa2O、Na2O2、Na2CO3、NaOH的混合物与200g质量分数为3.65%的盐酸恰好反应,最终得NaCl固体质量为___________ g。
(4)在VL硫酸铁溶液中,含有agFe3+,取出 L溶液,则取出的
L溶液,则取出的 L溶液中,SO
L溶液中,SO 的物质的量浓度为
的物质的量浓度为___________ mol/L。
(1)一定量的质量分数为10%的氢氧化钠溶液,若将其蒸发掉100g水,其质量分数恰好变为20%,溶液体积变为80mL,则浓缩后的氢氧化钠溶液物质的量浓度为
(2)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
(3)有8gNa2O、Na2O2、Na2CO3、NaOH的混合物与200g质量分数为3.65%的盐酸恰好反应,最终得NaCl固体质量为
(4)在VL硫酸铁溶液中,含有agFe3+,取出
 L溶液,则取出的
L溶液,则取出的 L溶液中,SO
L溶液中,SO 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
8 . 回答下列问题:
(1)在标准状况下,1.7g氨气所占的体积约为_______ L,它与_______ 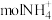 含有相同数目的电子。
含有相同数目的电子。
(2)某气态氧化物化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为_______ 。
(3)同温同压下, 与氦气的密度之比为
与氦气的密度之比为_______ ,若质量相同,两种气体的体积比为_______ 。
(4)在标准状况下,将A气体VL(摩尔质量是 )溶于0.5L水中,所得溶液的密度为
)溶于0.5L水中,所得溶液的密度为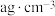 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为_______ 。
(5)现有含 和
和 的混合溶液200mL,其中
的混合溶液200mL,其中 物质的量浓度为
物质的量浓度为 ,
, 物质的量浓度为
物质的量浓度为 ,若向此溶液中加入一定量浓硫酸,使其配成
,若向此溶液中加入一定量浓硫酸,使其配成 和
和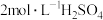 的混合溶液。请问最终所得混合溶液的体积是
的混合溶液。请问最终所得混合溶液的体积是_______ mL,需加入密度为 、质量分数为98%的浓硫酸
、质量分数为98%的浓硫酸_______ mL(保留到小数点后1位)。
(1)在标准状况下,1.7g氨气所占的体积约为
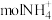 含有相同数目的电子。
含有相同数目的电子。(2)某气态氧化物化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物中R的相对原子质量为(3)同温同压下,
 与氦气的密度之比为
与氦气的密度之比为(4)在标准状况下,将A气体VL(摩尔质量是
 )溶于0.5L水中,所得溶液的密度为
)溶于0.5L水中,所得溶液的密度为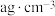 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(5)现有含
 和
和 的混合溶液200mL,其中
的混合溶液200mL,其中 物质的量浓度为
物质的量浓度为 ,
, 物质的量浓度为
物质的量浓度为 ,若向此溶液中加入一定量浓硫酸,使其配成
,若向此溶液中加入一定量浓硫酸,使其配成 和
和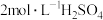 的混合溶液。请问最终所得混合溶液的体积是
的混合溶液。请问最终所得混合溶液的体积是 、质量分数为98%的浓硫酸
、质量分数为98%的浓硫酸
您最近一年使用:0次
9 . 回答下列问题
(1)①石墨 ②苛性钠 ③石灰乳 ④熔融氯化钾 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧铁⑨液态氯化氢 ⑩硫酸溶液,上述物质中能导电且属于电解质的是___________ ,属于混合物的是___________ (填编号)
(2)按要求进行化学计算:
①在同温、同压、同体积的条件下, 与某气体A的质量之比是1:16,则A的摩尔质量为
与某气体A的质量之比是1:16,则A的摩尔质量为___________ 。
②一定量的Al、Mg混合物加入一定物质的量浓度、一定体积的盐酸溶液中恰好完全反应,放出标况下11.2L气体,再向溶液中加入 氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为
氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为___________ mL。
③相同体积的 、
、 、
、 溶液,分别与足量的
溶液,分别与足量的 溶液反应,当生成的
溶液反应,当生成的 质量相同时,则三种溶液的物质的量浓度之比为
质量相同时,则三种溶液的物质的量浓度之比为___________ 。
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为
①配平该反应:_______

②当有32g硫单质完全反应时,生成氧化产物的物质的量是___________ mol。
(1)①石墨 ②苛性钠 ③石灰乳 ④熔融氯化钾 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧铁⑨液态氯化氢 ⑩硫酸溶液,上述物质中能导电且属于电解质的是
(2)按要求进行化学计算:
①在同温、同压、同体积的条件下,
 与某气体A的质量之比是1:16,则A的摩尔质量为
与某气体A的质量之比是1:16,则A的摩尔质量为②一定量的Al、Mg混合物加入一定物质的量浓度、一定体积的盐酸溶液中恰好完全反应,放出标况下11.2L气体,再向溶液中加入
 氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为
氢氧化钠溶液恰好使溶液中金属阳离子完全沉淀,则需要氢氧化钠溶液的体积为③相同体积的
 、
、 、
、 溶液,分别与足量的
溶液,分别与足量的 溶液反应,当生成的
溶液反应,当生成的 质量相同时,则三种溶液的物质的量浓度之比为
质量相同时,则三种溶液的物质的量浓度之比为(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为

①配平该反应:

②当有32g硫单质完全反应时,生成氧化产物的物质的量是
您最近一年使用:0次
解题方法
10 . 根据所学知识,回答下列问题:
(1)下图是中学化学中常用于混合物的分离和提纯的装置:
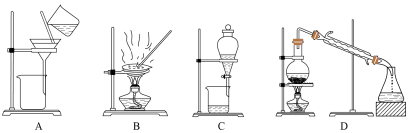
①分离花生油和水的混合物,选择装置_____ (填字母,下同)。
②提纯粗盐,并得到氯化钠晶体,选择装置_____ 。
③用 提取碘水中的碘,选择装置
提取碘水中的碘,选择装置_____ 。
④除去自来水中的 等杂质,选择装置
等杂质,选择装置_____ 。
(2)化学计量在中学化学中占有重要地位。
①标准状况下,体积为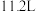 的
的 的质量为
的质量为_____ g。
②标准状况下, 某气体的质量为
某气体的质量为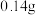 ,则其摩尔质量为
,则其摩尔质量为_____  。
。
③等物质的量的 和
和 中氢原子个数比是
中氢原子个数比是_____ 。
④ 的
的 溶液中含有的
溶液中含有的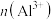 是
是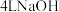 溶液中
溶液中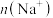 的两倍,则
的两倍,则
_____  。
。
(1)下图是中学化学中常用于混合物的分离和提纯的装置:

①分离花生油和水的混合物,选择装置
②提纯粗盐,并得到氯化钠晶体,选择装置
③用
 提取碘水中的碘,选择装置
提取碘水中的碘,选择装置④除去自来水中的
 等杂质,选择装置
等杂质,选择装置(2)化学计量在中学化学中占有重要地位。
①标准状况下,体积为
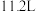 的
的 的质量为
的质量为②标准状况下,
 某气体的质量为
某气体的质量为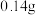 ,则其摩尔质量为
,则其摩尔质量为 。
。③等物质的量的
 和
和 中氢原子个数比是
中氢原子个数比是④
 的
的 溶液中含有的
溶液中含有的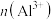 是
是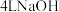 溶液中
溶液中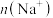 的两倍,则
的两倍,则
 。
。
您最近一年使用:0次



