名校
1 . 电解质溶于水时会发生电离产生自由移动的离子,电导率变化一定程度上可以反映溶液中自由移动的离子浓度变化。溶液中自由移动的离子浓度越大,电导率就越大。某同学向两份相同的Ba(OH)2溶液中,分别滴入浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
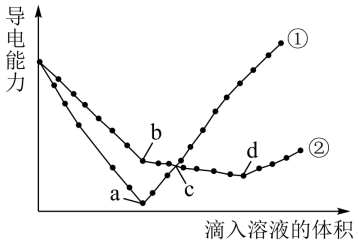
(1)请写出NaHSO4在水溶液中的电离方程式_____ 。
(2)曲线①代表滴加____ 溶液时导电能力的变化。
(3)曲线②上bd段的离子方程式为____ 。
(4)图中a、b、c、d四点中,对应溶液为中性的是____ ,对应溶液中Ba2+刚好完全沉淀的是_____ 。

(1)请写出NaHSO4在水溶液中的电离方程式
(2)曲线①代表滴加
(3)曲线②上bd段的离子方程式为
(4)图中a、b、c、d四点中,对应溶液为中性的是
您最近一年使用:0次
2022-10-15更新
|
363次组卷
|
3卷引用:黑龙江省哈尔滨市第三中学校2022-2023学年高一上学期10月月考化学试题
解题方法
2 . 现有下列物质:①草木灰② ③熔融
③熔融 ④
④ 胶体⑤液态氯化氢⑥稀硫酸⑦
胶体⑤液态氯化氢⑥稀硫酸⑦ 溶液⑧金刚石⑨氨水⑩酒精⑪
溶液⑧金刚石⑨氨水⑩酒精⑪ ⑫澄清石灰水。请将序号分别填入下面的横线处:
⑫澄清石灰水。请将序号分别填入下面的横线处:
(1)上述状态下可导电的是_____ ,属于电解质的是_____ ,属于非电解质的是_____ ,属于纯净物的是_______ ,属于盐的是_______ 。
(2)⑦与少量的⑫的离子反应方程式是_______ 。
(3)写出物质③溶于水的电离方程式:_______ 。
(4)将过量⑪通入⑫溶液中的现象是_______ 。
(5)将⑦加入 溶液中出现红褐色沉淀和无色无味气体的离子方程式
溶液中出现红褐色沉淀和无色无味气体的离子方程式_______ 。
 ③熔融
③熔融 ④
④ 胶体⑤液态氯化氢⑥稀硫酸⑦
胶体⑤液态氯化氢⑥稀硫酸⑦ 溶液⑧金刚石⑨氨水⑩酒精⑪
溶液⑧金刚石⑨氨水⑩酒精⑪ ⑫澄清石灰水。请将序号分别填入下面的横线处:
⑫澄清石灰水。请将序号分别填入下面的横线处:(1)上述状态下可导电的是
(2)⑦与少量的⑫的离子反应方程式是
(3)写出物质③溶于水的电离方程式:
(4)将过量⑪通入⑫溶液中的现象是
(5)将⑦加入
 溶液中出现红褐色沉淀和无色无味气体的离子方程式
溶液中出现红褐色沉淀和无色无味气体的离子方程式
您最近一年使用:0次
3 . 室温下,在1 mol·L-1的某二元酸H2A溶液中,存在HA-、A2-的物质的量分数随pH变化的关系如图所示,下列说法错误的是
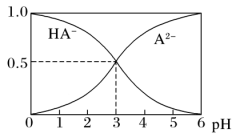

| A.0.1 mol·L-1 NaHA溶液中:c(OH- )>c(H+) |
B.室温下,HA- A2-+ H+的电离平衡常数Ka= 10-3 A2-+ H+的电离平衡常数Ka= 10-3 |
| C.在Na2A溶液中存在c(Na+)=2c(A2-)+2c(HA- ) |
D.H2A的电离方程式为H2A=H+ +HA-,HA- A2-+H+ A2-+H+ |
您最近一年使用:0次
2022-09-06更新
|
1069次组卷
|
3卷引用:河南省濮阳市2021-2022学年高二上学期期末学业质量监测化学试题
解题方法
4 . 十二水合硫酸铝钾[KA1(SO4)2﹒12H2O]俗名明矾,在生活、医药、工业上应用广泛。下面是实验室探究从铝土矿(主要成分是氧化铝,含少量氧化铁和二氧化硅杂质)制备明矾的流程示意图。
已知:二氧化硅不溶于水,也不与硫酸反应。
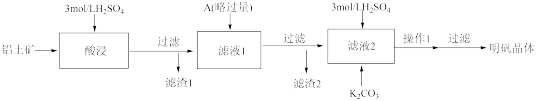
(1)铝元素在地壳中以_______ 态存在,写出KAl(SO4)2溶于水的电离方程式_______ 。
(2)滤渣1主要为_______ (填化学式)。
(3)若A为金属单质,则滤渣2的成分有_______ 。
(4)操作1是蒸发溶剂至有大量晶膜、冷却结晶。实验室进行该操作时,需要的实验仪器有铁架台、酒精灯、_______ 。
(5)下图为某硫酸试剂瓶的标签。若用其配制100mL3mol/L的溶液,需该硫酸_______ mL(含ρ的表达式即可)。
(6)若将铝箔包裹0.1mol金属钠用针扎若干小孔后,放入水中完全反应,用排水法收集到标准状况下气体的体积_______ (填字母序号)。
a.大于1.12L b.等于1.12L c.小于1.12L
已知:二氧化硅不溶于水,也不与硫酸反应。

(1)铝元素在地壳中以
(2)滤渣1主要为
(3)若A为金属单质,则滤渣2的成分有
(4)操作1是蒸发溶剂至有大量晶膜、冷却结晶。实验室进行该操作时,需要的实验仪器有铁架台、酒精灯、
(5)下图为某硫酸试剂瓶的标签。若用其配制100mL3mol/L的溶液,需该硫酸
| 硫酸 分子式:H2SO4 相对分子质量:98 外观:合格 密度:ρg/cm3 H2SO4的质量分数:70% |
a.大于1.12L b.等于1.12L c.小于1.12L
您最近一年使用:0次
名校
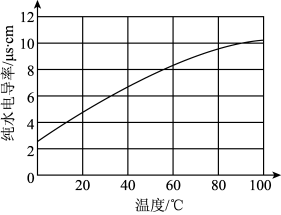
5 . 下列实验现象或数据不能用勒沙特列原理解释的是
 |  | ||||||
| A.探究溶液碱性强弱 | B.探究难溶性钡盐的生成 | ||||||
 |
| ||||||
| C.测定不同温度纯水的导电性 | D.测定不同浓度氨水的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 室温下,用0.1mol/L的盐酸滴定0.1mol/L溴化肼(N2H5Br)的25mL溶液,已知肼(N2H4)是二元弱碱(与NH3类似),滴定过程中混合溶液的相对导电能力变化曲线如图所示。下列叙述错误的是


A.N2H 与Cl-的导电能力之和大于N2H 与Cl-的导电能力之和大于N2H 的 的 |
B.b点表示盐酸与溴化肼恰好完全反应:c(Cl-)=c(Br-)>c(N2H ) ) |
C.c点的混合溶液中:c(H+)>c(N2H )>c(N2H )>c(N2H ) ) |
| D.N2H4与硫酸反应形成的酸式盐的化学式为N2H6(HSO4)2 |
您最近一年使用:0次
名校
7 . 对于成千上万、形形色色的化学物质,用分类的思想对其进行学习和研究极其重要。有以下物质,请按要求作答。
① ②
② ③熔融
③熔融 ④盐酸 ⑤葡萄糖溶液 ⑥
④盐酸 ⑤葡萄糖溶液 ⑥ ⑦
⑦ 胶体 ⑧
胶体 ⑧ ⑨细铁丝 ⑩
⑨细铁丝 ⑩
(1)上述物质能导电的有_______ (填序号,下同),属于电解质的有_______ 。
(2)请写出②与④反应的离子反应方程式_______ 。
(3)写出⑧在水溶液中的电离方程式_______
(4)向⑩的水溶液中逐滴滴加⑧的水溶液,溶液的导电能力变化曲线如图中的_______ (填字母),当溶液恰好呈中性时 与
与 的物质的量之比为
的物质的量之比为_______ 。
A. B.
B. 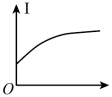
C.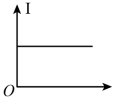 D.
D.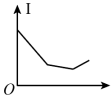
①
 ②
② ③熔融
③熔融 ④盐酸 ⑤葡萄糖溶液 ⑥
④盐酸 ⑤葡萄糖溶液 ⑥ ⑦
⑦ 胶体 ⑧
胶体 ⑧ ⑨细铁丝 ⑩
⑨细铁丝 ⑩
(1)上述物质能导电的有
(2)请写出②与④反应的离子反应方程式
(3)写出⑧在水溶液中的电离方程式
(4)向⑩的水溶液中逐滴滴加⑧的水溶液,溶液的导电能力变化曲线如图中的
 与
与 的物质的量之比为
的物质的量之比为A.
 B.
B. 
C.
 D.
D.
您最近一年使用:0次
8 . 数形结合思想是化学学科的重要思维模式,请结合所学知识和图象作答:
Ⅰ.回答下列问题
(1)如图为含氯元素物质的“价类二维图”,下列说法正确的是___________

Ⅱ.某实验小组向 溶液中通入氯气,溶液中
溶液中通入氯气,溶液中 、
、 的物质的量随通入的氯气的物质的量变化如图所示(不考虑与水的反应)。请回答下列问题:
的物质的量随通入的氯气的物质的量变化如图所示(不考虑与水的反应)。请回答下列问题:

(2)从开始通入 到
到 时,溶液中:
时,溶液中: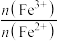
___________ 。
(3)通入0.15mol氯气的总反应的离子方程式为___________
Ⅲ.把 三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入
三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入 溶液,加入HCl溶液的体积与生成沉淀的关系如图。试回答:
溶液,加入HCl溶液的体积与生成沉淀的关系如图。试回答:

(4)AB段发生反应的离子方程式为___________ 。
(5)C点消耗HCl溶液的体积为___________ mL。
Ⅰ.回答下列问题
(1)如图为含氯元素物质的“价类二维图”,下列说法正确的是___________

| A.乙、丁均属于电解质 |
| B.丙的酸性强于碳酸 |
| C.乙是一种广谱型的消毒剂,可取代甲成为自来水的消毒剂 |
| D.戊→己必须加还原剂才能实现 |
Ⅱ.某实验小组向
 溶液中通入氯气,溶液中
溶液中通入氯气,溶液中 、
、 的物质的量随通入的氯气的物质的量变化如图所示(不考虑与水的反应)。请回答下列问题:
的物质的量随通入的氯气的物质的量变化如图所示(不考虑与水的反应)。请回答下列问题:
(2)从开始通入
 到
到 时,溶液中:
时,溶液中:
(3)通入0.15mol氯气的总反应的离子方程式为
Ⅲ.把
 三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入
三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入 溶液,加入HCl溶液的体积与生成沉淀的关系如图。试回答:
溶液,加入HCl溶液的体积与生成沉淀的关系如图。试回答:
(4)AB段发生反应的离子方程式为
(5)C点消耗HCl溶液的体积为
您最近一年使用:0次
9 . 向两份等物质的量浓度等体积的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其电导率随滴入溶液体积变化的曲线如图所示。下列分析正确的是
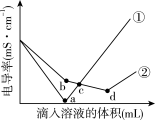

| A.①代表滴加NaHSO4溶液的变化曲线 |
B.c点两溶液中的 浓度不同 浓度不同 |
| C.a点对应溶液的pH大于d点 |
| D.等物质的量浓度H+和Na+,导电能力前者大 |
您最近一年使用:0次
名校
10 . 向20mLymol/L的HX和zmol/L的CH3COOH混合溶液中滴加0.1mol/L的氨水,维持其他条件不变时,测得混合溶液的电流强度(I)与加入氨水的体积(V)的关系如图所示(已知相同温度下CH3COOH与NH3•H2O的电离常数相等),下列说法错误的是


| A.y=z=0.1 |
| B.水的电离程度:c>b>a |
C.c点溶液中,c(NH )>c(X-)>c(CH3COO-)>c(H+)>c(OH-) )>c(X-)>c(CH3COO-)>c(H+)>c(OH-) |
| D.d点溶液中一定存在H2O、NH3•H2O、HX、CH3COOH四种分子 |
您最近一年使用:0次



