1 . 由铝土矿生产氧化铝的过程中产生的废渣(赤泥)中含有 、
、 、
、 ,可以通过下列工艺将各金属元素回收利用。
,可以通过下列工艺将各金属元素回收利用。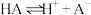 ,
, 可以与钢、铁元素离子络合,形成易溶于有机溶剂的配合物;溶液C中钛以
可以与钢、铁元素离子络合,形成易溶于有机溶剂的配合物;溶液C中钛以 存在。
存在。
下列说法错误的是
 、
、 、
、 ,可以通过下列工艺将各金属元素回收利用。
,可以通过下列工艺将各金属元素回收利用。 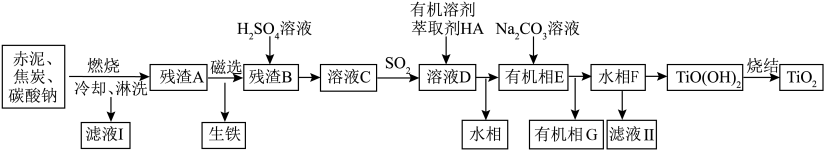

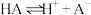 ,
, 可以与钢、铁元素离子络合,形成易溶于有机溶剂的配合物;溶液C中钛以
可以与钢、铁元素离子络合,形成易溶于有机溶剂的配合物;溶液C中钛以 存在。
存在。下列说法错误的是
A.滤液I中溶质的主要成分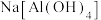 |
B. 的作用是还原 的作用是还原 |
| C.溶液D的pH越大,钛的萃取效果越好 |
D.有机相E与 反应的离子方程式: 反应的离子方程式: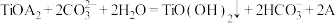 |
您最近一年使用:0次
2 . 利用电石渣[主要成分为 ,含少量
,含少量 、
、 、
、 等杂质]制备碳酸钙,同时获得氧化铝,工艺流程如图。下列说法错误的是
等杂质]制备碳酸钙,同时获得氧化铝,工艺流程如图。下列说法错误的是
 ,含少量
,含少量 、
、 、
、 等杂质]制备碳酸钙,同时获得氧化铝,工艺流程如图。下列说法错误的是
等杂质]制备碳酸钙,同时获得氧化铝,工艺流程如图。下列说法错误的是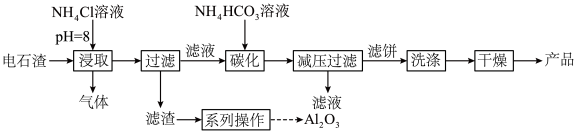
| A.“气体”为NH3 |
B.“碳化”反应为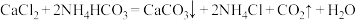 |
| C.“浸取”和“碳化”为了加快反应速率,需在高温下进行 |
D.“滤渣”主要成分为 、 、 |
您最近一年使用:0次
名校
3 . 氯化亚铜(CuCl)是石油工业常用的脱硫剂和脱色剂,以低品位铜矿(主要成分为 和铁的氧化物)为原料制备CuCl流程如图。
和铁的氧化物)为原料制备CuCl流程如图。
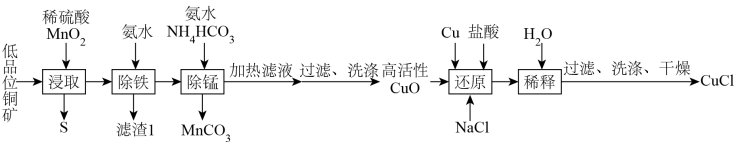
已知:CuCl难溶于醇和水,热水中能被氧化,CuCl易溶于浓度较大的 体系中(
体系中(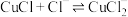 )。
)。
下列说法错误的是
 和铁的氧化物)为原料制备CuCl流程如图。
和铁的氧化物)为原料制备CuCl流程如图。
已知:CuCl难溶于醇和水,热水中能被氧化,CuCl易溶于浓度较大的
 体系中(
体系中(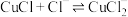 )。
)。下列说法错误的是
| A.“浸取”过程中可用浓硫酸代替稀硫酸 |
B.“除锰”过程中发生离子反应为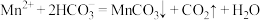 |
C.“还原”后所得产物主要为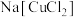 |
| D.产品CuCl可用冷的乙醇洗涤 |
您最近一年使用:0次
名校
解题方法
4 . 一种工业制备无水氯化镁的工艺流程如下:
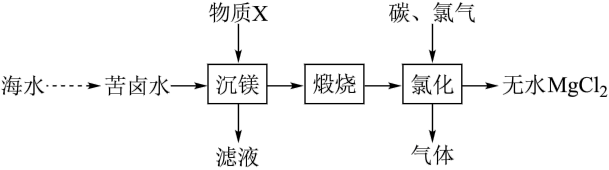
A.“沉镁”时可能发生反应: |
| B.在实验室中“煅烧”时使用的仪器为坩埚,同时需要用玻璃棒不断搅拌 |
| C.“氯化”过程中发生的反应为气体分子数增加的反应 |
D.不可以通过直接灼烧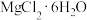 晶体的方法得到无水 晶体的方法得到无水 固体 固体 |
您最近一年使用:0次
2024-03-26更新
|
128次组卷
|
3卷引用:不定选择题11-15
5 . 下列离子方程式书写正确的是
A.稀硫酸与铁丝制取氢气: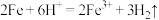 |
B. 溶液与少量NaOH溶液反应: 溶液与少量NaOH溶液反应: |
C.碳酸钙与稀盐酸制备二氧化碳: |
D. 溶液中滴加 溶液中滴加 溶液: 溶液: |
您最近一年使用:0次
6 . 已知25℃时,K(HClO)=4.0×10-8。下列关于NaClO溶液说法错误的是
| A.0.01mol/LNaClO溶液中,c(ClO-)<0.01mol/L |
| B.长期露置在空气中,释放Cl2,漂白能力减弱 |
C.通入过量SO2,反应的离子方程式为SO2+ ClO-+H2O=HSO +HClO +HClO |
| D.25℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)> c(ClO-)=c(Na+) |
您最近一年使用:0次
解题方法
7 . 工业上制备硼酸的工作原理如图所示。下列说法正确的是


A.电势: |
B.c膜为阴离子交换膜, 由N室向原料室迁移 由N室向原料室迁移 |
C.产品室中反应的离子方程式: |
D.理论上每生成  ,M、N两室共产生16.8L气体(标准状况) ,M、N两室共产生16.8L气体(标准状况) |
您最近一年使用:0次
名校
8 . 制药厂对产生的“三废”之一 有多种脱除或利用方法。下列说法正确的是
有多种脱除或利用方法。下列说法正确的是
 有多种脱除或利用方法。下列说法正确的是
有多种脱除或利用方法。下列说法正确的是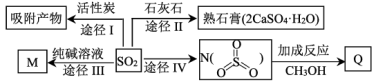
| A.途径Ⅰ,一般来说,温度低时活性炭对废气的吸附量更大 |
B.途径Ⅱ,每得到 熟石膏转移 熟石膏转移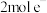 |
C.途径Ⅲ,纯碱溶液不足时离子方程式可能为: |
D.途径Ⅳ,若N与 按 按 加成,则所得化合物Q具有酸性 加成,则所得化合物Q具有酸性 |
您最近一年使用:0次
2024-02-06更新
|
265次组卷
|
2卷引用:山东省威海市2023-2024学年高三上学期期末考试化学试题
9 . 湿法制备多功能水处理剂K2FeO4固体的工艺流程如下:
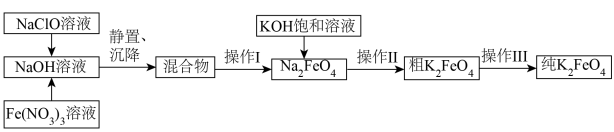
已知:NaCl、NaNO3在强碱中溶解度远小于Na2FeO4。
下列说法正确的是

已知:NaCl、NaNO3在强碱中溶解度远小于Na2FeO4。
下列说法正确的是
| A.溶解度:K2FeO4大于Na2FeO4 |
| B.“操作Ⅱ”所得副产物可循环使用 |
| C.“操作Ⅰ、Ⅱ、Ⅲ”都要使用的玻璃仪器有漏斗、玻璃棒、烧杯、酒精灯 |
D.生成Na2FeO4的离子方程式为 |
您最近一年使用:0次
名校
解题方法
10 . 下列反应对应的离子方程式正确的是
| A.Fe2(SO4)3的酸性溶液中通入足量硫化氢:Fe3++H2S=Fe2++S↓+2H+ |
B.碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++2 +2OH-=CaCO3↓+2H2O+ +2OH-=CaCO3↓+2H2O+ |
| C.氯化铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ |
D.用Na2SO3溶液吸收少量Cl2:3 +Cl2+H2O=2 +Cl2+H2O=2 +2Cl-+ +2Cl-+ |
您最近一年使用:0次



