1 . 人类社会的发展离不开“求知求真”.某化学兴趣小组以 溶液与
溶液与 溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。
溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。
(1)实验预测
(2)实验探究
实验一:探究 与
与 能否发生反应①,设计装置如下图,能证明反应已经发生的现象有
能否发生反应①,设计装置如下图,能证明反应已经发生的现象有_______ [已知: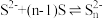 ]。
]。

实验二:探究 与
与 能否发生反应②和③,设计如下实验:
能否发生反应②和③,设计如下实验:
实验结论
 与
与 在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
 溶液与
溶液与 溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。
溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。(1)实验预测
| 推测可能发生的反应 | 推测依据 | 预期的实验现象 |
| ①氧化还原反应 |  具有一定的氧化性, 具有一定的氧化性, 具有较强的还原性 具有较强的还原性 | 若 过量,则有淡黄色沉淀(S)生成若 过量,则有淡黄色沉淀(S)生成若 过量,则有黑色沉淀 过量,则有黑色沉淀 |
| ②复分解反应 |  为黑色难溶物, 为黑色难溶物,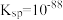 | 有黑色固体生成 |
| ③彻底双水解反应 |  、 、 水解能力均较强 水解能力均较强 | 有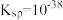 )产生,同时有臭鸡蛋气味的气体(H2S)生成 )产生,同时有臭鸡蛋气味的气体(H2S)生成 |
实验一:探究
 与
与 能否发生反应①,设计装置如下图,能证明反应已经发生的现象有
能否发生反应①,设计装置如下图,能证明反应已经发生的现象有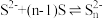 ]。
]。
实验二:探究
 与
与 能否发生反应②和③,设计如下实验:
能否发生反应②和③,设计如下实验:| 实验步骤 | 实验现象 | 实验解释或结论 |
ⅰ.向 饱和 饱和 溶液中,滴加2滴饱和 溶液中,滴加2滴饱和 溶液 溶液 | 有黑色沉淀生成,而后黑色沉淀消失,出现淡黄色沉淀 | 用离子方程式解释黑色沉淀消失的原因: |
ⅱ.将 饱和 饱和 溶液与 溶液与 饱和 饱和 溶液直接混合 溶液直接混合 | 先有黑色和另一种颜色的沉淀生成,而后都变为黑色;同时有臭鸡蛋气味的气体生成 | 试解释:沉淀最终都变为黑色的原因是 |
ⅲ.取ⅱ中最终生成的黑色沉淀样品,用无水乙醇多次洗涤后,干燥称量得 黑色固体,然后在空气中灼烧至恒重 黑色固体,然后在空气中灼烧至恒重 | 灼烧后,所得红棕色固体质量为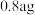 | 经计算判断,黑色固体样品的成份为 |
 与
与 在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
您最近一年使用:0次
2 . 二氧化铈(CeO2) 是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含 SiO2、 Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。
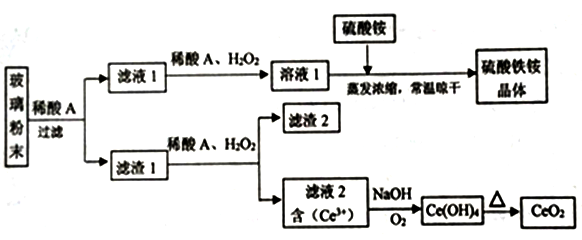
已知: CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1) 稀酸A的分子式是__________ 。
(2) 滤液I中加入H2O2溶液的目的是__________ 。
(3) 由滤渣1生成滤液2的离子方程式为__________ 。
(4) 设计实验证明滤液1中含有Fe2+__________ 。
(5) 已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe2O4,写出该反应的离子方程式__________ 。
(6)由滤液2 生成Ce(OH)4的离子方程式为__________ 。
(7) 硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,用离子方程式表示其净水原理__________ 。

已知: CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1) 稀酸A的分子式是
(2) 滤液I中加入H2O2溶液的目的是
(3) 由滤渣1生成滤液2的离子方程式为
(4) 设计实验证明滤液1中含有Fe2+
(5) 已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe2O4,写出该反应的离子方程式
(6)由滤液2 生成Ce(OH)4的离子方程式为
(7) 硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,用离子方程式表示其净水原理
您最近一年使用:0次
3 . 某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
(1)制取新制Cu(OH)2悬浊液的离子方程式为_________ 。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:_________ 。检验Cu(OH)2洗涤干净的方法是_________ 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O = Cu(NH3) +Cl- + 2H2O 、
+Cl- + 2H2O 、 _________ 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:

填写下表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式:_________ 。
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中,__________ ,则说明砖红色沉淀是Cu2O。
| 装置 | 序号 | 试管中的药品 | 现象 |
持续通入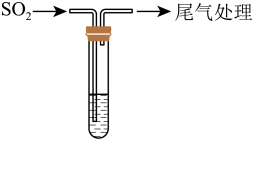 | 实验Ⅰ | 1.5 mL 1 mol·L-1 CuSO4溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
实验Ⅱ | 1.5 mL 1 mol·L-1 CuCl2溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O = Cu(NH3)
 +Cl- + 2H2O 、
+Cl- + 2H2O 、 ②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:

填写下表空格:
| 试剂1 | 试剂2 | 蒸馏水 | |
| 现象1 | 现象2 |
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中,
您最近一年使用:0次
11-12高三上·广西桂林·阶段练习
解题方法
4 . 1.电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代。处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。
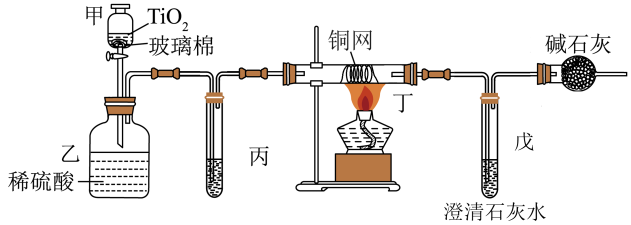
将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol·L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
1.⑴乙中反应的离子方程式为______________________________________________ 。
2.⑵乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__________ (填字母)
a.饱和食盐水 b.饱和NaHCO3溶液 c.浓NaOH溶液 d.浓硫酸
3.⑶丁在实验中的作用是____________________________________________________ ,
装有碱石灰的干燥管的作用是___________________________________________ 。
4.⑷戊中盛有含Ca(OH)20.02mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于________________________________ ,请说明该测得值与实际处理的百分率相比偏高还是偏低________________________________ ?简要说明可能的原因____________________________________________________ 。

将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol·L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
1.⑴乙中反应的离子方程式为
2.⑵乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是
a.饱和食盐水 b.饱和NaHCO3溶液 c.浓NaOH溶液 d.浓硫酸
3.⑶丁在实验中的作用是
装有碱石灰的干燥管的作用是
4.⑷戊中盛有含Ca(OH)20.02mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于
您最近一年使用:0次
解题方法
5 . 锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231 ℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为________ 。
(2)用于微电子器件生产的锡粉纯度测定:
①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
②加入过量的Fe2(SO4)3;
③用0.1 000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是__________________ ;此锡粉样品中锡的质量分数:____________ 。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
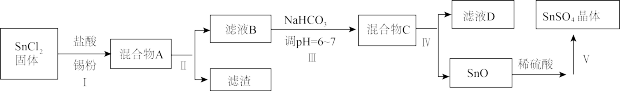
①步骤Ⅰ加入Sn粉的作用:____________________ 及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、________________________ 。
③步骤Ⅲ生成SnO的离子方程式:__________________________ 。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是___________________ ,证明已洗净。
⑤步骤Ⅴ操作依次为___________________ 、过滤、洗涤、低温干燥。
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为:_____________ 。实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是_______________
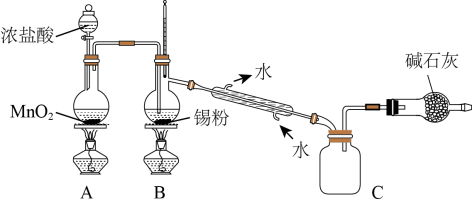
(5)利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是______________________ 。
(1)元素锡比同主族碳的周期数大3,锡的原子序数为
(2)用于微电子器件生产的锡粉纯度测定:
①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
②加入过量的Fe2(SO4)3;
③用0.1 000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
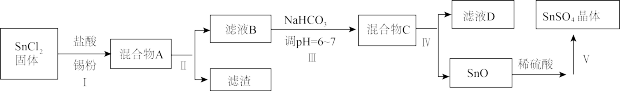
①步骤Ⅰ加入Sn粉的作用:
②步骤Ⅱ用到的玻璃仪器有烧杯、
③步骤Ⅲ生成SnO的离子方程式:
④步骤Ⅳ中检验SnO是否洗涤干净的操作是
⑤步骤Ⅴ操作依次为
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为:

(5)利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是
您最近一年使用:0次
2016-12-09更新
|
257次组卷
|
4卷引用:2015届天津市河西区高三下学期总复习质量调查(二)化学试卷
6 . 某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究。
查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O
探究一:用下图所示装置进行实验,回答下列问题:

(1)仪器组装完成后,夹好止水夹,___________ 。则说明装置A的气密性良好。
(2)装置A是氢气的发生装置,可以选用的药品是___________(填选项)
(3)从下列实验步骤中,选择正确的操作顺序:①___________ ③(填序号)
① 打开止水夹
② 熄灭C处的酒精喷灯
③ C处冷却至室温后,关闭止水夹
④ 点燃C处的酒精喷灯
⑤ 收集氢气并验纯
⑥ 通入气体一段时间,排尽装置内的空气
(4)收集氢气验纯时,最好采用___________ 方法收集氢气。
探究二:
(5)取少量样品于试管中,加入适量的稀硫酸,若无红色物质生成,则说明样品中不含Cu2O;此观点是否正确___________ 。(填“是”或“否”)若填“否”,则原因是___________ (用离子方程式说明);另取少量样品于试管中,加入适量的浓硝酸,产生红棕色的气体。
证明样品中一定含有___________ ,取少量反应后的溶液,加适量蒸馏水稀释后,滴加___________ (填试剂和实验现象),则可证明另一成分存在,反之,说明样品中不含该成分。
探究三:
(6)取一定量样品于烧杯中,加入足量的稀硫酸,若反应后经过滤得到固体3.2g,滤液中Fe2+有1.0mol,则样品中n(Cu2O)=___________ mol。
查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O
探究一:用下图所示装置进行实验,回答下列问题:

(1)仪器组装完成后,夹好止水夹,
(2)装置A是氢气的发生装置,可以选用的药品是___________(填选项)
| A.稀硫酸和锌片 | B.稀硝酸和铁片 | C.氢氧化钠溶液和铝片D.浓硫酸和镁片 |
① 打开止水夹
② 熄灭C处的酒精喷灯
③ C处冷却至室温后,关闭止水夹
④ 点燃C处的酒精喷灯
⑤ 收集氢气并验纯
⑥ 通入气体一段时间,排尽装置内的空气
(4)收集氢气验纯时,最好采用
探究二:
(5)取少量样品于试管中,加入适量的稀硫酸,若无红色物质生成,则说明样品中不含Cu2O;此观点是否正确
证明样品中一定含有
探究三:
(6)取一定量样品于烧杯中,加入足量的稀硫酸,若反应后经过滤得到固体3.2g,滤液中Fe2+有1.0mol,则样品中n(Cu2O)=
您最近一年使用:0次
名校
解题方法
7 . 取某铁铝铜合金9.34g,溶于足量的稀硝酸中,金属无剩余,收集到的一种气体是唯一还原产物。向溶液中加过量的氢氧化钠溶液,小心收集沉淀洗涤干净称重11.23g,加热分解至衡重,得固体质量为8.80g。则下列说法不正确的是
| A.参加反应的氢氧化钠不一定比参加反应的硝酸的物质的量多 |
| B.合金中铁铝的物质的量之比为1:2 |
| C.收集到的气体在标准状况下为4.256L |
| D.与铁铝铜合金反应的硝酸的物质的量是0.57mol |
您最近一年使用:0次
8 . 已知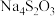 和
和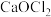 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法不正确 的是
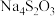 和
和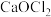 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法A.1mo 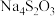 固体中共含有6mol离子 固体中共含有6mol离子 |
B.向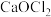 中加入足量稀硫酸会有 中加入足量稀硫酸会有 产生,被氧化与被还原的原子数相等 产生,被氧化与被还原的原子数相等 |
C.向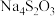 中加入足量稀硫酸时发生反应: 中加入足量稀硫酸时发生反应: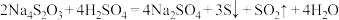 。 。 |
D. 是含有极性键的非极性分子 是含有极性键的非极性分子 |
您最近一年使用:0次
名校
解题方法
9 . 硝酸工业生产中常用纯碱溶液吸收排出的氮氧化物废气,废气中只含有NO、 两种气体。将一定量废气通入到足量的
两种气体。将一定量废气通入到足量的 溶液中被完全吸收,溶液中生成的
溶液中被完全吸收,溶液中生成的 、
、 两种离子的物质的量与废气中
两种离子的物质的量与废气中 的物质的量分数
的物质的量分数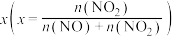 变化关系可用如图所示。
变化关系可用如图所示。
①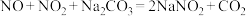 ;
;
②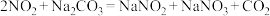 。
。
下列说法不正确的是
 两种气体。将一定量废气通入到足量的
两种气体。将一定量废气通入到足量的 溶液中被完全吸收,溶液中生成的
溶液中被完全吸收,溶液中生成的 、
、 两种离子的物质的量与废气中
两种离子的物质的量与废气中 的物质的量分数
的物质的量分数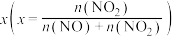 变化关系可用如图所示。
变化关系可用如图所示。
①
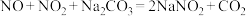 ;
;②
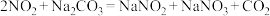 。
。下列说法不正确的是
A.图中线段b表示 离子 离子 |
B.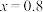 时,反应中可收集到标准状况下44.8L 时,反应中可收集到标准状况下44.8L  |
C.随x值增大,溶液中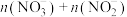 不变 不变 |
D.若测得所得溶液中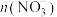 为0.5mol,则x值为0.75 为0.5mol,则x值为0.75 |
您最近一年使用:0次
10 .  电化学循环氧化法将酸性废水中的苯酚降解为
电化学循环氧化法将酸性废水中的苯酚降解为 ,加入
,加入 可加快苯酚的降解,原理如图。已知:
可加快苯酚的降解,原理如图。已知: ,
, 有强氧化性。下列说法错误的是
有强氧化性。下列说法错误的是
 电化学循环氧化法将酸性废水中的苯酚降解为
电化学循环氧化法将酸性废水中的苯酚降解为 ,加入
,加入 可加快苯酚的降解,原理如图。已知:
可加快苯酚的降解,原理如图。已知: ,
, 有强氧化性。下列说法错误的是
有强氧化性。下列说法错误的是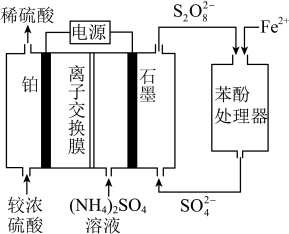
| A.铂连接电源负极,发生还原反应 |
B.石墨上的电极反应: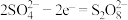 |
C.苯酚降解时发生反应: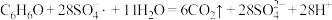 |
D.处理1mol苯酚,有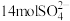 从左向右通过离子交换膜 从左向右通过离子交换膜 |
您最近一年使用:0次
2024-05-12更新
|
287次组卷
|
2卷引用:山东省德州市2024届高三下学期高考适应性练习(二)化学试题



