解题方法
1 . 室温下,下列实验方案能得出相应结论的是
| 选项 | 方案 | 结论 |
| A | 将灼热的木炭加入浓硝酸中,有红棕色气体产生 | 木炭在加热条件下能与浓硝酸反应 |
| B | 将少量 溶于过量的浓盐酸中,再添加几滴 溶于过量的浓盐酸中,再添加几滴 溶液, 溶液, 溶液褪色 溶液褪色 |  中含 中含 离子 离子 |
| C | 向 和 和 的混合溶液中滴入酸化的 的混合溶液中滴入酸化的 溶液震荡,溶液颜色变红 溶液震荡,溶液颜色变红 | 氧化性: |
| D | 向某盐溶液中加入少量浓 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 该溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-19更新
|
297次组卷
|
2卷引用:2024届四川省雅安市天全中学高三下学期模拟预测化学试题
解题方法
2 . 根据下列实验操作及现象,所得结论或解释正确的是
| 选项 | 实验操作和现象 | 结论或解释 |
| A | 将 和另一气体的混合物通入 和另一气体的混合物通入 溶液中,产生白色沉淀 溶液中,产生白色沉淀 | 白色沉淀为 |
| B | 向盛有 和 和 的试管中分别滴加浓盐酸,盛 的试管中分别滴加浓盐酸,盛 的试管中产生黄绿色气体 的试管中产生黄绿色气体 | 氧化性: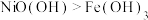 |
| C | 取久置的 粉末,向其中滴加过量的盐酸,得到的气体使澄清石灰水变浑浊 粉末,向其中滴加过量的盐酸,得到的气体使澄清石灰水变浑浊 |  粉末完全变质 粉末完全变质 |
| D | 取两份新制氯水,分别滴加 溶液和淀粉KI溶液,前者有白色沉淀,后者溶液变蓝色 溶液和淀粉KI溶液,前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 某兴趣小组通过下列实验探究 与
与 的氧化性强弱,并对实验原理所涉及的反应进行定性、定量研究。
的氧化性强弱,并对实验原理所涉及的反应进行定性、定量研究。
(1)探究 与
与 的氧化性强弱
的氧化性强弱
【实验 】将
】将 溶液和
溶液和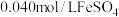 溶液(
溶液( )等体积混合,产生灰黑色沉淀,溶液呈黄色。该条件下,根据实验现象可以判断出氧化性:
)等体积混合,产生灰黑色沉淀,溶液呈黄色。该条件下,根据实验现象可以判断出氧化性:
_____  (填“>”“<”)。
(填“>”“<”)。
(2)验证反应 是可逆反应
是可逆反应
【实验Ⅱ】
①取实验 反应后的上层清液或沉淀进行实验,将表格补充完整。
反应后的上层清液或沉淀进行实验,将表格补充完整。
②根据实验数据,证明该反应为可逆反应,不需要完成表格中编号_____ 的实验。
(3)测定反应 的平衡常数
的平衡常数
测定方案:通过氧化还原滴定法可测定平衡时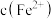 ,再根据实验
,再根据实验 反应物浓度数据计算得出
反应物浓度数据计算得出 和
和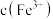 ,进而求算出平衡常数
,进而求算出平衡常数 。
。
【实验Ⅲ】室温下,待实验Ⅰ中反应达到平衡状态时,取 上层清液,用
上层清液,用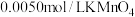 标准溶液滴定
标准溶液滴定 ,达到滴定终点记录消耗
,达到滴定终点记录消耗 标准溶液的体积。重复实验3次,平均消耗
标准溶液的体积。重复实验3次,平均消耗 标准溶液的体积为
标准溶液的体积为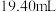 。
。
①用于盛装 标准溶液进行滴定的玻璃仪器名称为
标准溶液进行滴定的玻璃仪器名称为_____ 。
②平衡时
_____  ,平衡常数
,平衡常数
_____ 。
③若取实验 反应后的含
反应后的含 浊液进行实验Ⅱ,会使测得的平衡常数
浊液进行实验Ⅱ,会使测得的平衡常数 值
值_____ 。
A.偏大 B.偏小 C.无影响 D.无法判断
 与
与 的氧化性强弱,并对实验原理所涉及的反应进行定性、定量研究。
的氧化性强弱,并对实验原理所涉及的反应进行定性、定量研究。(1)探究
 与
与 的氧化性强弱
的氧化性强弱【实验
 】将
】将 溶液和
溶液和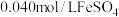 溶液(
溶液( )等体积混合,产生灰黑色沉淀,溶液呈黄色。该条件下,根据实验现象可以判断出氧化性:
)等体积混合,产生灰黑色沉淀,溶液呈黄色。该条件下,根据实验现象可以判断出氧化性:
 (填“>”“<”)。
(填“>”“<”)。(2)验证反应
 是可逆反应
是可逆反应【实验Ⅱ】
①取实验
 反应后的上层清液或沉淀进行实验,将表格补充完整。
反应后的上层清液或沉淀进行实验,将表格补充完整。| 实验编号 | 操作及现象 | 结论 |
| 1 | 取上层黄色清液,滴加 | 存在 |
| 2 | 取少量灰黑色沉淀,滴加浓硝酸,沉淀溶解,出现红棕色气体 | 存在 |
| 3 | 操作及现象是: | 存在 |
| 4 | 取上层清液,滴加 溶液,产生蓝色沉淀 溶液,产生蓝色沉淀 |
(3)测定反应
 的平衡常数
的平衡常数测定方案:通过氧化还原滴定法可测定平衡时
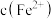 ,再根据实验
,再根据实验 反应物浓度数据计算得出
反应物浓度数据计算得出 和
和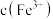 ,进而求算出平衡常数
,进而求算出平衡常数 。
。【实验Ⅲ】室温下,待实验Ⅰ中反应达到平衡状态时,取
 上层清液,用
上层清液,用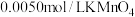 标准溶液滴定
标准溶液滴定 ,达到滴定终点记录消耗
,达到滴定终点记录消耗 标准溶液的体积。重复实验3次,平均消耗
标准溶液的体积。重复实验3次,平均消耗 标准溶液的体积为
标准溶液的体积为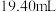 。
。①用于盛装
 标准溶液进行滴定的玻璃仪器名称为
标准溶液进行滴定的玻璃仪器名称为②平衡时

 ,平衡常数
,平衡常数
③若取实验
 反应后的含
反应后的含 浊液进行实验Ⅱ,会使测得的平衡常数
浊液进行实验Ⅱ,会使测得的平衡常数 值
值A.偏大 B.偏小 C.无影响 D.无法判断
您最近一年使用:0次
解题方法
4 . 下列对化学实验及现象的解释合理的是
| 选项 | 化学实验及现象 | 解释 |
| A | 久置的 遇盐酸有气泡产生 遇盐酸有气泡产生 |  已完全转化为 已完全转化为 |
| B |  与 与 光照下反应产生的气体使湿润的蓝色石蕊试纸变红 光照下反应产生的气体使湿润的蓝色石蕊试纸变红 | 气态氯代甲烷溶于水显酸性 |
| C | 向 溶液中加入少量氯水和 溶液中加入少量氯水和 ,振荡、静置,下层溶液为紫红色 ,振荡、静置,下层溶液为紫红色 | 还原性: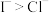 |
| D | 向  溶液中,加入少量 溶液中,加入少量 固体,溶液颜色加深 固体,溶液颜色加深 |  水解程度增大 水解程度增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 用铂丝蘸取某溶液进行焰色反应 | 火焰呈黄色 | 溶液为钠盐溶液 |
B | 取少量溶液于试管中,先加入BaCl2溶液,再滴加稀盐酸, | 产生的白色沉淀不溶解 | 溶液中含 |
C | 将新制氯水和KI溶液在试管中混合后,加入CCl4,振荡静置 | 溶液分层,下层呈紫色 | 还原性: Cl-<I- |
D | 取少量溶液于试管中,滴加几滴新制氯水,振荡,加入KSCN溶液 | 溶液变红色 | 溶液中含有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-18更新
|
576次组卷
|
2卷引用:四川省绵阳南山中学2023届高三下学期高考仿真考试理综化学试题
名校
6 . 南高实验学习小组经查阅资料发现:K2FeO4(Mr=198)为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。现将他们制备高铁酸钾(K2FeO4),测定其纯度并探究其性质的过程展示如下。
(1)制备K2FeO4(夹持装置略)
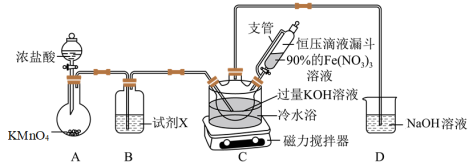
①A为氯气发生装置,盛KMnO4固体的仪器名称是___________ 。
②装置B中所用的试剂X为___________ 。
③装置C中首先制备KClO,然后在快速搅拌下将90%的Fe(NO3)3溶液分批加入装置C中,充分反应得K2FeO4固体,写出该反应的化学方程式___________ 。
(2)K2FeO4的纯度测定
向3mLCrCl3溶液中加入20mL饱和KOH溶液(Cr3++4OH-=CrO +2H2O),再加入5mL蒸馏水,冷却至室温,准确称取1.98g样品,加入上述溶液中使其溶解,充分反应(FeO
+2H2O),再加入5mL蒸馏水,冷却至室温,准确称取1.98g样品,加入上述溶液中使其溶解,充分反应(FeO +CrO
+CrO +2H2O=CrO
+2H2O=CrO +Fe(OH)3↓+OH-),过滤后加入稀硫酸酸化(2CrO
+Fe(OH)3↓+OH-),过滤后加入稀硫酸酸化(2CrO +2H+=Cr2O
+2H+=Cr2O +H2O),并加入1mL苯二胺磺酸钠作指示剂,用1.00mol/L的标准硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定(Cr2O
+H2O),并加入1mL苯二胺磺酸钠作指示剂,用1.00mol/L的标准硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定(Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O),至终点时,消耗(NH4)2Fe(SO4)2溶液的体积为27.00mL。则K2FeO4的质量分数为
+6Fe2++14H+=2Cr3++6Fe3++7H2O),至终点时,消耗(NH4)2Fe(SO4)2溶液的体积为27.00mL。则K2FeO4的质量分数为___________ (过程中杂质不参与反应)。
(3)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2.为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
Ⅰ.方案Ⅰ中溶液变红可知a中含有___________ 离子,但该离子的产生不能判断一定是K2FeO4被Cl-还原得到,还可能由___________ 产生(用离子反应方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是___________ 。
②根据K2FeO4的制备实验得出:氧化性Cl2___________ FeO (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是___________ 。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置,盛KMnO4固体的仪器名称是
②装置B中所用的试剂X为
③装置C中首先制备KClO,然后在快速搅拌下将90%的Fe(NO3)3溶液分批加入装置C中,充分反应得K2FeO4固体,写出该反应的化学方程式
(2)K2FeO4的纯度测定
向3mLCrCl3溶液中加入20mL饱和KOH溶液(Cr3++4OH-=CrO
 +2H2O),再加入5mL蒸馏水,冷却至室温,准确称取1.98g样品,加入上述溶液中使其溶解,充分反应(FeO
+2H2O),再加入5mL蒸馏水,冷却至室温,准确称取1.98g样品,加入上述溶液中使其溶解,充分反应(FeO +CrO
+CrO +2H2O=CrO
+2H2O=CrO +Fe(OH)3↓+OH-),过滤后加入稀硫酸酸化(2CrO
+Fe(OH)3↓+OH-),过滤后加入稀硫酸酸化(2CrO +2H+=Cr2O
+2H+=Cr2O +H2O),并加入1mL苯二胺磺酸钠作指示剂,用1.00mol/L的标准硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定(Cr2O
+H2O),并加入1mL苯二胺磺酸钠作指示剂,用1.00mol/L的标准硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定(Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O),至终点时,消耗(NH4)2Fe(SO4)2溶液的体积为27.00mL。则K2FeO4的质量分数为
+6Fe2++14H+=2Cr3++6Fe3++7H2O),至终点时,消耗(NH4)2Fe(SO4)2溶液的体积为27.00mL。则K2FeO4的质量分数为(3)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2.为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量b,滴加盐酸,有Cl2产生。 |
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是
您最近一年使用:0次
名校
解题方法
7 . 某离子反应中涉及H+、Fe3+、MnO 、FeO
、FeO 、Mn2+、H2O六种粒子,其中MnO
、Mn2+、H2O六种粒子,其中MnO 的浓度随反应进行逐渐增大。下列说法不正确的是
的浓度随反应进行逐渐增大。下列说法不正确的是
 、FeO
、FeO 、Mn2+、H2O六种粒子,其中MnO
、Mn2+、H2O六种粒子,其中MnO 的浓度随反应进行逐渐增大。下列说法不正确的是
的浓度随反应进行逐渐增大。下列说法不正确的是A.该反应的氧化产物为MnO |
| B.氧化剂与还原剂的物质的量之比为5:3 |
C.该溶液中FeO 的氧化性强于MnO 的氧化性强于MnO |
D.溶液中FeO 、Na+、C1-、S2-能大量共存 、Na+、C1-、S2-能大量共存 |
您最近一年使用:0次
2022-07-23更新
|
490次组卷
|
3卷引用:四川省泸州市2021-2022学年高三第一次教学质量诊断性考试理科综合化学试题
名校
解题方法
8 . 如图所示实验装置或方案可以达到预期实验目的的是
 |  |  |  |
| A.用图甲在铁上镀铜 | B.用图乙加热金属钠观察钠燃烧的现象 | C.用图丙验证氧化性有: Cl2>Br2>I2 | D.用图丁进行酸式滴定管排气泡操作 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-26更新
|
485次组卷
|
4卷引用:四川省成都市石室天府中学2024届高三一诊模拟(二)理综-化学试题
名校
解题方法
9 . 下列相关实验方案正确的是
| 选项 | 实验目的 | 实验方案 |
| A | 配制100mL 0.1000 的 的 溶液 溶液 | 将2.5000g  溶于100mL水中并充分搅拌 溶于100mL水中并充分搅拌 |
| B | 证明 有还原性 有还原性 | 向酸性 溶液中滴加少量 溶液中滴加少量 溶液,观察紫色是否变浅 溶液,观察紫色是否变浅 |
| C | 比较S与N元素的非金属性强弱 | 分别测定等浓度 、 、 溶液的pH,通过pH的大小判断 溶液的pH,通过pH的大小判断 |
| D | 证明酸的相对强弱:醋酸>碳酸>硼酸 | 向两只分别盛有0.1mol/L醋酸和饱和硼酸溶液(0.8mol/L)的试管中滴加等浓度的 溶液,观察是否有气体逸出 溶液,观察是否有气体逸出 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-25更新
|
1275次组卷
|
3卷引用:四川省遂宁市2022届高三第二次诊断性考试(二模)理综化学试题
解题方法
10 . 室温下进行下列实验根据实验操作和现象,所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 某气体通入品红溶液中,溶液变红 | 该气体是 |
| B | 向 和KSCN的混合溶液中滴入硝酸酸化的 和KSCN的混合溶液中滴入硝酸酸化的 溶液,溶液变红 溶液,溶液变红 | 氧化性: |
| C | 向盛 溶液的试管中滴加 溶液的试管中滴加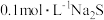 溶液至不再有白色沉淀产生,向其中滴加 溶液至不再有白色沉淀产生,向其中滴加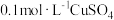 溶液,白色沉淀转化为黑色沉淀 溶液,白色沉淀转化为黑色沉淀 | 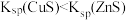 |
| D | 取家用食盐少量,溶于水,加入少量淀粉,充分搅拌后,无明显变化 | 这是一种没有添加碘的食盐 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



