解题方法
1 .  还原
还原 是实现“双碳”经济的有效途径之一。在密闭容器中(
是实现“双碳”经济的有效途径之一。在密闭容器中( 和
和 按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现
按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现 的高效转化。
的高效转化。
 还原
还原 是实现“双碳”经济的有效途径之一。在密闭容器中(
是实现“双碳”经济的有效途径之一。在密闭容器中( 和
和 按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现
按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现 的高效转化。
的高效转化。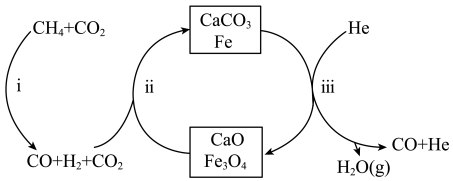
A.该反应的催化剂为 和 和 |
| B.过程iii在恒压条件下通入He,有利于增加CO的产量 |
| C.过程i、ii、iii均涉及置换反应 |
D.每生成4mol的CO,转移的电子数约为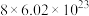 |
您最近一年使用:0次
2 . 水体中氨氮含量超标会造成水体富营养化,用次氯酸钙除去氨氮的原理如图所示。下列说法错误的是
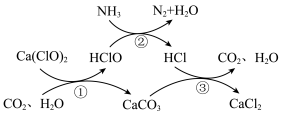
A.标准状况下, 所含的共用电子对数目为 所含的共用电子对数目为 |
B.标准状况下, 所含的原子总数为 所含的原子总数为 |
C.标准状况下, 气体溶于 气体溶于 水中形成的溶液浓度为 水中形成的溶液浓度为 |
D.反应②每生成 消耗 消耗 分子数目为 分子数目为 |
您最近一年使用:0次
解题方法
3 . 在酸性条件下,黄铁矿 催化氧化反应的离子方程式为
催化氧化反应的离子方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
 催化氧化反应的离子方程式为
催化氧化反应的离子方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是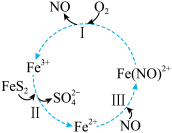
| A.黄铁矿催化氧化中NO作催化剂 |
B.反应Ⅰ的离子方程式为 |
| C.反应Ⅲ是非氧化还原反应 |
D.反应Ⅱ中若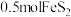 被还原,转移电子的物质的量为 被还原,转移电子的物质的量为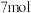 |
您最近一年使用:0次
名校
解题方法
4 . 高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:____________ 。当有1molC参与反应时,该反应转移的电子数是_____________ 。
(2)还原炉中发生的化学反应方程式为:____________ 。
(3)上述工艺生产中循环使用的物质除Si、SiHCl3外,还有_____________ 。
(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为____________ 。
(5)关于硅及其相关化合物的叙述正确的是_____________
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于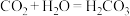 ,因此
,因此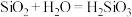
C.硅元素在金属与非金属的分界线处,一般可用于作为半导体材料
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
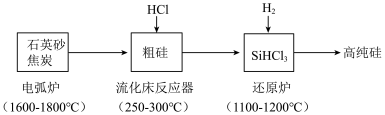
(2)还原炉中发生的化学反应方程式为:
(3)上述工艺生产中循环使用的物质除Si、SiHCl3外,还有
(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
(5)关于硅及其相关化合物的叙述正确的是
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于
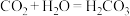 ,因此
,因此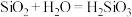
C.硅元素在金属与非金属的分界线处,一般可用于作为半导体材料
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
您最近一年使用:0次
解题方法
5 . 钯(Pd)是航天、航空等高科技领域不可缺少的关键材料。一种从铂钯精矿[含有Pt、Pd、Au、Cu、Bi]中分离提取钯的工艺流程如图所示:
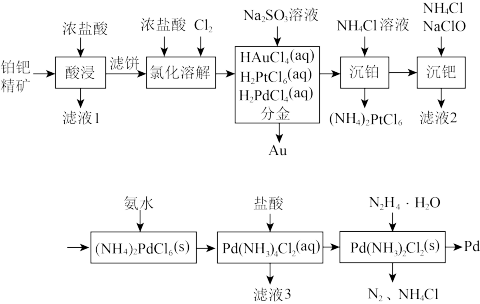
(1)“滤液1”中含有 和
和 ,
, 中Cu的化合价为
中Cu的化合价为________ ;Bi与As在周期表中位于同一主族,基态As原子的简化电子排布式为________ 。
(2)“氯化溶解”时氯气的作用是_________ 。
(3)“分金”时, 的氧化性
的氧化性____ (填“大于”或“小于”)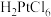 ,理由是
,理由是_____ 。
(4)“沉铂”时发生反应的化学方程式为_________ 。
(5)“沉钯”时反应的化学方程式为___________ 。“滤液3”可以进入到________ 中循环利用。
(6) (水合肼)将
(水合肼)将 还原为金属钯时,还原剂与氧化剂的物质的量之比为
还原为金属钯时,还原剂与氧化剂的物质的量之比为________ 。

(1)“滤液1”中含有
 和
和 ,
, 中Cu的化合价为
中Cu的化合价为(2)“氯化溶解”时氯气的作用是
(3)“分金”时,
 的氧化性
的氧化性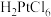 ,理由是
,理由是(4)“沉铂”时发生反应的化学方程式为
(5)“沉钯”时反应的化学方程式为
(6)
 (水合肼)将
(水合肼)将 还原为金属钯时,还原剂与氧化剂的物质的量之比为
还原为金属钯时,还原剂与氧化剂的物质的量之比为
您最近一年使用:0次
2024-04-09更新
|
277次组卷
|
3卷引用:山西省晋中市2024届高三第二次优生测试理综合化学试题-
名校
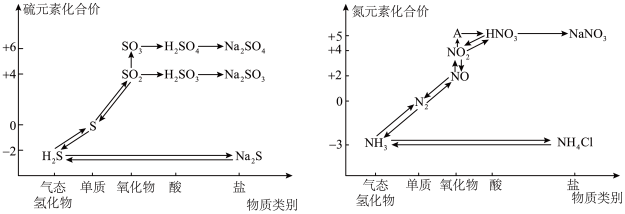
6 . 硫、氮的氧化物都会引起环境问题,越来越引起人们的重视。如图是硫、氮元素的各种价态与物质类别的对应关系:
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为_________ 。
(2)写出浓硫酸与木炭在加热条件下反应的化学方程式:_________________________ ;若要除去 中的
中的 可以使用
可以使用_________ (填试剂名称)。
(3)根据A对应的化合价和物质类别,A为_________ (写分子式)。
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择_________ ,反应的离子方程式为__________________ 。
(5)工业生产中利用氨水吸收 和
和 ,流程如图所示:
,流程如图所示: 被吸收过程的离子方程式是
被吸收过程的离子方程式是_______________________ 。
(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: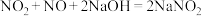
 ;
; 。现有V L某NaOH溶液能完全吸收含m mol NO和n mol
。现有V L某NaOH溶液能完全吸收含m mol NO和n mol  的大气污染物,则NaOH溶液的物质的量浓度至少为
的大气污染物,则NaOH溶液的物质的量浓度至少为________  。若所得溶液
。若所得溶液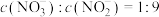 ,则原混合气体中NO和
,则原混合气体中NO和 物质的量之比m∶n=
物质的量之比m∶n=_____ 。
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为
(2)写出浓硫酸与木炭在加热条件下反应的化学方程式:
 中的
中的 可以使用
可以使用(3)根据A对应的化合价和物质类别,A为
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(5)工业生产中利用氨水吸收
 和
和 ,流程如图所示:
,流程如图所示: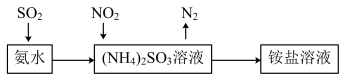
 被吸收过程的离子方程式是
被吸收过程的离子方程式是(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
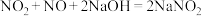
 ;
; 。现有V L某NaOH溶液能完全吸收含m mol NO和n mol
。现有V L某NaOH溶液能完全吸收含m mol NO和n mol  的大气污染物,则NaOH溶液的物质的量浓度至少为
的大气污染物,则NaOH溶液的物质的量浓度至少为 。若所得溶液
。若所得溶液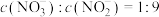 ,则原混合气体中NO和
,则原混合气体中NO和 物质的量之比m∶n=
物质的量之比m∶n=
您最近一年使用:0次
2024-03-26更新
|
319次组卷
|
2卷引用:山西省大同市2023-2024学年高一下学期3月月考化学试题
名校
7 . 大气中 主要来自天然气净化、炼焦、石油精炼、人造丝生产、造纸、橡胶、染料、制药等工业生产过程。将
主要来自天然气净化、炼焦、石油精炼、人造丝生产、造纸、橡胶、染料、制药等工业生产过程。将 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,正确的是
 主要来自天然气净化、炼焦、石油精炼、人造丝生产、造纸、橡胶、染料、制药等工业生产过程。将
主要来自天然气净化、炼焦、石油精炼、人造丝生产、造纸、橡胶、染料、制药等工业生产过程。将 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,正确的是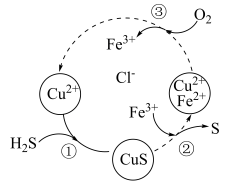
A.过程①中,生成CuS的反应为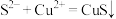 |
B.过程②中, 作还原剂 作还原剂 |
C.过程③中,每消耗1mol  ,转移2mol ,转移2mol  |
D.回收S的总反应为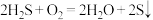 |
您最近一年使用:0次
2024-03-26更新
|
62次组卷
|
3卷引用:山西省大同市2023-2024学年高一下学期3月月考化学试题
名校
8 . 汽车剧烈碰撞时,安全气囊中发生反应:NaN3+KNO3→K2O+Na2O+N2↑(未配平)。对上述反应的描述错误的是
| A.NaN3是还原剂,KNO3是氧化剂 |
| B.该反应中只有1种元素的化合价发生变化 |
| C.配平后物质的化学计量数依次为10、2、1、5、16 |
| D.生成N2的个数与转移电子个数之比为4:5 |
您最近一年使用:0次
2024-03-22更新
|
105次组卷
|
2卷引用:山西省运城市康杰中学2023-2024学年高一下学期化学试题
名校
9 . 为了防止钢铁零件生锈,常采用化学处理使钢铁零件表面生成 ,致密保护层—“发蓝”。化学处理过程中涉及到的反应为
,致密保护层—“发蓝”。化学处理过程中涉及到的反应为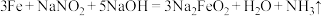 ,下列叙述错误的是
,下列叙述错误的是
 ,致密保护层—“发蓝”。化学处理过程中涉及到的反应为
,致密保护层—“发蓝”。化学处理过程中涉及到的反应为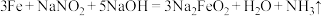 ,下列叙述错误的是
,下列叙述错误的是| A.铁做还原剂,被氧化 | B. 中N元素的化合价为+3价 中N元素的化合价为+3价 |
C.氧化性: | D.反应中每转移3mol电子,生成11.2L |
您最近一年使用:0次
2024-02-22更新
|
124次组卷
|
2卷引用:山西省长治市上党好教育联盟2023-2024学年高一上学期1月期末化学试题
10 . 海洋中的 可以通过借助某些生物酶体系(可以促进
可以通过借助某些生物酶体系(可以促进 和
和 的转移)转化为
的转移)转化为 进入大气层,反应过程如图所示.下列说法错误的是
进入大气层,反应过程如图所示.下列说法错误的是

 可以通过借助某些生物酶体系(可以促进
可以通过借助某些生物酶体系(可以促进 和
和 的转移)转化为
的转移)转化为 进入大气层,反应过程如图所示.下列说法错误的是
进入大气层,反应过程如图所示.下列说法错误的是
A.过程Ⅰ中 是还原产物 是还原产物 |
B.过程Ⅲ中 是氧化剂 是氧化剂 |
C.总反应为 |
D.每生成标准状况下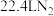 ,总反应中转移 ,总反应中转移 电子 电子 |
您最近一年使用:0次



