20-21高三上·河南南阳·期中
名校
解题方法
1 . 硫酸的工业制备是一个重要的化工生产过程,但在生产过程中会产生大量污染,需要在生产工艺中考虑到绿色工艺.以硫酸工业产生的二氧化硫尾气、氨水、石灰石、焦炭、碳酸氢铵为原料可以合成硫化钙、硫酸铵、亚硫酸铵等物质.合成路线如下:
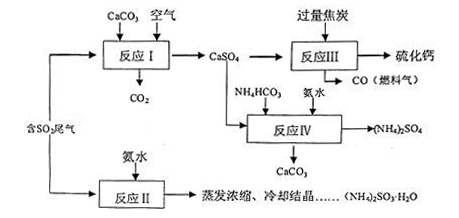
(1)写出反应Ⅰ的化学方程式________________________ .
(2)反应Ⅲ中每生成lmol硫化钙理论上转移电子数________ ;为充分利用副产品CO,有人提出以熔融的K2C03为电解质,设计燃料电池,请写出此电池的负极反应_____________ .
(3)为检验反应Ⅱ得到的产品是否因部分被氧化而变质,需选择的化学试剂有__________________ .
(4)根据合成流程,可以循环利用的是____________ .
(5)(NH4)2SO3溶液可用于电厂产生的烟道气的脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统.写出二氧化氮与亚硫酸铵反应的离子方程式___________________ .

(1)写出反应Ⅰ的化学方程式
(2)反应Ⅲ中每生成lmol硫化钙理论上转移电子数
(3)为检验反应Ⅱ得到的产品是否因部分被氧化而变质,需选择的化学试剂有
(4)根据合成流程,可以循环利用的是
(5)(NH4)2SO3溶液可用于电厂产生的烟道气的脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统.写出二氧化氮与亚硫酸铵反应的离子方程式
您最近一年使用:0次
2017-02-28更新
|
302次组卷
|
4卷引用:专题七 工艺流程题(提分特训)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训
(已下线)专题七 工艺流程题(提分特训)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训河南省南阳市2020届高三上学期期中质量评估化学试题陕西省西安市第一中学2021届高三上学期第五次模拟考试化学试题2016-2017学年辽宁省六校协作体高二下学期期初化学试卷
2022·广东汕头·一模
名校
2 . 2021年,我国科学家首次在实验室实现 到淀粉的全合成,其合成路线如下:设
到淀粉的全合成,其合成路线如下:设 为阿伏加德罗常数,下列有关说法不正确的是
为阿伏加德罗常数,下列有关说法不正确的是
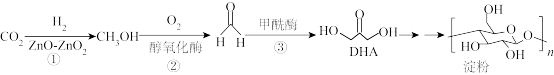
 到淀粉的全合成,其合成路线如下:设
到淀粉的全合成,其合成路线如下:设 为阿伏加德罗常数,下列有关说法不正确的是
为阿伏加德罗常数,下列有关说法不正确的是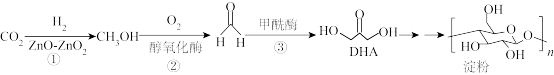
A.标况下,11.2L  中含有共用电子对数目为2 中含有共用电子对数目为2 |
| B.反应②、③无法在高温下进行 |
C.反应②中,3.2g  生成HCHO时转移电子数目为0.2 生成HCHO时转移电子数目为0.2 |
D.1mol DHA与乙酸发生取代反应,可消耗乙酸分子数目为 |
您最近一年使用:0次
2022-03-01更新
|
1424次组卷
|
9卷引用:押广东卷化学第11题 阿伏加德罗常数-备战2022年高考化学临考题号押题(广东卷)
(已下线)押广东卷化学第11题 阿伏加德罗常数-备战2022年高考化学临考题号押题(广东卷)(已下线)第一章 化学计量在实验中的应用(测)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题09 物质的量-备战2023年高考化学母题题源解密(广东卷)广东省汕头市2022届高三下学期第一次模拟考试化学试题北京市通州区2022届高三查缺补漏化学试题北京市顺义牛栏山第一中学2022届高三下学期保温练习化学试题广西南宁市第二中学2021-2022学年高三下学期5月诊断理科综合化学试题北京市第十七中学2021-2022学年高三下学期5月模拟考试化学试题北京市顺义区第一中学2022届高三下学期三模化学试题
名校
3 . 氢氧化铈[Ce(OH)4]是一种重要的稀土氢氧化物。平板电视显示屏生产过程中会产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2),某课题组以此粉末为原料回收铈,设计实验流程如下:
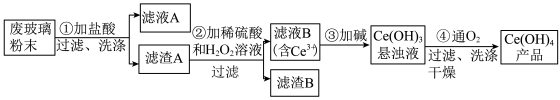
下列说法错误的是

下列说法错误的是
| A.滤渣A中主要含有SiO2、CeO2 |
| B.过滤操作中用到的玻璃仪器有烧杯、漏斗、玻璃棒 |
| C.过程②中发生反应的离子方程式为CeO2+H2O2+3H+=Ce3++2H2O+O2↑ |
| D.过程④中消耗 11.2L O2(已折合成标准状况),转移电子数为2×6.02×1023 |
您最近一年使用:0次
2019-05-31更新
|
1861次组卷
|
12卷引用:专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升
专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专题08 元素及其化合物(测)-2023年高考化学二轮复习讲练测(新高考专用)【市级联考】福建省福州市2019届高三第三次质量检测理科综合化学试题(已下线)【新东方】 2020-17四川省成都市实验中学2020届高考化学模拟试卷(二)河南省商丘市第一高级中学2021-2022学年高一上学期期末考试化学试题河南省南阳市2021-2022学年高一下学期期终质量评估化学试题 陕西省安康中学2023届高三第一次检测性考试化学试题湖北省麻城市实验高级中学2021-2022学年高三下学期第一次联考化学试题天津市静海一中20223-2023学年高三上学期期末定时测验化学试题山东省滕州市第一中学2022-2023学年高一下学期6月月考化学试题天津市第四十七中学2023-2024学年高三上学期第一次阶段性检测化学试题
4 . 硝酸铈铵[(NH4)2Ce(NO3)6]广泛应用于电子、催化工业,其合成路线如下:

(1)已知(NH4)2Ce(NO3)6受热易分解,某科研小组认为反应原理如下,请补充完整:(NH4)2Ce(NO3)6 CeO2·8OH + 8
CeO2·8OH + 8_____ ↑;CeO2·8OH CeO2+ 4H2O↑+2O2↑。
CeO2+ 4H2O↑+2O2↑。
在空气中加热(NH4)2Ce(NO3)6,除固体颜色有变化外,还可观察到的现象是_________ 。
(2)步骤Ⅰ中,将Ce(NO3)3·6H2O配成溶液,保持pH到4~5,缓慢加入H2O2溶液搅拌混合均匀,再加入氨水调节溶液pH,得到Ce(OH)4沉淀。该过程中参加反应的氧化剂与还原剂物质的量之比为___________ 。
(3)298K时,Ksp[Ce(OH)4]=1×10—29。Ce(OH)4的溶度积表达式为Ksp=___________ 。
为了使溶液中Ce4+沉淀完全,即残留在溶液中的c(Ce4+)小于1×10—5mol·L-1,需调节pH为______ 以上。
(4)为了研究步骤Ⅲ的工艺条件,科研小组测定了(NH4)2Ce(NO3)6在不同温度、不同浓度硝酸中的溶解度,结果如图。从图中可得出三条主要规律:

① (NH4)2Ce(NO3)6在硝酸中的溶解度随温度升高而增大;
②_____________________________________________ ;
③_____________________________________________ 。

(1)已知(NH4)2Ce(NO3)6受热易分解,某科研小组认为反应原理如下,请补充完整:(NH4)2Ce(NO3)6
 CeO2·8OH + 8
CeO2·8OH + 8 CeO2+ 4H2O↑+2O2↑。
CeO2+ 4H2O↑+2O2↑。在空气中加热(NH4)2Ce(NO3)6,除固体颜色有变化外,还可观察到的现象是
(2)步骤Ⅰ中,将Ce(NO3)3·6H2O配成溶液,保持pH到4~5,缓慢加入H2O2溶液搅拌混合均匀,再加入氨水调节溶液pH,得到Ce(OH)4沉淀。该过程中参加反应的氧化剂与还原剂物质的量之比为
(3)298K时,Ksp[Ce(OH)4]=1×10—29。Ce(OH)4的溶度积表达式为Ksp=
为了使溶液中Ce4+沉淀完全,即残留在溶液中的c(Ce4+)小于1×10—5mol·L-1,需调节pH为
(4)为了研究步骤Ⅲ的工艺条件,科研小组测定了(NH4)2Ce(NO3)6在不同温度、不同浓度硝酸中的溶解度,结果如图。从图中可得出三条主要规律:

① (NH4)2Ce(NO3)6在硝酸中的溶解度随温度升高而增大;
②
③
您最近一年使用:0次
22-23高三上·安徽芜湖·阶段练习
名校
解题方法
5 . 用 、
、 和
和 为原料催化制乙酸的反应机理如图所示。下列叙述不正确的是
为原料催化制乙酸的反应机理如图所示。下列叙述不正确的是

 、
、 和
和 为原料催化制乙酸的反应机理如图所示。下列叙述不正确的是
为原料催化制乙酸的反应机理如图所示。下列叙述不正确的是
| A.HI是合成乙酸的中间体 |
| B.总反应的原子利用率达到了80% |
C.催化剂可加快 加氢制乙酸平衡之前的反应速率 加氢制乙酸平衡之前的反应速率 |
D.生成乙酸的反应中若消耗22.4 L  (标况下),则转移电子总数为 (标况下),则转移电子总数为 |
您最近一年使用:0次
2022-12-06更新
|
271次组卷
|
3卷引用:专题12 化学反应机理(练)-2023年高考化学二轮复习讲练测(新高考专用)
(已下线)专题12 化学反应机理(练)-2023年高考化学二轮复习讲练测(新高考专用)安徽省芜湖市第一中学2022-2023学年高三上学期12月月考化学试题安徽鼎尖名校联盟2023届高三上学期12月联考化学试题
23-24高三上·河北石家庄·阶段练习
解题方法
6 . 锰酸锂离子蓄电池是第二代锂离子动力电池,性能优良。工业上用某软锰矿(主要成分为MnO2,还含有少量铁、铝及硅等氧化物)为原料制备锰酸锂(LiMn2O4)。流程如图:
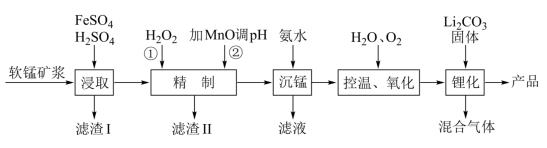
已知:Ksp[Fe(OH)3]=2.6×10-39,,Ksp[Mn(OH)2]=1.6×10-13,Ksp[Fe(OH)2]=4.9×10-17,Ksp[Al(OH)3]=1.0×10-33,lg2≈0.3
(1)“浸取”得到的浸取液中阳离子主要是Mn2+,生成Mn2+的离子方程式为_______ 。
(2)“精制”中加入H2O2的量比理论值大得多,其主要原因是______ ;若Mn2+的浓度为1.0mol•L-1,则加MnO调节pH的范围为_______ (离子浓度≤1.0×10-6mol•L-1时,可认为沉淀完全)。
(3)“沉锰”得到的是Mn(OH)2和Mn2(OH)2SO4滤饼,二者均可被氧化为MnO2,控温氧化时溶液的pH随时间的变化如图,其中pH下降的原因是_______ (用化学方程式表示)。

(4)工业上也可以将“精制”后的滤液加入K2S2O8来合成MnO2,K2S2O8中S元素的化合价为_______ ;此反应的氧化剂和还原剂的物质的量之比为________ 。
(5)“锂化”是将MnO2和Li2CO3按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品。写出反应的化学方程式_______ 。

已知:Ksp[Fe(OH)3]=2.6×10-39,,Ksp[Mn(OH)2]=1.6×10-13,Ksp[Fe(OH)2]=4.9×10-17,Ksp[Al(OH)3]=1.0×10-33,lg2≈0.3
(1)“浸取”得到的浸取液中阳离子主要是Mn2+,生成Mn2+的离子方程式为
(2)“精制”中加入H2O2的量比理论值大得多,其主要原因是
(3)“沉锰”得到的是Mn(OH)2和Mn2(OH)2SO4滤饼,二者均可被氧化为MnO2,控温氧化时溶液的pH随时间的变化如图,其中pH下降的原因是

(4)工业上也可以将“精制”后的滤液加入K2S2O8来合成MnO2,K2S2O8中S元素的化合价为
(5)“锂化”是将MnO2和Li2CO3按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品。写出反应的化学方程式
您最近一年使用:0次
7 . 银及其化合物在制造钱币、电子工业、医药等方面具有广泛用途。
Ⅰ.银的冶炼及性质
(1)热分解法是金属冶炼方法之一。以Ag2O为原料冶炼银的化学方程式为__ 。
(2)电解精炼银的工作原理如图所示,___ (填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成该气体的电极反应式为___ 。
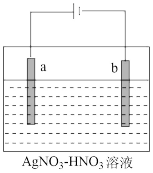
Ⅱ.银的化合物的性质
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式__ 。
(4)在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物。称取34g AgNO3固体,充分光照使其完全分解,测得反应后生成O2的体积(折合成标准状况)为2.24L,反应过程中转移电子的物质的量为__ 。
(5)纳米硫化(Ag2S)应用广泛。Ag2S溶于浓HNO3后,产生淡黄色固体及无色气体,该气体遇空气迅速变为红棕色。写出反应的化学方程式__ 。
Ⅰ.银的冶炼及性质
(1)热分解法是金属冶炼方法之一。以Ag2O为原料冶炼银的化学方程式为
(2)电解精炼银的工作原理如图所示,

Ⅱ.银的化合物的性质
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式
(4)在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物。称取34g AgNO3固体,充分光照使其完全分解,测得反应后生成O2的体积(折合成标准状况)为2.24L,反应过程中转移电子的物质的量为
(5)纳米硫化(Ag2S)应用广泛。Ag2S溶于浓HNO3后,产生淡黄色固体及无色气体,该气体遇空气迅速变为红棕色。写出反应的化学方程式
您最近一年使用:0次
2021-05-03更新
|
598次组卷
|
4卷引用:第二章能力提升检测卷-2022年高考化学一轮复习讲练测
(已下线)第二章能力提升检测卷-2022年高考化学一轮复习讲练测(已下线)第二章 化学物质及其变化(测)-2023年高考化学一轮复习讲练测(全国通用)北京市丰台区2021届高三第二次模拟考试化学试题北京市第三中学2021-2022学年高三上学期期中考试化学试题
20-21高三上·辽宁·期中
解题方法
8 . 硼氢化钠(NaBH4)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33 ℃)。工业上可用硼镁矿(主要成分为Mg2B2O5·H2O,含少量杂质Fe3O4)制取NaBH4,其工艺流程如下:
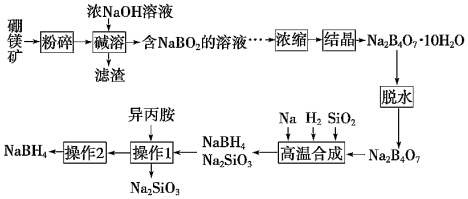
回答下列问题:
(1)NaBH4的电子式为________ 。
(2)碱溶时Mg2B2O5发生反应的化学方程式是________ 。
(3)滤渣的成分是________ 。
(4)高温合成中,加料之前需将反应器加热至100 ℃以上并通入氩气,该操作的目的是____________________ ,原料中的金属钠通常保存在________ 中,实验室取用少量金属钠用到的实验用品有________ 、玻璃片和小刀。
(5)操作2的名称为________ 。流程中可循环利用的物质是________ 。
(6)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1gNaBH4的还原能力相当于________ g H2的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同,计算结果保留两位小数)。

回答下列问题:
(1)NaBH4的电子式为
(2)碱溶时Mg2B2O5发生反应的化学方程式是
(3)滤渣的成分是
(4)高温合成中,加料之前需将反应器加热至100 ℃以上并通入氩气,该操作的目的是
(5)操作2的名称为
(6)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1gNaBH4的还原能力相当于
您最近一年使用:0次



