解题方法
1 . 铅渣由多种氧化物及它们相互结合而形成的化合物、固溶体、共晶混合物所组成。对铅渣进行综合利用,回收其中的有价金属(Cu、Fe、Pb、Zn、Sb)的部分工艺流程如下: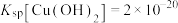 ,
, ,
, 。
。
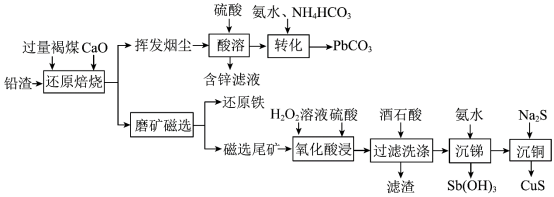
②金属离子浓度等于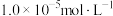 时,可认为其恰好沉淀完全。
时,可认为其恰好沉淀完全。
(1)Sb元素的原子序数为51,与氮元素同主族,其基态电子排布式为[Kr]___________ 。
(2)“还原焙烧”时, 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(3)挥发烟尘中的主要氧化物为 。“转化”过程中,发生反应的离子方程式为
。“转化”过程中,发生反应的离子方程式为___________ 。
(4)“氧化酸浸”过程中,若将物质的量为2mol的 合金(其中Cu与Sb物质的量之比为
合金(其中Cu与Sb物质的量之比为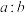 )氧化,至少需要
)氧化,至少需要 的物质的量为
的物质的量为___________ mol(用含a、b的式子表示)。
(5)“过滤洗涤”过程中,加入酒石酸(分子式为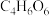 ,结构简式
,结构简式 )发生如下反应:
)发生如下反应: ;
;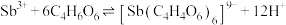 。
。
①上述两个配合物中,提供孤对电子的元素为___________ (填元素符号)。
②“过滤洗涤”时,用酒石酸稀溶液洗涤滤渣而不用水。用酒石酸稀溶液洗涤可减少金属离子的损失,原因为___________ 。
(6)“沉锑”过程中,锑恰好沉淀完全时,溶液中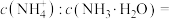
___________ 。
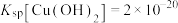 ,
, ,
, 。
。②金属离子浓度等于
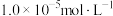 时,可认为其恰好沉淀完全。
时,可认为其恰好沉淀完全。(1)Sb元素的原子序数为51,与氮元素同主族,其基态电子排布式为[Kr]
(2)“还原焙烧”时,
 发生反应的化学方程式为
发生反应的化学方程式为(3)挥发烟尘中的主要氧化物为
 。“转化”过程中,发生反应的离子方程式为
。“转化”过程中,发生反应的离子方程式为(4)“氧化酸浸”过程中,若将物质的量为2mol的
 合金(其中Cu与Sb物质的量之比为
合金(其中Cu与Sb物质的量之比为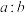 )氧化,至少需要
)氧化,至少需要 的物质的量为
的物质的量为(5)“过滤洗涤”过程中,加入酒石酸(分子式为
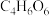 ,结构简式
,结构简式 )发生如下反应:
)发生如下反应: ;
;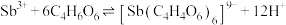 。
。①上述两个配合物中,提供孤对电子的元素为
②“过滤洗涤”时,用酒石酸稀溶液洗涤滤渣而不用水。用酒石酸稀溶液洗涤可减少金属离子的损失,原因为
(6)“沉锑”过程中,锑恰好沉淀完全时,溶液中
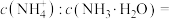
您最近一年使用:0次
解题方法
2 . 氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业氧化锌[含有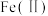 、
、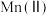 、
、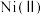 等杂质]的流程如下
等杂质]的流程如下


已知:①在本实验条件下,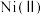 不能被氧化;高锰酸钾的还原产物是
不能被氧化;高锰酸钾的还原产物是 。
。
②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业 粉碎,其目的是
粉碎,其目的是_____ 。
(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和________ ,其中玻璃棒的作用为_________ 。
(3)②发生反应的离子方程式有 和
和________ 。
(4)若④中产物仅为 ,则发生反应的离子方程式为
,则发生反应的离子方程式为________ ;取干燥后的滤饼 ,煅烧后可得到产品(
,煅烧后可得到产品( )
) ,则
,则 等于
等于_____ (用含a、m的代数式表示)。
(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是________ 。
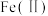 、
、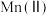 、
、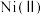 等杂质]的流程如下
等杂质]的流程如下

已知:①在本实验条件下,
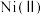 不能被氧化;高锰酸钾的还原产物是
不能被氧化;高锰酸钾的还原产物是 。
。②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业
 粉碎,其目的是
粉碎,其目的是(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和
(3)②发生反应的离子方程式有
 和
和(4)若④中产物仅为
 ,则发生反应的离子方程式为
,则发生反应的离子方程式为 ,煅烧后可得到产品(
,煅烧后可得到产品( )
) ,则
,则 等于
等于(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是
您最近一年使用:0次
解题方法
3 . 高铁酸盐是优良的多功能水处理剂。K2FeO4为紫色固体,可溶于水,微溶于浓KOH溶液,难溶于有机物;在0~5℃、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2.某实验小组制备高铁酸钾(K2FeO4)并测定产品纯度。回答下列问题:
Ⅰ.制备K2FeO4
装置如下图所示,夹持、加热等装置略。___________ ,装置B中除杂质所用试剂是___________ ,装置D的作用是___________ 。
(2)A中发生反应的离子方程式为___________ 。
(3)C中反应为放热反应,而反应温度须控制在0~5℃,反应中KOH必须过量的原因是___________ 。
(4)写出C中总反应的离子方程式:___________ 。C中混合物经重结晶、有机物洗涤纯化、真空干燥,得到高铁酸钾晶体。
Ⅱ.K2FeO4产品纯度的测定
准确称取1.00 g制得的晶体,配成250 mL溶液,准确量取25.00 mL K2FeO4溶液放入锥形瓶,加入足量CrCl3和NaOH溶液,振荡,再加入稀硫酸酸化后得Fe3+和Cr2O ,滴入几滴二苯胺磺酸钠作指示剂,用0.0500 mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗(NH4)2Fe(SO4)2标准溶液28.00 mL。
,滴入几滴二苯胺磺酸钠作指示剂,用0.0500 mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗(NH4)2Fe(SO4)2标准溶液28.00 mL。
(5)根据以上数据,样品中K2FeO4的质量分数为___________ 。若(NH4)2Fe(SO4)2标准溶液部分变质,会使测定结果___________ (填“偏高”“偏低”或“无影响”)。
Ⅰ.制备K2FeO4
装置如下图所示,夹持、加热等装置略。
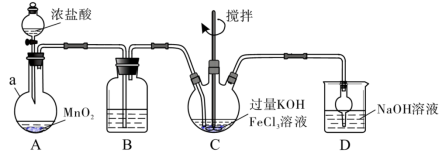
(2)A中发生反应的离子方程式为
(3)C中反应为放热反应,而反应温度须控制在0~5℃,反应中KOH必须过量的原因是
(4)写出C中总反应的离子方程式:
Ⅱ.K2FeO4产品纯度的测定
准确称取1.00 g制得的晶体,配成250 mL溶液,准确量取25.00 mL K2FeO4溶液放入锥形瓶,加入足量CrCl3和NaOH溶液,振荡,再加入稀硫酸酸化后得Fe3+和Cr2O
 ,滴入几滴二苯胺磺酸钠作指示剂,用0.0500 mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗(NH4)2Fe(SO4)2标准溶液28.00 mL。
,滴入几滴二苯胺磺酸钠作指示剂,用0.0500 mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗(NH4)2Fe(SO4)2标准溶液28.00 mL。(5)根据以上数据,样品中K2FeO4的质量分数为
您最近一年使用:0次
4 . 联氨 是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是
是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是
 是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是
是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是A.向装有少量 的试管中加入联氨溶液,可观察到固体逐渐变黑,发生的反应为 的试管中加入联氨溶液,可观察到固体逐渐变黑,发生的反应为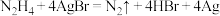 |
B.碱性: |
C.理论上1mol 可处理水中1mol 可处理水中1mol |
D. 是极性分子 是极性分子 |
您最近一年使用:0次
名校
5 . SO2、NOx为常见的空气污染物,会引起酸雨、光化学烟雾等污染问题。为消除燃煤烟气中含有的SO2、NO,研究者以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的pH=5.5,一定时间内,温度对SO2、NO脱除率的影响如图所示:

已知烟气中SO2与NO的体积比为4:1,且吸收后转化为: 、
、 。下列说法正确的是
。下列说法正确的是

已知烟气中SO2与NO的体积比为4:1,且吸收后转化为:
 、
、 。下列说法正确的是
。下列说法正确的是| A.SO2和NO均为酸性氧化物 |
| B.温度越高,“脱硫”“脱硝”效率越高 |
C.SO2在吸收过程中,反应的离子方程式是: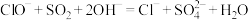 |
D.50℃时,吸收液中烟气转化生成的Cl-和 的物质的量之比13:2 的物质的量之比13:2 |
您最近一年使用:0次
名校
6 . 填空
(1)某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程:
①该反应中的还原剂是______ .
②该反应中,发生还原反应的过程是______ .
③写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目______ .
④如反应转移了0.3mol电子,则产生的气体在标准状况下体积为______ .
(2)在反应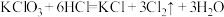 中,还原产物是
中,还原产物是______ ,反应中的氧化剂与还原剂物质的量之比为______ .
(1)某一反应体系有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程:
①该反应中的还原剂是
②该反应中,发生还原反应的过程是
③写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目
④如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
(2)在反应
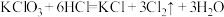 中,还原产物是
中,还原产物是
您最近一年使用:0次
名校
7 . 含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠( )较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。
)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。
(2)我国用 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,用单线桥法表示反应中电子得失的方向和数目:
,用单线桥法表示反应中电子得失的方向和数目:___________ 。将该反应化学方程式改写为离子方程式:___________ 。
(3)工业上可利用 制备亚氯酸钠(
制备亚氯酸钠( ),反应体系中涉及下列6种物质:
),反应体系中涉及下列6种物质: 、
、 、
、 、NaOH、
、NaOH、 、
、 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ 。
(4)某温度下降 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11:1,则
的个数之比为11:1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(5)实验室用下列方法均可制取氯气
① ③
③
② ②
②
③ ④
④
若各反应转移的电子数相同,①②③生成的氯气质量比为___________ 。
(1)亚氯酸钠(
 )较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。
)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。A.NaCl、 | B.NaCl、NaClO |
C. 、 、 | D.NaCl、 |
 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,用单线桥法表示反应中电子得失的方向和数目:
,用单线桥法表示反应中电子得失的方向和数目:(3)工业上可利用
 制备亚氯酸钠(
制备亚氯酸钠( ),反应体系中涉及下列6种物质:
),反应体系中涉及下列6种物质: 、
、 、
、 、NaOH、
、NaOH、 、
、 ,写出反应的化学方程式:
,写出反应的化学方程式:(4)某温度下降
 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11:1,则
的个数之比为11:1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(5)实验室用下列方法均可制取氯气
①
 ③
③②
 ②
②③
 ④
④若各反应转移的电子数相同,①②③生成的氯气质量比为
您最近一年使用:0次
名校
8 . B、Al、Ga位于元素周期表中ⅢA族。 为无色气体,主要用作有机合成中的催化剂,极易水解生成
为无色气体,主要用作有机合成中的催化剂,极易水解生成 (
( 在水中完全电离为
在水中完全电离为 和
和 )和硼酸(
)和硼酸( )。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯
)。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯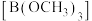 ,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下
,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下 和焦炭在氯气的氛围中获得
和焦炭在氯气的氛围中获得 。GaN的结构与晶体硅类似,是第三代半导体研究的热点。下列化学反应表示
。GaN的结构与晶体硅类似,是第三代半导体研究的热点。下列化学反应表示不正确 的是
 为无色气体,主要用作有机合成中的催化剂,极易水解生成
为无色气体,主要用作有机合成中的催化剂,极易水解生成 (
( 在水中完全电离为
在水中完全电离为 和
和 )和硼酸(
)和硼酸( )。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯
)。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯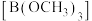 ,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下
,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下 和焦炭在氯气的氛围中获得
和焦炭在氯气的氛围中获得 。GaN的结构与晶体硅类似,是第三代半导体研究的热点。下列化学反应表示
。GaN的结构与晶体硅类似,是第三代半导体研究的热点。下列化学反应表示A.制备 : : |
B. 和NaOH溶液反应: 和NaOH溶液反应: |
C.高温下 、焦炭在氯气中反应: 、焦炭在氯气中反应: |
D.电解 (熔融)制备Al的阳极反应: (熔融)制备Al的阳极反应: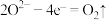 |
您最近一年使用:0次
2023-09-07更新
|
127次组卷
|
2卷引用:湖南省岳阳市第一中学2023-2024学年高三下学期开学化学试题
名校
解题方法
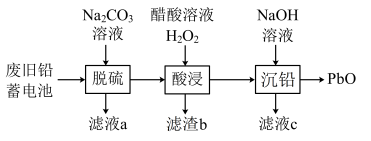
9 . 废旧电池中含有重金属以及电解质溶液,随意丢弃会对环境造成重大污染。以下是对废旧铅蓄电池的回收利用过程,通过此过程最终实现铅的回收。已知废旧铅蓄电池中主要含有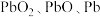 和
和 ,还有少量
,还有少量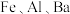 的氧化物等。
的氧化物等。
已知:①一定条件下,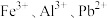 完全生成对应金属氢氧化物沉淀时的pH分别为:3.2、4.6、9.1;
完全生成对应金属氢氧化物沉淀时的pH分别为:3.2、4.6、9.1;
②“脱硫”的反应原理为: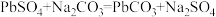 。
。
回答下列问题:
(1)铅蓄电池负极反应是:_______ ,当铅蓄电池工作一段时间,电路中通过的电量为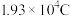 ,则负极增重
,则负极增重_______ g(保留三位有效数字)(已知:电子的电量约为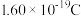 )
)
(2)在“酸浸”中,加入醋酸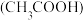 使溶液pH约为4.7,则滤渣b的主要成分有
使溶液pH约为4.7,则滤渣b的主要成分有_______ 。
(3)“酸浸”后溶液中的溶质主要为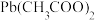 ,请写出
,请写出 与
与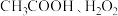 反应的化学方程式
反应的化学方程式_______ ,此反应中 的作用是
的作用是_______ (“氧化剂”、“还原剂”、“既是氧化剂又是还原剂”)。
(4)“沉铅”的滤液c中金属离子有_______ 。
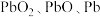 和
和 ,还有少量
,还有少量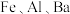 的氧化物等。
的氧化物等。
已知:①一定条件下,
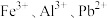 完全生成对应金属氢氧化物沉淀时的pH分别为:3.2、4.6、9.1;
完全生成对应金属氢氧化物沉淀时的pH分别为:3.2、4.6、9.1;②“脱硫”的反应原理为:
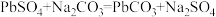 。
。回答下列问题:
(1)铅蓄电池负极反应是:
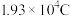 ,则负极增重
,则负极增重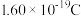 )
)(2)在“酸浸”中,加入醋酸
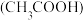 使溶液pH约为4.7,则滤渣b的主要成分有
使溶液pH约为4.7,则滤渣b的主要成分有(3)“酸浸”后溶液中的溶质主要为
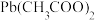 ,请写出
,请写出 与
与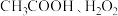 反应的化学方程式
反应的化学方程式 的作用是
的作用是(4)“沉铅”的滤液c中金属离子有
您最近一年使用:0次
2023-05-11更新
|
429次组卷
|
2卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
10 . 下列解释事实的离子方程式正确的是
A.实验室配制的亚铁盐溶液在空气中被氧化: |
B.漂白粉溶液在空气中失效: |
C.向硫酸铜溶液中加入NaHS溶液生成黑色沉淀: |
D.用 做碘量法实验时,溶液pH不可太低,否则溶液变浑浊: 做碘量法实验时,溶液pH不可太低,否则溶液变浑浊: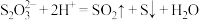 |
您最近一年使用:0次
2023-03-29更新
|
1073次组卷
|
5卷引用:湖南省岳阳市2023届高三下学期教学质量监测(二模)化学试题
湖南省岳阳市2023届高三下学期教学质量监测(二模)化学试题江西省铜鼓中学2022-2023学年高二下学期4月月考化学试题(已下线)狂飙卷 04-【热题狂飙】2023年高考化学样卷(全国卷专用)广东省茂名市第一中学2023届高三下学期模拟预测化学试题(已下线)2019年高考浙江卷化学试题变式题(单选题11-15)



