1 . 黑木耳富含蛋白质、铁、具有还原性的维生素C等,每100 g黑木耳含铁量高达185 mg。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。____________ 。
(2)步骤④检验Fe3+所用试剂是_____________ (填化学式)溶液。
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的阳离子 的离子符号为____________ 。
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。_______ (填序号)。
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为_______________ 。
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是_______________ 。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。
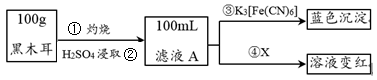
(2)步骤④检验Fe3+所用试剂是
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
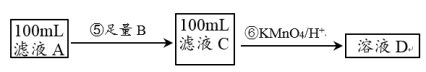
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是
您最近一年使用:0次
名校
解题方法
2 . 氮化硅( )是一种重要的结构陶瓷材料。用石英砂和原料气(含
)是一种重要的结构陶瓷材料。用石英砂和原料气(含 和少量
和少量 )制备
)制备 的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物):
的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物):
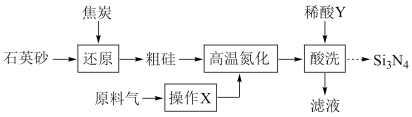
下列叙述不正确的是
 )是一种重要的结构陶瓷材料。用石英砂和原料气(含
)是一种重要的结构陶瓷材料。用石英砂和原料气(含 和少量
和少量 )制备
)制备 的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物):
的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物):
下列叙述不正确的是
A.“还原”主要被氧化为 |
B.“高温氮化”反应的化学方程式为 |
| C.“操作X”可将原料气通过灼热的铜粉 |
| D.“稀酸Y”可选用稀硝酸 |
您最近一年使用:0次
2023-03-07更新
|
410次组卷
|
13卷引用:湖南省娄底市双峰县第一中学2023届高三第七次月考化学试题
湖南省娄底市双峰县第一中学2023届高三第七次月考化学试题江苏省南京市、盐城市2022届高三年级第二次模拟考试化学试题江苏省南京市、盐城市2022届高三第二次模拟化学试题(已下线)必刷卷04-2022年高考化学考前信息必刷卷(江苏专用)(已下线)押江苏卷第9题 化学工艺流程选择题 -备战2022年高考化学临考题号押题(江苏卷)广东省广州市育才中学2021-2022学年高一下学期期中考试化学试题江苏省南京市六校联合体2021-2022高一下学期期中考试化学试题河南省禹州市2021-2022学年高一下学期期末调研考试化学试题江苏省泰州中学2022-2023学年高三上学期第一次月度检测化学试题进阶训练3湖南省邵阳市第一中学2023届高三第七次月考化学试题江苏省南通市海安高级中学2022-2023学年高一下学期第一次月考化学试题广东省广州科学城中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
3 . 下列离子方程式正确的是
| A.磁性氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++H2O |
| B.四氯化钛的浓溶液制备水合二氧化钛:Ti4++(x+2)H2O=TiO2·xH2O↓+4H+ |
C.水玻璃中通入少量CO2:Na2SiO3+CO2+H2O=CO +H2SiO3↓+2Na+ +H2SiO3↓+2Na+ |
D.酸性KMnO4溶液滴定双氧水:2MnO +H2O2+6H+=2Mn2++3O2↑+4H2O +H2O2+6H+=2Mn2++3O2↑+4H2O |
您最近一年使用:0次
2022-05-20更新
|
345次组卷
|
4卷引用:湖南省娄底市双峰县第一中学2023届高三下学期第五次月考化学试题
湖南省娄底市双峰县第一中学2023届高三下学期第五次月考化学试题(已下线)化学-2022年高考考前押题密卷(北京卷)(已下线)1.2.2 离子反应和离子方程式(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)?湖南省株洲市第八中学2022-2023学年高三上学期第五次月考化学试题
解题方法
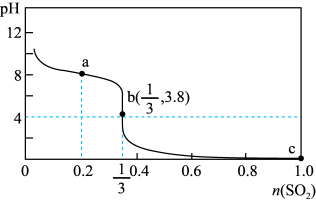
4 . 常温下,向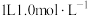 的NaClO溶液中缓慢通入
的NaClO溶液中缓慢通入 气体,使其充分吸收,溶液pH与通入
气体,使其充分吸收,溶液pH与通入 的物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
的物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
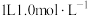 的NaClO溶液中缓慢通入
的NaClO溶液中缓慢通入 气体,使其充分吸收,溶液pH与通入
气体,使其充分吸收,溶液pH与通入 的物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
的物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
A.常温下,HClO电离平衡常数的数量级为 |
| B.水的电离程度:a<b<c |
C.b点溶液中: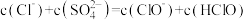 |
D.c点溶液中: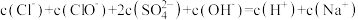 |
您最近一年使用:0次
名校
5 . 二氧化氯(ClO2)是广泛应用的高效安全消毒剂。
(1)ClO2性质活泼,气体及水溶液均不能稳定存在,使用时需现场制备或用稳定剂吸收、转化。用 和
和 将ClO2转化为
将ClO2转化为 ,的反应装置如图1,已知反应放出大量的热,且温度高于60℃时
,的反应装置如图1,已知反应放出大量的热,且温度高于60℃时 分解生成
分解生成 和
和 。
。
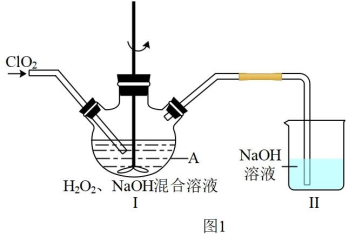
①仪器A的名称为_______ ,写出A中发生反应的化学方程式_______ 。
②实验时吸收液中 和
和 的物料比小于反应的化学计量数之比,原因可能是
的物料比小于反应的化学计量数之比,原因可能是_______ ;为提高 吸收率,在不改变吸收液的物料比的条件下,可以改进的措施是
吸收率,在不改变吸收液的物料比的条件下,可以改进的措施是_______ (写出一点即可)。
(2)用 处理过的饮用水常含有一定量的
处理过的饮用水常含有一定量的 ,饮用水中
,饮用水中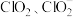 的含量可用连续碘量法进行测定。
的含量可用连续碘量法进行测定。 被
被 还原为
还原为 或
或 的转化率与溶液的
的转化率与溶液的 关系如图2所示。反应生成的
关系如图2所示。反应生成的 用标准
用标准 溶液滴定:
溶液滴定: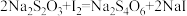 。
。
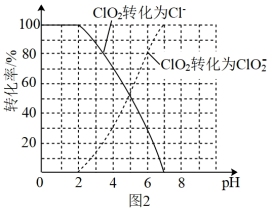
滴定过程为:准确量取VmL水样加入到碘量瓶中,调节水样的 为
为 ,加入足量的
,加入足量的 晶体,充分反应后,用
晶体,充分反应后,用 溶液滴定至淡黄色,加入淀粉溶液,滴定至第一次终点,消耗
溶液滴定至淡黄色,加入淀粉溶液,滴定至第一次终点,消耗 溶液
溶液 ;调节溶液的pH≤2.0,继续用
;调节溶液的pH≤2.0,继续用 溶液滴定至第二次终点,消耗
溶液滴定至第二次终点,消耗 溶液
溶液 。
。
①写出当pH≤2.0时, 与
与 反应的离子方程式
反应的离子方程式_______ 。
②两次滴定终点的现象_______ (填“相同”或“不相同”),根据上述数据,测得该水样中的 浓度为
浓度为_______  (用含字母的代数式表示)。
(用含字母的代数式表示)。
③滴定所用碘量瓶(如图3,瓶口为喇叭形,磨口玻璃塞与瓶口间可形成一圈水槽),加入水样和KI晶体后,盖上磨口塞并加蒸馏水液封,滴定前打开瓶塞,让水流下,并用少量水冲洗瓶塞和内壁,该操作的目的是_______ 。

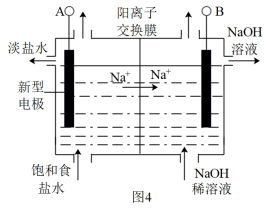
(3)图4为新型电极材料电解食盐水制取ClO2和烧碱的装置示意图。则A极为_______ 极,B极的电极反应式为_______ 。
(1)ClO2性质活泼,气体及水溶液均不能稳定存在,使用时需现场制备或用稳定剂吸收、转化。用
 和
和 将ClO2转化为
将ClO2转化为 ,的反应装置如图1,已知反应放出大量的热,且温度高于60℃时
,的反应装置如图1,已知反应放出大量的热,且温度高于60℃时 分解生成
分解生成 和
和 。
。
①仪器A的名称为
②实验时吸收液中
 和
和 的物料比小于反应的化学计量数之比,原因可能是
的物料比小于反应的化学计量数之比,原因可能是 吸收率,在不改变吸收液的物料比的条件下,可以改进的措施是
吸收率,在不改变吸收液的物料比的条件下,可以改进的措施是(2)用
 处理过的饮用水常含有一定量的
处理过的饮用水常含有一定量的 ,饮用水中
,饮用水中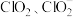 的含量可用连续碘量法进行测定。
的含量可用连续碘量法进行测定。 被
被 还原为
还原为 或
或 的转化率与溶液的
的转化率与溶液的 关系如图2所示。反应生成的
关系如图2所示。反应生成的 用标准
用标准 溶液滴定:
溶液滴定: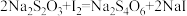 。
。
滴定过程为:准确量取VmL水样加入到碘量瓶中,调节水样的
 为
为 ,加入足量的
,加入足量的 晶体,充分反应后,用
晶体,充分反应后,用 溶液滴定至淡黄色,加入淀粉溶液,滴定至第一次终点,消耗
溶液滴定至淡黄色,加入淀粉溶液,滴定至第一次终点,消耗 溶液
溶液 ;调节溶液的pH≤2.0,继续用
;调节溶液的pH≤2.0,继续用 溶液滴定至第二次终点,消耗
溶液滴定至第二次终点,消耗 溶液
溶液 。
。①写出当pH≤2.0时,
 与
与 反应的离子方程式
反应的离子方程式②两次滴定终点的现象
 浓度为
浓度为 (用含字母的代数式表示)。
(用含字母的代数式表示)。③滴定所用碘量瓶(如图3,瓶口为喇叭形,磨口玻璃塞与瓶口间可形成一圈水槽),加入水样和KI晶体后,盖上磨口塞并加蒸馏水液封,滴定前打开瓶塞,让水流下,并用少量水冲洗瓶塞和内壁,该操作的目的是

(3)图4为新型电极材料电解食盐水制取ClO2和烧碱的装置示意图。则A极为

您最近一年使用:0次
2022-04-14更新
|
1079次组卷
|
7卷引用:湖南省涟源市第一中学2023届高三第五次月考化学试题
湖南省涟源市第一中学2023届高三第五次月考化学试题安徽省宣城市2022届高三第二次调研理综测试试题(已下线)押江苏卷第17题 化学实验综合题 -备战2022年高考化学临考题号押题(江苏卷)湖南省常德市澧县一中2021-2022学年高三下学期期中考试化学试题(已下线)微专题20 新型含氯化合物的制备与性质探究(ClO2、NOCl等)-备战2023年高考化学一轮复习考点微专题湖南省常德市澧县第一中学2021-2022学年高三下学期期中考试化学试题湖南省攸县第一中学2022-2023学年高三第六次月考化学试题
名校
解题方法
6 . 硫脲[ ]是一种白色晶体,熔点180℃,易溶于水和乙醇,受热时部分发生异构化反应而生成硫氰化铵,可用于制造药物,也可用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
]是一种白色晶体,熔点180℃,易溶于水和乙醇,受热时部分发生异构化反应而生成硫氰化铵,可用于制造药物,也可用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
I.硫脲的制备:
已知:将石灰氮( )和水的混合物加热至80℃时,通入硫化氢气体反应可生成硫脲溶液和石灰乳,实验装置如图所示。
)和水的混合物加热至80℃时,通入硫化氢气体反应可生成硫脲溶液和石灰乳,实验装置如图所示。
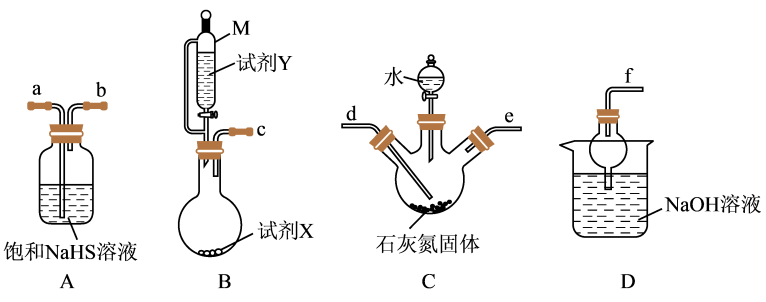
(1)装置B中的试剂X和试剂Y的最佳组合是_______ (填序号)。
A. 固体+浓硫酸 B.
固体+浓硫酸 B. 固体+稀硝酸 C.
固体+稀硝酸 C. 固体+稀盐酸
固体+稀盐酸
(2)仪器M的名称为_______ 。按(1)中所选试剂组合,按气流从左到右的方向,上述装置的合理连接顺序为c→_______ (填仪器接口的小写字母)。
(3)装置C中反应温度控制在80℃,温度不宜过高或过低的原因是_______ ,装置C中反应的化学方程式为_______ 。
II.硫脲的分离及产品含量的测定:
(4)装置C反应后的液体过滤后,将滤液减压蒸发浓缩,之后冷却结晶,离心分离,烘干即可得到产品。称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用 标准溶液滴定,滴定至终点时消耗
标准溶液滴定,滴定至终点时消耗 标准溶液
标准溶液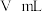 。
。
①硫脲[ ]中硫元素的化合价为
]中硫元素的化合价为_______ 价。
②滴定时,硫脲转化为 、
、 、
、 的离子方程式为
的离子方程式为_______ 。
③样品中硫脲的质量分数为_______ (用含“m,c、V”的式子表示)。
 ]是一种白色晶体,熔点180℃,易溶于水和乙醇,受热时部分发生异构化反应而生成硫氰化铵,可用于制造药物,也可用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:
]是一种白色晶体,熔点180℃,易溶于水和乙醇,受热时部分发生异构化反应而生成硫氰化铵,可用于制造药物,也可用作橡胶的硫化促进剂以及金属矿物的浮选剂等。回答下列问题:I.硫脲的制备:
已知:将石灰氮(
 )和水的混合物加热至80℃时,通入硫化氢气体反应可生成硫脲溶液和石灰乳,实验装置如图所示。
)和水的混合物加热至80℃时,通入硫化氢气体反应可生成硫脲溶液和石灰乳,实验装置如图所示。
(1)装置B中的试剂X和试剂Y的最佳组合是
A.
 固体+浓硫酸 B.
固体+浓硫酸 B. 固体+稀硝酸 C.
固体+稀硝酸 C. 固体+稀盐酸
固体+稀盐酸(2)仪器M的名称为
(3)装置C中反应温度控制在80℃,温度不宜过高或过低的原因是
II.硫脲的分离及产品含量的测定:
(4)装置C反应后的液体过滤后,将滤液减压蒸发浓缩,之后冷却结晶,离心分离,烘干即可得到产品。称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用
 标准溶液滴定,滴定至终点时消耗
标准溶液滴定,滴定至终点时消耗 标准溶液
标准溶液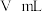 。
。①硫脲[
 ]中硫元素的化合价为
]中硫元素的化合价为②滴定时,硫脲转化为
 、
、 、
、 的离子方程式为
的离子方程式为③样品中硫脲的质量分数为
您最近一年使用:0次
2022-04-10更新
|
1107次组卷
|
11卷引用:湖南省娄底市双峰县第一中学2023届高三下学期第五次月考化学试题
湖南省娄底市双峰县第一中学2023届高三下学期第五次月考化学试题河北省保定市2022届高三第一次模拟考试(一模)化学试题(已下线)化学-2022年高考考前押题密卷(福建卷)江西省南昌市第二中学2022-2023学年高三上学期第四次考试化学试题(已下线)化学(辽宁B卷)-学易金卷:2023年高考第一次模拟考试卷天天练11-15辽宁省本溪市高级中学2023届高三下学期第一次摸底考试化学试题河南省淮滨高级中学2022-2023学年高二下学期期中教学质量检测化学试题河南省信阳市第十高级中学2022-2023学年高二下学期期中教学质量检测化学试卷福建省厦门第一中学2022-2023学年高三上学期11月期中考试化学试题(已下线)实验综合题
名校
解题方法
7 . 实验室用N2H4(肼,又名联氨,常温下为无色油状液体,沸点为113.5 ℃,具有与氨相似的气味,有弱碱性和较强的还原性)还原Cu(OH)2制备纳米Cu2O的装置(部分加热装置已省略)如图所示:已知:NaNO2溶液与NH4Cl溶液反应能得到N2。

下列说法不正确的是

下列说法不正确的是
| A.装置②⑥中分别盛装浓硫酸和稀硫酸 |
| B.无水硫酸铜由白色变为蓝色说明从装置④中出来的气体中含有水蒸气 |
C.装置④中发生反应的化学方程式为N2H4+4Cu(OH)2 2Cu2O+N2↑+6H2O 2Cu2O+N2↑+6H2O |
| D.加入反应试剂后,先打开K2,待装置④中反应完且冷却至室温,再打开K1排尽装置中的N2H4 |
您最近一年使用:0次
2022-03-31更新
|
981次组卷
|
9卷引用:湖南省娄底市双峰县第一中学2023届高三下学期第五次月考化学试题
湖南省娄底市双峰县第一中学2023届高三下学期第五次月考化学试题湖南省常德市第二中学2021届高三上学期开学考试化学试题(已下线)专题14 无机综合运用(选择题)-2022年高考化学二轮复习重点专题常考点突破练湖南省邵阳邵东市第一中学2021-2022学年高一下学期第一次月考化学试题重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题福建省龙岩第一中学2022届高三下学期第一次模拟考试化学试题江苏省前黄高级中学2021-2022学年高一下学期4月调研考试化学试题河南省平顶山第一中学2022-2023学年高一下学期校内质量检测(一)化学试题福建省福州延安中学2023-2024学年高三上学期期中考试化学试题
8 . 请按要求回答下列问题:
(1)钠在空气中燃烧生成淡黄色的固体,则其化学方程式为___________ ;
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则是一种___________ (填“酸性”、“碱性”或“两性”)氧化物;
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式___________ ;
(4)氨气极易溶于水,其水溶液显___________ (填“酸”、“碱”或“中”)性;
(5)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“氧化”)性;
(6)向试管中的品红溶液中通入一段时间的SO2,观察到品红溶液褪色,然后再加热试管,已褪色的溶液___________ (填“恢复”或“不恢复”)红色。
(7)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式___________ ;
(1)钠在空气中燃烧生成淡黄色的固体,则其化学方程式为
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则是一种
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式
(4)氨气极易溶于水,其水溶液显
(5)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出(6)向试管中的品红溶液中通入一段时间的SO2,观察到品红溶液褪色,然后再加热试管,已褪色的溶液
(7)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式
您最近一年使用:0次
2022-02-15更新
|
578次组卷
|
2卷引用:湖南省娄底市新化县2021-2022学年高一上学期期末考试化学试题
9 . 工业用强氧化剂 PbO2来制备 KClO4的工业流程如图:
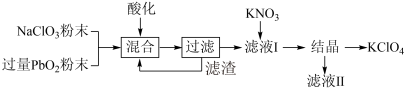
下列判断不正确的是

下列判断不正确的是
| A.“滤渣”的主要成分是 PbO2,可循环使用 |
| B.“酸化”的试剂可用浓盐酸 |
| C.NaClO3与 PbO2反应的物质的量之比为1:1 |
| D.在滤液1中加入 KNO3制得 KClO4利用的是体系中各物质溶解度不同 |
您最近一年使用:0次
2021-03-19更新
|
676次组卷
|
4卷引用:湖南省娄底市第五中学2021-2022学年高三下学期期中考试化学试题
湖南省娄底市第五中学2021-2022学年高三下学期期中考试化学试题山东省德州市2021届高三下学期高考第一次模拟考试化学试题(已下线)第06讲 氧化还原反应(精练)-2022年高考化学一轮复习讲练测(已下线)专题12 工艺流程选择题-备战2022年高考化学真题及地市好题专项集训【山东专用】
解题方法
10 . (1)写出下列物质在水溶液中的电离方程式:
①KOH:_______________________________________________ ;
②KHSO4:____________________________________________ ;
③Fe2(SO4)3:__________________________________________ ;
(2)写出下列反应的离子方程式:
④Ba(OH)2溶液和H2SO4溶液反应________________________________________ ;
⑤Na2CO3溶液和HNO3溶液反应_________________________________________ ;
(3)配平下列方程式
⑥ NaClO3+ SO2+ H2SO4= ClO2+ NaHSO4_________________________________________ ;
⑦ Cl-+ MnO + H+= Mn2++ Cl2↑+ H2O
+ H+= Mn2++ Cl2↑+ H2O_________________________________________ 。
①KOH:
②KHSO4:
③Fe2(SO4)3:
(2)写出下列反应的离子方程式:
④Ba(OH)2溶液和H2SO4溶液反应
⑤Na2CO3溶液和HNO3溶液反应
(3)配平下列方程式
⑥ NaClO3+ SO2+ H2SO4= ClO2+ NaHSO4
⑦ Cl-+ MnO
 + H+= Mn2++ Cl2↑+ H2O
+ H+= Mn2++ Cl2↑+ H2O
您最近一年使用:0次



