名校
解题方法
1 . 五氧化二氮(N2O5)是有机合成中常用的绿色硝化剂。N2O5常温下为白色固体,可溶于CH2Cl2等氯代经溶剂,微溶于水且与水反应生成强酸,高于室温时对热不稳定。
(1)某化学兴趣小组设计臭氧(O3)氧化法制备N2O5,反应原理为N2O4+O3=N2O5+O2。实验装置如图:

回答下列问题:
①装置C的名称__ ,装置E的作用是__ 。
②写出装置A中发生反应的化学方程式__ 。
③实验时,将装置C浸入__ (填“热水”或“冰水”)中,打开装置A中分液漏斗的活塞,一段时间后C中液体变为红棕色。关闭分液漏斗的活塞,打开活塞K,通过臭氧发生器向装置C中通入含有臭氧的氧气。
(2)判断C中反应已结束的简单方法是__ 。
(3)该兴趣小组用滴定法测定N2O5粗产品中N2O4的含量。取2.0g粗产品,加入20.00mL0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。(已知:H2O2与HNO3不反应且不考虑其分解)
①产品中N2O4与KMnO4发生反应的离子方程式为__ 。
②判断滴定终点的方法是__ 。
③产品中N2O4的质量分数为__ 。
(1)某化学兴趣小组设计臭氧(O3)氧化法制备N2O5,反应原理为N2O4+O3=N2O5+O2。实验装置如图:

回答下列问题:
①装置C的名称
②写出装置A中发生反应的化学方程式
③实验时,将装置C浸入
(2)判断C中反应已结束的简单方法是
(3)该兴趣小组用滴定法测定N2O5粗产品中N2O4的含量。取2.0g粗产品,加入20.00mL0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。(已知:H2O2与HNO3不反应且不考虑其分解)
①产品中N2O4与KMnO4发生反应的离子方程式为
②判断滴定终点的方法是
③产品中N2O4的质量分数为
您最近一年使用:0次
2021-12-19更新
|
736次组卷
|
7卷引用:陕西省汉中市2021-2022学年高三上学期教学质量第一次检测考试化学试题
陕西省汉中市2021-2022学年高三上学期教学质量第一次检测考试化学试题山东省滨州市2021-2022学年高三上学期第一次检测化学试题(已下线)专题36 物质的制备及实验方案的设计与评价(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练内蒙古包钢第一中学2021-2022学年高三下学期一模检测(B)化学试题湖南师范大学附属中学2021-2022学年高三下学期第六次月考化学试题(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)湖南省株洲市第八中学021-2022学年高三下学期5月月考化学试题
解题方法
2 . 钛白粉(纳米级TiO2)广泛用作功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料,是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。以钛铁矿(主要成分为FeTiO3、MgO)为原料制备高纯度钛白粉,同时得到绿矾的工艺流程如图1。
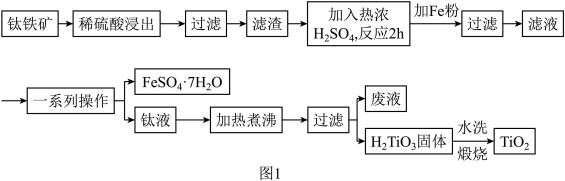
已知:常温下,稀硫酸几乎与FeTiO3不反应。
(1)稀硫酸浸出的目的是___________ 。
(2)图2、图3分别为不同固液比、温度下滤渣与热浓硫酸反应时的Ti浸出率,据图分析,最适合的固液比和温度分别是___________ 和___________ ,原因为___________ 。

(3)若用浓硫酸浸出后Ti元素的存在形式为 ,则浓硫酸与FeTiO3反应的化学方程式为
,则浓硫酸与FeTiO3反应的化学方程式为___________ 。
(4)“一系列操作”得到的绿矾先用稀钛液洗涤,再用冰水洗涤的目的是___________ ,过滤时用到的玻璃仪器有玻璃棒、___________ 。
(5)将钛液加热煮沸的目的是___________ 。
(6)若取10kg钛铁矿(FeTiO3的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为___________ kg。

已知:常温下,稀硫酸几乎与FeTiO3不反应。
(1)稀硫酸浸出的目的是
(2)图2、图3分别为不同固液比、温度下滤渣与热浓硫酸反应时的Ti浸出率,据图分析,最适合的固液比和温度分别是

(3)若用浓硫酸浸出后Ti元素的存在形式为
 ,则浓硫酸与FeTiO3反应的化学方程式为
,则浓硫酸与FeTiO3反应的化学方程式为(4)“一系列操作”得到的绿矾先用稀钛液洗涤,再用冰水洗涤的目的是
(5)将钛液加热煮沸的目的是
(6)若取10kg钛铁矿(FeTiO3的质量分数为95%,)经过上述流程(钛元素在整个流程中损失率为5%),则可制得钛白粉固体的质量为
您最近一年使用:0次
3 .  具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。
(1)实验室检验 的方法为
的方法为_______ 。 溶液对钢铁设备的腐蚀,除
溶液对钢铁设备的腐蚀,除 的腐蚀作用外,另一离子的腐蚀主要原因是
的腐蚀作用外,另一离子的腐蚀主要原因是_______ (用离子方程式表示)
(2)实验室可用NaClO氧化酸性 废液得到
废液得到 ,发生反应的离子方程式为
,发生反应的离子方程式为_______ 。若要制取1000mL2mol/L ,则需要NaClO的质量为
,则需要NaClO的质量为_______ g。
(3)通过控制条件, 溶液的水解产物聚合,生成聚合氯化铁,离子方程式为
溶液的水解产物聚合,生成聚合氯化铁,离子方程式为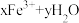
 。欲使平衡正向移动可采用的方法是_______(填字母)。
。欲使平衡正向移动可采用的方法是_______(填字母)。
(4)工业上可用废铁屑来制备 ,流程如下:
,流程如下:
废铁屑
 晶体
晶体 无水
无水
①在HCl气流中加热的原因是_______ 。
②若某废铁屑中铁的质量分数为84%,用1000g废铁屑反应,最后制取的 质量为1625g,则该制取过程中的产率为
质量为1625g,则该制取过程中的产率为_______ (精确到0.1%)
 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。(1)实验室检验
 的方法为
的方法为 溶液对钢铁设备的腐蚀,除
溶液对钢铁设备的腐蚀,除 的腐蚀作用外,另一离子的腐蚀主要原因是
的腐蚀作用外,另一离子的腐蚀主要原因是(2)实验室可用NaClO氧化酸性
 废液得到
废液得到 ,发生反应的离子方程式为
,发生反应的离子方程式为 ,则需要NaClO的质量为
,则需要NaClO的质量为(3)通过控制条件,
 溶液的水解产物聚合,生成聚合氯化铁,离子方程式为
溶液的水解产物聚合,生成聚合氯化铁,离子方程式为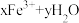
 。欲使平衡正向移动可采用的方法是_______(填字母)。
。欲使平衡正向移动可采用的方法是_______(填字母)。| A.降温 | B.加水稀释 | C.加入 | D.加入 |
 ,流程如下:
,流程如下:废铁屑

 晶体
晶体 无水
无水
①在HCl气流中加热的原因是
②若某废铁屑中铁的质量分数为84%,用1000g废铁屑反应,最后制取的
 质量为1625g,则该制取过程中的产率为
质量为1625g,则该制取过程中的产率为
您最近一年使用:0次
解题方法
4 . 水处理包括水的净化、杀菌消毒等。其中常见的杀菌消毒剂包括氯气、漂白粉、高铁酸钾等。回答下列问题:
(一)氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。
(1)新制氯水呈浅黄绿色,且有刺激性气味,说明有_______ (填化学式)存在;将新制氯水滴入紫色石蕊试液中,可观察到的现象为_______ 。
(2)新制饱和氯水经光照后,其酸性会_______ (填“增大”或“减小”)。
(3)漂白粉的有效成分是_______ ,其与空气中 、
、 反应生成不稳定的次氯酸而易失效,该反应的化学方程式为
反应生成不稳定的次氯酸而易失效,该反应的化学方程式为_______ 。
(二)某工厂的废金属屑中主要成分为 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,该厂用此废金属屑制取新型高效水处理剂
,该厂用此废金属屑制取新型高效水处理剂 (高铁酸钠)等产品的过程如下:
(高铁酸钠)等产品的过程如下:
I.向废金属屑中加入过量的 溶液,充分反应后过滤;
溶液,充分反应后过滤;
II.向I所得固体中加入过量稀 ,充分反应后过滤;
,充分反应后过滤;
III.向II所得固体中继续加入热的稀 ,同时不断鼓入空气,固体全部溶解得
,同时不断鼓入空气,固体全部溶解得 溶液。
溶液。
(4)步骤I过滤后所得滤液的溶质成分为_______ (填化学式)。
(5)步骤II所得滤液经进一步处理可制得 ,流程如下:
,流程如下:

写出由 制取
制取 的化学方程式
的化学方程式_______ 。
(6)某小组同学取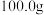 该废金属屑,经过一系列步骤,从
该废金属屑,经过一系列步骤,从 溶液中获得胆矾晶体
溶液中获得胆矾晶体 ,该废料中铜的质量分数为
,该废料中铜的质量分数为_______ 。
(一)氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。
(1)新制氯水呈浅黄绿色,且有刺激性气味,说明有
(2)新制饱和氯水经光照后,其酸性会
(3)漂白粉的有效成分是
 、
、 反应生成不稳定的次氯酸而易失效,该反应的化学方程式为
反应生成不稳定的次氯酸而易失效,该反应的化学方程式为(二)某工厂的废金属屑中主要成分为
 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,该厂用此废金属屑制取新型高效水处理剂
,该厂用此废金属屑制取新型高效水处理剂 (高铁酸钠)等产品的过程如下:
(高铁酸钠)等产品的过程如下:I.向废金属屑中加入过量的
 溶液,充分反应后过滤;
溶液,充分反应后过滤;II.向I所得固体中加入过量稀
 ,充分反应后过滤;
,充分反应后过滤;III.向II所得固体中继续加入热的稀
 ,同时不断鼓入空气,固体全部溶解得
,同时不断鼓入空气,固体全部溶解得 溶液。
溶液。(4)步骤I过滤后所得滤液的溶质成分为
(5)步骤II所得滤液经进一步处理可制得
 ,流程如下:
,流程如下:
写出由
 制取
制取 的化学方程式
的化学方程式(6)某小组同学取
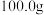 该废金属屑,经过一系列步骤,从
该废金属屑,经过一系列步骤,从 溶液中获得胆矾晶体
溶液中获得胆矾晶体 ,该废料中铜的质量分数为
,该废料中铜的质量分数为
您最近一年使用:0次
5 . 含锰化合物在化学工业中有十分重要的用途。某含锰矿石的主要成分是 ,还含CaO、
,还含CaO、 、FeS等杂质,由此矿石生产
、FeS等杂质,由此矿石生产 的工艺流程如图所示:
的工艺流程如图所示:
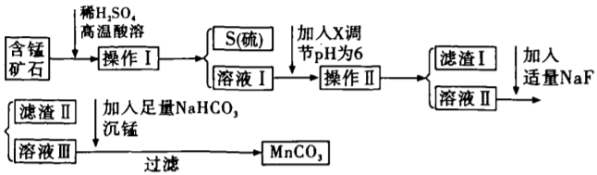
相关金属离子生成氢氧化物沉淀的pH如表所示:
回答下列问题:
(1)酸溶时,不能将稀硫酸换成浓盐酸,原因是___________ 。
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血红色,试写出酸溶过程中FeS发生反应的离子方程式:___________ 。
(3)调节溶液Ⅰ的pH时所用的物质X最好是___________ 。
(4)滤渣Ⅱ为___________ (填化学式)。
(5)沉锰的化学方程式为___________ 。
(6)沉锰后过滤得到固体 ,设计实验方案验证
,设计实验方案验证 固体是否洗涤干净:
固体是否洗涤干净:___________ 。
(7) 可用于生产
可用于生产 等盐类。通过用草酸滴定
等盐类。通过用草酸滴定 溶液的方法可测定
溶液的方法可测定 粗品的纯度(质量分数)。若量取
粗品的纯度(质量分数)。若量取 溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将
溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将___________ (填“偏大”、“偏小”或“不变”)。
 ,还含CaO、
,还含CaO、 、FeS等杂质,由此矿石生产
、FeS等杂质,由此矿石生产 的工艺流程如图所示:
的工艺流程如图所示:
相关金属离子生成氢氧化物沉淀的pH如表所示:
| 物质 | 开始沉淀 | 沉淀完全 |
 | 2.7 | 3.7 |
 | 12 | ______ |
 | 3.8 | 4.7 |
回答下列问题:
(1)酸溶时,不能将稀硫酸换成浓盐酸,原因是
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血红色,试写出酸溶过程中FeS发生反应的离子方程式:
(3)调节溶液Ⅰ的pH时所用的物质X最好是
(4)滤渣Ⅱ为
(5)沉锰的化学方程式为
(6)沉锰后过滤得到固体
 ,设计实验方案验证
,设计实验方案验证 固体是否洗涤干净:
固体是否洗涤干净:(7)
 可用于生产
可用于生产 等盐类。通过用草酸滴定
等盐类。通过用草酸滴定 溶液的方法可测定
溶液的方法可测定 粗品的纯度(质量分数)。若量取
粗品的纯度(质量分数)。若量取 溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将
溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将
您最近一年使用:0次
名校
6 . 国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g•L-1。某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中的SO2,并对其含量进行测定。
实验步骤如图1:

I.向B中加入300.00mL葡萄酒和适量稀硫酸,加热,使SO2全部逸出并与C中的H2O2完全反应,加热除去H2O2,得到待测液并稀释至500mL。
II.取25.00mL待测液于锥形瓶中,加入指示剂,用0.0100mol·L-1NaOH标准溶液进行滴定。
III.数据处理。
回答下列问题:
(1)仪器A的名称为____ 。
(2)写出C中发生的离子反应方程式_____ 。
(3)NaOH标准溶液盛装在图2____ (填“甲”或“乙”)滴定管中。若滴定终点溶液pH为8.8,则选择的指示剂为____ ;滴定过程中,眼睛应注视____ ;滴定终点的判断依据为____ 。

(4)根据下列表格中的数据计算该葡萄酒中SO2含量为___ g•L-1。
(5)下列操作会导致实验结果偏低的是____ (填字母)。
a.滴定管在装液前未用标准溶液润洗
b.滴定过程中,锥形瓶振荡得太剧烈,锥形瓶内有液滴溅出
c.达到滴定终点时,仰视读数
d.装标准溶液的滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
实验步骤如图1:

I.向B中加入300.00mL葡萄酒和适量稀硫酸,加热,使SO2全部逸出并与C中的H2O2完全反应,加热除去H2O2,得到待测液并稀释至500mL。
II.取25.00mL待测液于锥形瓶中,加入指示剂,用0.0100mol·L-1NaOH标准溶液进行滴定。
III.数据处理。
回答下列问题:
(1)仪器A的名称为
(2)写出C中发生的离子反应方程式
(3)NaOH标准溶液盛装在图2

(4)根据下列表格中的数据计算该葡萄酒中SO2含量为
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.10 | 7.60 |
| 2 | 25.00 | 7.60 | 15.00 |
| 3 | 25.00 | 0.20 | 7.80 |
a.滴定管在装液前未用标准溶液润洗
b.滴定过程中,锥形瓶振荡得太剧烈,锥形瓶内有液滴溅出
c.达到滴定终点时,仰视读数
d.装标准溶液的滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
您最近一年使用:0次
2022-05-01更新
|
23次组卷
|
2卷引用:陕西省汉中市2021-2022学年高二下学期期中考试化学试题
名校
解题方法
7 . 在肉制品加工中,常使用来硝酸钠作发色剂,但必须严格控制亚硝酸钠的用量,以确保使用安全。亚硝酸钠也是一种常见的水污染物,在工业废水中亚硝酸盐的含量较高,如不做处理排放在环境中,对人体、水生物有毒害作用。
Ⅰ.某一反应体系中反应物和生成物共六种:NaNO2 、H2O、NO 、I2、NaI、HI。已知该反应中 NaNO2只发生还原反应。
(1)该反应的还原剂__________ 。
(2)写出该反应的化学方程式_____________________________________ ,该反应中,氧化剂和氧化产物的微粒数之比为_____________ ,当有n个氧化产物生成时,转移电子数为____ e-。
(3)HI在上述反应中表现出的性质是____________________ 。
(4)误食 NaNO2 会导致血红蛋白中 Fe2+转化 Fe3+而中毒,服用维生素 C 可以解除 NaNO2
引起的中毒。下列关于上述中毒、解毒过程的说法中正确的是_________ 。
A.中毒过程NaNO2 是还原剂 B.解毒过程维生素 C 是还原剂
C.解毒过程,维生素 C 能把 Fe2+氧化 Fe3+ D.中毒时亚硝酸盐发生还原反应
Ⅱ.工业废水中亚硝酸盐的处理这一研究已有很久的历史了,传统常见的方法有离子交换法、反渗透法、电渗析法、生物及反硝化法、化学还原法和化学催化硝化法,其中化学还原法是利用加NH4Cl进行处理含亚硝酸盐的废水,转化为无污染的物质进行排放。
(5)写出该处理方法的离子方程式________________________________________ 。
Ⅰ.某一反应体系中反应物和生成物共六种:NaNO2 、H2O、NO 、I2、NaI、HI。已知该反应中 NaNO2只发生还原反应。
(1)该反应的还原剂
(2)写出该反应的化学方程式
(3)HI在上述反应中表现出的性质是
(4)误食 NaNO2 会导致血红蛋白中 Fe2+转化 Fe3+而中毒,服用维生素 C 可以解除 NaNO2
引起的中毒。下列关于上述中毒、解毒过程的说法中正确的是
A.中毒过程NaNO2 是还原剂 B.解毒过程维生素 C 是还原剂
C.解毒过程,维生素 C 能把 Fe2+氧化 Fe3+ D.中毒时亚硝酸盐发生还原反应
Ⅱ.工业废水中亚硝酸盐的处理这一研究已有很久的历史了,传统常见的方法有离子交换法、反渗透法、电渗析法、生物及反硝化法、化学还原法和化学催化硝化法,其中化学还原法是利用加NH4Cl进行处理含亚硝酸盐的废水,转化为无污染的物质进行排放。
(5)写出该处理方法的离子方程式
您最近一年使用:0次
2020-10-21更新
|
244次组卷
|
2卷引用:陕西省汉中市龙岗学校2020-2021学年高一上学期10月月考化学试题
8 . PdCl2广泛用作催化剂和一些物质的检测试剂。由Pd(NH3)2Cl2制备PdCl2工艺流程如图所示。

(1)肼(N2H4)可以被看作二元弱碱,结合质子生成N2H5+或N2H62+。肼与少量稀硫酸混合后,得到产物的化学式为___ 。
(2)对工艺流程图中的滤液处理办法最好的是:___
a.返到提钯废液中,循环使用 b.转化为无毒物质后排放 c.深埋于地下
(3)王水溶钯时,Pd被氧化为H2PdCl4。同时得到唯一还原产物亚硝酰氯(NOCl)。反应消耗的HCl与HNO3的物质的量之比为___ 。
(4)赶硝,是将残余的NO3−浓度降低到不大于0.04%。实验数据记录如表:
表一:不同HCl用量和MxOy用量(每10gPd)与NO3−残留量
处理1吨Pd,需要用到HCl和MxOy的总体积至少为___ m3(合理选择表格里相关数据计算)。
(5)煅烧过程发生分解反应,化学方程式为:___ 。
(6)浸有磷钼酸铵溶液的氯化钯试纸遇微量CO立即变成蓝色。原理较为复杂,第一步是CO还原PdCl2得到Pd单质,同时有常见的氧化物生成。 写出反应原理中第一步的化学方程式:___

(1)肼(N2H4)可以被看作二元弱碱,结合质子生成N2H5+或N2H62+。肼与少量稀硫酸混合后,得到产物的化学式为
(2)对工艺流程图中的滤液处理办法最好的是:
a.返到提钯废液中,循环使用 b.转化为无毒物质后排放 c.深埋于地下
(3)王水溶钯时,Pd被氧化为H2PdCl4。同时得到唯一还原产物亚硝酰氯(NOCl)。反应消耗的HCl与HNO3的物质的量之比为
(4)赶硝,是将残余的NO3−浓度降低到不大于0.04%。实验数据记录如表:
表一:不同HCl用量和MxOy用量(每10gPd)与NO3−残留量
| HCl用量(mL) | MxOy用量(mL) | NO3−含量(%) |
| 5 | 0、10、20、30、40 | 0.15、0.10、0.05、0.04、0.03 |
| 10 | 0、5、10、15、20 | 0.10、0.08、0.05、0.03、0.02 |
| 15 | 0、5、10、15、20 | 0.08、0.06、0.05、0.03、0.02 |
处理1吨Pd,需要用到HCl和MxOy的总体积至少为
(5)煅烧过程发生分解反应,化学方程式为:
(6)浸有磷钼酸铵溶液的氯化钯试纸遇微量CO立即变成蓝色。原理较为复杂,第一步是CO还原PdCl2得到Pd单质,同时有常见的氧化物生成。 写出反应原理中第一步的化学方程式:
您最近一年使用:0次
名校
9 . 工业上常利用反应Cr2O7n-+CH3OH+H+→Cr3++CO2↑+H2O(未配平)来测定工业甲醇中甲醇的含量,下列说法中正确的是
| A.溶液的颜色从灰绿色变为橙色 |
| B.Cr2O7n-发生氧化反应 |
| C.若配平后Cr3+和CO2的化学计量数比为2:1,则Cr2O7n-中的n=2 |
| D.若有3.2 g CH3OH参加反应,则转移的电子数为6.02×1022 |
您最近一年使用:0次
2018-10-09更新
|
1030次组卷
|
6卷引用:陕西省汉中市汉中中学2019届高三上学期第二次月考化学试题
解题方法
10 . 二氧化氯(ClO2)可用于自来水消毒。以粗盐为原料生产ClO2的工艺主要包括:①粗盐精制;②电解微酸性NaCl溶液;③ClO2的制取。工艺流程如下图:

⑴ 粗食盐水中含有Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的试剂X,X是_____ (填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO42-,其原因是_______ 。(已知:Ksp(BaSO4)=1.1×10-10;Ksp(BaCO3)=5.1×10-9)
⑵上述过程中,将食盐水在特定条件下电解得到的氯酸钠与盐酸反应生成ClO2。电解时生成的气体B是__ ;反应Ⅲ的化学方程式为________________ 。
⑶ ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。(已知:I2+2S2O32-=2I-+S4O62-)
① 准确量取10.00 mL ClO2溶液的玻璃仪器是_________________________ 。
② 滴定过程中,至少须平行测定两次的原因是________________________ 。
③ 根据上述步骤可计算出原ClO2溶液的物质的量浓度为__________ mol·L-1(用含字母的代数式表示)。

⑴ 粗食盐水中含有Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的试剂X,X是
⑵上述过程中,将食盐水在特定条件下电解得到的氯酸钠与盐酸反应生成ClO2。电解时生成的气体B是
⑶ ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。(已知:I2+2S2O32-=2I-+S4O62-)
① 准确量取10.00 mL ClO2溶液的玻璃仪器是
② 滴定过程中,至少须平行测定两次的原因是
③ 根据上述步骤可计算出原ClO2溶液的物质的量浓度为
您最近一年使用:0次
2016-12-09更新
|
1483次组卷
|
5卷引用:陕西省汉中市龙岗学校2019-2020学年高二上学期期末考试化学试题
陕西省汉中市龙岗学校2019-2020学年高二上学期期末考试化学试题(已下线)2014届江苏省扬州中学高三年级模拟考试化学试卷(已下线)2014届江苏省高三百校联合调研测试(一)化学试卷(已下线)2014届江苏启东中学第二学期期中考试高二实验班化学试卷2017届内蒙古赤峰市宁城县高三上统一考试化学试卷



