解题方法
1 . 某兴趣小组的学生根据Mg与CO2反应原理推测钠也能在CO2中燃烧,为了确定其产物并进行试验论证,某同学设计了下列装置进行试验(已知PdCl2能被CO还原为Pd),请回答下列问题:
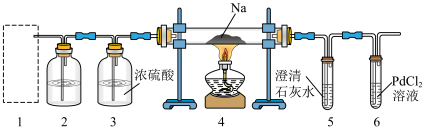

(1)上图装置2中应盛放__________ 溶液。
(2)为了使反应随开随用,随关随停,上图方框内应选用_____ 装置(填上图字母代号)。
(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行1装置的操作,待装置______ (填数字编号)中出现_______________ 现象时,再点燃酒精灯。
(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_________ 。
②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_____________ 。


(1)上图装置2中应盛放
(2)为了使反应随开随用,随关随停,上图方框内应选用
(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行1装置的操作,待装置
(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为
②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为
您最近一年使用:0次
名校
2 . 作为食品添加剂时,亚硝酸钠 可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。
可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。
Ⅰ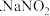 制备
制备
实验室以木炭、浓硝酸、 为主要原料按照如图所示装置制备亚硝酸钠
为主要原料按照如图所示装置制备亚硝酸钠 加热装置及部分夹持装置已略去
加热装置及部分夹持装置已略去 ,反应原理为:
,反应原理为:
回答下列问题:
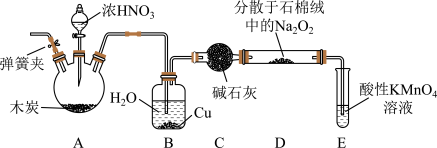
(1)连接好装置之后,下一步实验操作是______ 。
(2) 装置中铜的作用是
装置中铜的作用是______ 。
(3) 装置用于尾气处理,E中反应的离子方程式为
装置用于尾气处理,E中反应的离子方程式为______ 。
(4)实验结束阶段,熄灭酒精灯之后继续通入 直至装置冷却。此时通入
直至装置冷却。此时通入 的目的是
的目的是______ 。
Ⅱ 含量的测定
含量的测定
查阅资料可知:酸性 溶液可将
溶液可将 氧化为
氧化为 ,
, 还原成
还原成 。
。
(5)溶液配制:称取装置D中反应后的固体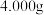 ,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的
,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的______ 中,加蒸馏水至______ 。
滴定:取 溶液于锥形瓶中,用
溶液于锥形瓶中,用 酸性
酸性 溶液进行滴定,实验数据如下表所示:
溶液进行滴定,实验数据如下表所示:
(6)第4组实验数据出现异常,造成这种异常的原因可能是______  双项选择
双项选择 。
。
A.锥形瓶洗净后未干燥 滴定终了仰视读数
滴定终了仰视读数
C.滴定终了俯视读数 酸式滴定管用蒸馏水洗净后未用标准液润洗
酸式滴定管用蒸馏水洗净后未用标准液润洗
(7)根据表中数据,计算所得固体中亚硝酸钠的质量分数______ 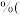 保留2位小数
保留2位小数 。
。
 可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。
可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。Ⅰ
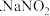 制备
制备实验室以木炭、浓硝酸、
 为主要原料按照如图所示装置制备亚硝酸钠
为主要原料按照如图所示装置制备亚硝酸钠 加热装置及部分夹持装置已略去
加热装置及部分夹持装置已略去 ,反应原理为:
,反应原理为:
回答下列问题:

(1)连接好装置之后,下一步实验操作是
(2)
 装置中铜的作用是
装置中铜的作用是(3)
 装置用于尾气处理,E中反应的离子方程式为
装置用于尾气处理,E中反应的离子方程式为(4)实验结束阶段,熄灭酒精灯之后继续通入
 直至装置冷却。此时通入
直至装置冷却。此时通入 的目的是
的目的是Ⅱ
 含量的测定
含量的测定查阅资料可知:酸性
 溶液可将
溶液可将 氧化为
氧化为 ,
, 还原成
还原成 。
。(5)溶液配制:称取装置D中反应后的固体
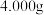 ,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的
,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的滴定:取
 溶液于锥形瓶中,用
溶液于锥形瓶中,用 酸性
酸性 溶液进行滴定,实验数据如下表所示:
溶液进行滴定,实验数据如下表所示:| 滴定次数 | 1 | 2 | 3 | 4 |
 溶液体积 溶液体积 | 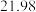 | 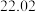 |  | 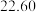 |
 双项选择
双项选择 。
。A.锥形瓶洗净后未干燥
 滴定终了仰视读数
滴定终了仰视读数C.滴定终了俯视读数
 酸式滴定管用蒸馏水洗净后未用标准液润洗
酸式滴定管用蒸馏水洗净后未用标准液润洗(7)根据表中数据,计算所得固体中亚硝酸钠的质量分数
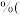 保留2位小数
保留2位小数 。
。
您最近一年使用:0次
2020-11-14更新
|
144次组卷
|
2卷引用:宁夏石嘴山市平罗中学2021-2022学年高三上学期期中考试化学试题
名校
3 . ClO2(黄绿色易溶于水的气体)是一种高效、低毒的消毒剂。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收和释放进行了研究。

(1)仪器A的名称是_______________________ 。
(2)安装F中导管时,应选用图2中的___________________ 。
(3)A中发生反应生成ClO2和Cl2,其氧化产物和还原产物物质的量之比为__________ 。
(4)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是__________________ 。
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为____ 。
(6)ClO2很不稳定,需随用随制,产物用水吸收可得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样,量取V0 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L−1 Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V1 mL。
(已知2ClO2+10I−+8H+=2Cl−+5I2+4H2O 2Na2S2O3+I2 Na2S4O6+2NaI)
Na2S4O6+2NaI)
计算该ClO2的浓度为______ g/L(用含字母的代数式表示,计算结果化简)。

(1)仪器A的名称是
(2)安装F中导管时,应选用图2中的
(3)A中发生反应生成ClO2和Cl2,其氧化产物和还原产物物质的量之比为
(4)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(6)ClO2很不稳定,需随用随制,产物用水吸收可得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样,量取V0 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L−1 Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V1 mL。
(已知2ClO2+10I−+8H+=2Cl−+5I2+4H2O 2Na2S2O3+I2
 Na2S4O6+2NaI)
Na2S4O6+2NaI)计算该ClO2的浓度为
您最近一年使用:0次
2020-03-27更新
|
388次组卷
|
6卷引用:宁夏回族自治区2020届高三下学期在线模拟化学试题
宁夏回族自治区2020届高三下学期在线模拟化学试题吉林省白城市第四中学2020届高三3月网上模拟测试化学试题江西省南昌市四校联盟2020届高三第二次联考理综化学试题福建省莆田第十五中学2019届高三上学期期中考试化学试题(已下线)专题11 富集在海水中的元素——氯 (限时精炼)-2022年高三毕业班化学常考点归纳与变式演练福建省长汀县第一中学2021-2022学年高三上学期第二次月考化学试题



