1 . 阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)制备 需要在
需要在___________ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是___________ 。
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)高铁酸钠 是一种新型的净水剂,可以通过氢氧化铁、氢氧化钠与次氯酸钠反应制得。
是一种新型的净水剂,可以通过氢氧化铁、氢氧化钠与次氯酸钠反应制得。
①请写出制取 的化学方程式
的化学方程式___________ 。
②该反应中氧化剂是___________ (用化学式表示,下同),___________ 元素被氧化,还原产物为___________ 。
(5)请将 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整:___________ 。

| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气  通过强烈的氧化作用可迅速杀灭细菌有消毒作用,同时不会产生有害物质。 通过强烈的氧化作用可迅速杀灭细菌有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用 胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放: 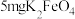 ,即可达到卫生标准 ,即可达到卫生标准 |
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)高铁酸钠
 是一种新型的净水剂,可以通过氢氧化铁、氢氧化钠与次氯酸钠反应制得。
是一种新型的净水剂,可以通过氢氧化铁、氢氧化钠与次氯酸钠反应制得。①请写出制取
 的化学方程式
的化学方程式②该反应中氧化剂是
(5)请将
 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整:
您最近一年使用:0次
2 . 水体中氨氮含量超标会造成水体富营养化,用次氯酸钙除去氨氮的原理如图所示。下列说法不正确的是


| A.①③属于复分解反应,②属于氧化还原反应 |
| B.CO2、H2O两种物质可循环使用 |
C.每生成1mol ,转移3mol电子 ,转移3mol电子 |
D.除去氨氮的总反应方程式为: |
您最近一年使用:0次
3 . 氧化铈( )是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含
)是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备氧化铈,其工艺流程如图所示;
等)为原料制备氧化铈,其工艺流程如图所示;
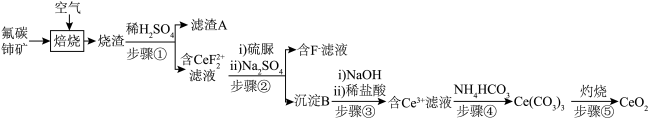
已知:①稀土离子易与 形成复盐沉淀。
形成复盐沉淀。
步骤②中 )发生的反应为:
)发生的反应为:
② 在空气中易被氧化为
在空气中易被氧化为 。
。
回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为___________ 。
(2)滤渣A的主要成分是___________ 。
(3)操作①所需的玻璃实验仪器有烧杯、___________ 。
(4)加入硫脲的目的是___________ 。
(5)步骤④中发生的离子方程式为___________ 。
(6)步骤④中生成的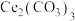 中
中 的空间构型是
的空间构型是___________ 。
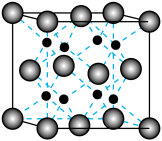
(7)氧化铈的晶体结构如图所示,其已知晶胞参数为a pm,阿伏伽德罗常数为 ,则晶胞中铈离子间最短的距离为
,则晶胞中铈离子间最短的距离为___________ ,晶体密度为___________  (写出计算式)。
(写出计算式)。
 )是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含
)是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备氧化铈,其工艺流程如图所示;
等)为原料制备氧化铈,其工艺流程如图所示;
已知:①稀土离子易与
 形成复盐沉淀。
形成复盐沉淀。步骤②中
 )发生的反应为:
)发生的反应为:
②
 在空气中易被氧化为
在空气中易被氧化为 。
。回答下列问题:
(1)
 中
中 元素的化合价为
元素的化合价为(2)滤渣A的主要成分是
(3)操作①所需的玻璃实验仪器有烧杯、
(4)加入硫脲的目的是
(5)步骤④中发生的离子方程式为
(6)步骤④中生成的
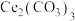 中
中 的空间构型是
的空间构型是(7)氧化铈的晶体结构如图所示,其已知晶胞参数为a pm,阿伏伽德罗常数为
 ,则晶胞中铈离子间最短的距离为
,则晶胞中铈离子间最短的距离为 (写出计算式)。
(写出计算式)。
您最近一年使用:0次
2023-07-13更新
|
231次组卷
|
2卷引用:广东省广州市番禺区2022-2023学年高二下学期期末教学质量监测化学试题
名校
解题方法
4 . 生活无处不化学,例如生活中常见消毒剂:臭氧、“84”消毒液、二氧化氯、高铁酸钠等。
(1)臭氧和氧气互为_______ (填“同位素”或“同素异形体”),它们在一定条件下可以相互转化,该变化过程属于_______ (填“氧化还原反应”或“非氧化还原反应”)。
(2)常温下,将氯气通入NaOH溶液中,可以制得“84”消毒液,写出发生反应的离子方程式:_______ 。生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是_______ 。
(3) 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得: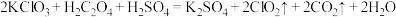 。产生1 mol
。产生1 mol  时,转移的电子的物质的量为
时,转移的电子的物质的量为_______ ;该反应中的氧化剂是_______ (填化学式)。
(4)高铁酸钠( )是一种新型的净水剂。其净水过程中发生的化学反应主要为
)是一种新型的净水剂。其净水过程中发生的化学反应主要为 (胶体)
(胶体)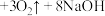 ,证明有
,证明有 胶体生成的方法为
胶体生成的方法为_______ 。
(1)臭氧和氧气互为
(2)常温下,将氯气通入NaOH溶液中,可以制得“84”消毒液,写出发生反应的离子方程式:
(3)
 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得: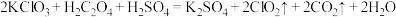 。产生1 mol
。产生1 mol  时,转移的电子的物质的量为
时,转移的电子的物质的量为(4)高铁酸钠(
 )是一种新型的净水剂。其净水过程中发生的化学反应主要为
)是一种新型的净水剂。其净水过程中发生的化学反应主要为 (胶体)
(胶体)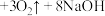 ,证明有
,证明有 胶体生成的方法为
胶体生成的方法为
您最近一年使用:0次
名校
解题方法
5 . 锌锰干电池由于其贮存和使用寿命较短,大都为一次性电池,用完之后被当作垃圾扔掉。这不仅浪费了宝贵的金属资源,而且还会产生严重的环境污染。下表是各类电池的综合成分分析结果:
通过简单的机械处理,将电池中各组分进行最大在限度的分离,从而使整个处理过程得到简化。再分别对锌皮和锰粉(MnO2)进行湿法处理,通过预处理、浸取、净化等工序制出产品。工艺流程如下图:

查阅资料知各离子沉淀完全的pH为
已知:锌元素与铝元素相似,具有两性。
(1)市售锌锰干电池为碱性电池,电解质溶液为KOH,则其正极反应为___________ ;电极总反应方程为___________ ;
(2)在预处理中,分离铁皮和锌皮的方法是___________ 。洗液加(NH4)2CO3在pH=7.5沉淀出一种碱式盐,该物质的化学式为___________ 。
(3)二氧化锰生产中,写出加入30%盐酸溶解时的离子方程式___________ ;盐酸溶解后回收的渣是___________ ;
(4)已知第二次加H2O2后调节pH≈9的目的为将Mn2+转化为MnO2,则第一次加H2O2后调节pH≈5,目的是___________ ;
(5)实验室中用高锰酸钾溶液检验Mn2+时,产生黑色沉淀,该反应的离子方程式为_______ :
(6)硫酸锰在高温条件下可以得到三种氧化物,该热分解的方程式为___________ 。
| 元素 | 锌 | 锰 | 铁 | 铜 | 碳 | 其它 |
| 质量百分含量 | 13~27 | 14~28 | 23~26 | 0.5~0.7 | 5~6 | 13 |

查阅资料知各离子沉淀完全的pH为
| 离子 | Fe3+ | Fe2+ | Cu2+ | Mn2+ |
| pH | 3.2 | 9.0 | 6.7 | 10.1 |
(1)市售锌锰干电池为碱性电池,电解质溶液为KOH,则其正极反应为
(2)在预处理中,分离铁皮和锌皮的方法是
(3)二氧化锰生产中,写出加入30%盐酸溶解时的离子方程式
(4)已知第二次加H2O2后调节pH≈9的目的为将Mn2+转化为MnO2,则第一次加H2O2后调节pH≈5,目的是
(5)实验室中用高锰酸钾溶液检验Mn2+时,产生黑色沉淀,该反应的离子方程式为
(6)硫酸锰在高温条件下可以得到三种氧化物,该热分解的方程式为
您最近一年使用:0次
名校
6 . 实验室可用NaClO3制取ClO2气体,再由ClO2制得NaClO2,实验装置如图所示:回答下列问题:
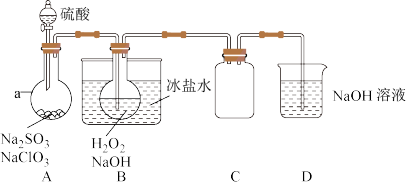
(1)仪器a的名称为___________ ;装置C的作用是___________ 。
(2)B中发生反应的化学方程式为___________ 。
(3)该实验必须使NaClO3稍微过量,目的是___________ 。
(4)证明NaClO2具有氧化性的方法是:取少量将B中溶液于试管中,先___________ ,再加入___________ (填序号,下同)酸化,最后加入___________ 检验。
①稀HNO3②稀H2SO4③K2SO3溶液④BaCl2溶液⑤FeCl2溶液⑥KSCN溶液

(1)仪器a的名称为
(2)B中发生反应的化学方程式为
(3)该实验必须使NaClO3稍微过量,目的是
(4)证明NaClO2具有氧化性的方法是:取少量将B中溶液于试管中,先
①稀HNO3②稀H2SO4③K2SO3溶液④BaCl2溶液⑤FeCl2溶液⑥KSCN溶液
您最近一年使用:0次
名校
7 . 依据图中氮元素及其化合物的转化关系,判断下列说法中不正确的是
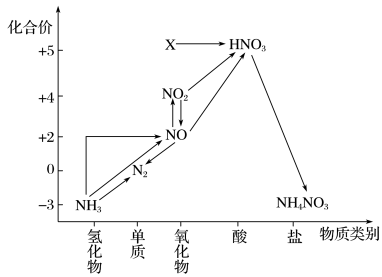

A.X是 |
| B.为提高作物的养分,可以将铵态氮肥与碱性肥料混合使用 |
C.工业上制备硝酸是利用 和 和 反应生成 反应生成 ,进一步转化为 ,进一步转化为 及 及 |
D.从原理上看, 可与 可与 反应实现 反应实现 的转化 的转化 |
您最近一年使用:0次
名校
解题方法
8 . 某体系中发生的一个反应,反应物和生成物共六种微粒:Fe3+、Mn2+、MnO 、H2O、Fe2+、H+,已知MnO
、H2O、Fe2+、H+,已知MnO 为其中一种反应物,下列说法正确的是
为其中一种反应物,下列说法正确的是
 、H2O、Fe2+、H+,已知MnO
、H2O、Fe2+、H+,已知MnO 为其中一种反应物,下列说法正确的是
为其中一种反应物,下列说法正确的是A.只有MnO 和Fe2+是反应物 和Fe2+是反应物 | B.被还原的元素是Fe |
C.发生氧化反应的物质是MnO | D.氧化剂与还原剂的个数比为1∶5 |
您最近一年使用:0次
22-23高一上·广东广州·期中
9 .  是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与还原剂接触或加热时会发生燃烧并爆炸。制取
是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与还原剂接触或加热时会发生燃烧并爆炸。制取 的装置如图所示。
的装置如图所示。

已知: 的熔点为
的熔点为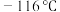 ,沸点为
,沸点为 ,
, 的沸点为
的沸点为 ;
;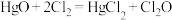 。回答下列问题。
。回答下列问题。
(1)写出①中发生的化学反应方程式_______ ;该反应中 显示出来的性质为
显示出来的性质为_______ 。
(2)装置②中盛放的试剂为_______ ;装置③的作用为_______ 。
(3)产物 在装置
在装置_______ 中收集。
(4)从装置⑤中逸出的气体主要成分为_______ 。
 是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与还原剂接触或加热时会发生燃烧并爆炸。制取
是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与还原剂接触或加热时会发生燃烧并爆炸。制取 的装置如图所示。
的装置如图所示。
已知:
 的熔点为
的熔点为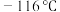 ,沸点为
,沸点为 ,
, 的沸点为
的沸点为 ;
;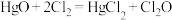 。回答下列问题。
。回答下列问题。(1)写出①中发生的化学反应方程式
 显示出来的性质为
显示出来的性质为(2)装置②中盛放的试剂为
(3)产物
 在装置
在装置(4)从装置⑤中逸出的气体主要成分为
您最近一年使用:0次
10 . 下列关于铁及其化合物之间转化反应的方程式书写正确的是
A. (g)通过灼热铁粉: (g)通过灼热铁粉: |
B.过量铁粉加入稀硝酸中: |
C.氢氧化铁中加入氢碘酸: |
D. 溶液中加入酸性 溶液中加入酸性 溶液: 溶液: |
您最近一年使用:0次
2023-04-19更新
|
1244次组卷
|
3卷引用:广东省广州市2023届高三二模考试化学试题



