名校
解题方法
1 . 下列过程中的化学反应,相应的离子方程式书写正确的是
A.KClO与Fe(OH)3在碱性条件下反应制备K2FeO4:3ClO-+2Fe(OH)3=2 +3Cl-+4H++H2O +3Cl-+4H++H2O |
| B.向含lmolFeI2溶液中通入lmolCl2:2I-+Cl2=2Cl-+I2 |
C.电解MgCl2水溶液:2Cl-+2H2O 2OH-+Cl2↑+H2↑ 2OH-+Cl2↑+H2↑ |
D.NaHSO4溶液与Ba(OH)2溶液反应至溶液呈中性: +H++OH-+Ba2+=BaSO4↓+H2O +H++OH-+Ba2+=BaSO4↓+H2O |
您最近一年使用:0次
名校
解题方法
2 . 某铜矿石的主要成分为 ,还含有少量
,还含有少量 、
、 、
、 。工业上用该矿石获取铜和胆矾的操作流程如下:
。工业上用该矿石获取铜和胆矾的操作流程如下:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)实际生产中,将矿石粉碎为矿渣的目的是_______ 。
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为_______ 。
(3)反应I完成后的滤液中铁元素的存在形式为________ (填离子符号),检验该离子常用的试剂为_______ ,生成该离子的离子方程式为________ 。
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为_______ ,该反应中氧化剂与还原剂物质的量之比为________ 。
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围________ 。
(6)操作1主要包括:______ 、过滤、冷水洗涤得到 。
。
 ,还含有少量
,还含有少量 、
、 、
、 。工业上用该矿石获取铜和胆矾的操作流程如下:
。工业上用该矿石获取铜和胆矾的操作流程如下: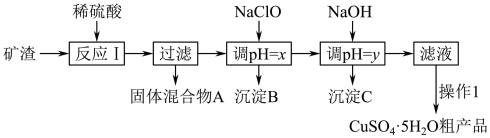

②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |  |  |  |  |
| 开始沉淀的pH | 5.4 | 4.0 | 2.7 | 5.8 |
| 沉淀完全的pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)实际生产中,将矿石粉碎为矿渣的目的是
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为
(3)反应I完成后的滤液中铁元素的存在形式为
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围
(6)操作1主要包括:
 。
。
您最近一年使用:0次
名校
3 . 图中展示的是乙烯催化氧化的过程(部分相关离子未画出),下列描述正确的是
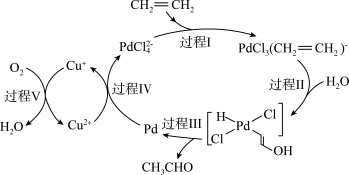
A.乙烯催化氧化反应的化学方程式为 |
B.反应中只有 作催化剂 作催化剂 |
| C.该转化过程中,没有极性键的断裂与形成 |
D.该转化过程中,涉及反应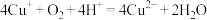 |
您最近一年使用:0次
2024-04-10更新
|
287次组卷
|
2卷引用:广东省深圳市福田区福田中学2023-2024学年高三下学期开学考试化学试题
解题方法
4 . Ⅰ.铁及其化合物在生产生活中有极其重要的用途。 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:
(1)由上述实验能否得出“维生素C可将 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:______ 。
Ⅱ.高铁酸钾( )是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于水而形成暗紫色溶液,静置后会分解并释放出大量氧气,同时生成KOH和
)是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于水而形成暗紫色溶液,静置后会分解并释放出大量氧气,同时生成KOH和 胶体。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法等。
胶体。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法等。
(2)熔融法:在苛性碱存在的环境中,铁盐被过氧化钠高温氧化成高铁酸钠: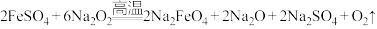 ,再加入适量饱和KOH溶液反应得到
,再加入适量饱和KOH溶液反应得到 。上述反应在熔融状态下进行,而不在水溶液中进行的原因是
。上述反应在熔融状态下进行,而不在水溶液中进行的原因是______ 。
(3)高铁酸钾可通过次氯酸钾氧化 溶液来制备。次氯酸钾的制备装置如图所示。
溶液来制备。次氯酸钾的制备装置如图所示。
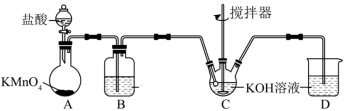
回答下列问题:
①装置A中 与盐酸反应生成
与盐酸反应生成 和
和 ,其化学方程式为
,其化学方程式为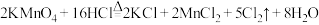 。
。
a.请用双线桥法标出电子转移方向与数目_______ 。
b.上述反应中的HCl体现了什么性质?_______ 。
②将制备的 通过装置B可除去杂质HCl,B中的溶液为
通过装置B可除去杂质HCl,B中的溶液为_____ 。
③ 和KOH溶液在较高温度下反应生成
和KOH溶液在较高温度下反应生成 。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是
。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是______ 。
④若实验制得的次氯酸钾溶液中 (N代表微粒个数),则
(N代表微粒个数),则
_______ 。
⑤装置D的作用是_______ 。
⑥次氯酸盐氧化法是在碱性条件下,KClO饱和溶液可将 转化为
转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:________ 。
 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:| 实验方案 | 实验现象 |
取适量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 | 紫色褪去 |
(1)由上述实验能否得出“维生素C可将
 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:Ⅱ.高铁酸钾(
 )是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于水而形成暗紫色溶液,静置后会分解并释放出大量氧气,同时生成KOH和
)是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于水而形成暗紫色溶液,静置后会分解并释放出大量氧气,同时生成KOH和 胶体。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法等。
胶体。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法等。(2)熔融法:在苛性碱存在的环境中,铁盐被过氧化钠高温氧化成高铁酸钠:
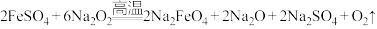 ,再加入适量饱和KOH溶液反应得到
,再加入适量饱和KOH溶液反应得到 。上述反应在熔融状态下进行,而不在水溶液中进行的原因是
。上述反应在熔融状态下进行,而不在水溶液中进行的原因是(3)高铁酸钾可通过次氯酸钾氧化
 溶液来制备。次氯酸钾的制备装置如图所示。
溶液来制备。次氯酸钾的制备装置如图所示。
回答下列问题:
①装置A中
 与盐酸反应生成
与盐酸反应生成 和
和 ,其化学方程式为
,其化学方程式为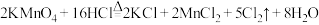 。
。a.请用双线桥法标出电子转移方向与数目
b.上述反应中的HCl体现了什么性质?
②将制备的
 通过装置B可除去杂质HCl,B中的溶液为
通过装置B可除去杂质HCl,B中的溶液为③
 和KOH溶液在较高温度下反应生成
和KOH溶液在较高温度下反应生成 。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是
。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是④若实验制得的次氯酸钾溶液中
 (N代表微粒个数),则
(N代表微粒个数),则
⑤装置D的作用是
⑥次氯酸盐氧化法是在碱性条件下,KClO饱和溶液可将
 转化为
转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:
您最近一年使用:0次
名校
解题方法
5 . 请默写下列方程式。
(1)写出NH3与氧气发生催化氧化反应的化学方程式:_______ 。
(2)浓硝酸见光分解的化学方程式:_______ 。
(3)浓硝酸和铜反应的化学方程式:_______ 。
(4)硫化氢和二氧化硫气体混合的化学方程式:_______ 。
(5)二氧化氮通入水中反应的离子方程式:_______ 。
(1)写出NH3与氧气发生催化氧化反应的化学方程式:
(2)浓硝酸见光分解的化学方程式:
(3)浓硝酸和铜反应的化学方程式:
(4)硫化氢和二氧化硫气体混合的化学方程式:
(5)二氧化氮通入水中反应的离子方程式:
您最近一年使用:0次
6 . 活化二氧化锰在能源化学上有着重要作用,工业上利用精制软锰矿粉(MnO2)通过下列流程制备:
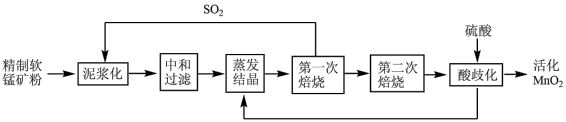
已知:蒸发结晶得到MnSO4。
(1)将软锰矿粉泥浆化的目的是________ ;反应方程式为_____________ ;
(2)“第一次焙烧”温度是1000℃,生成Mn3O4、SO2和O2,“第二次焙烧”温度为700℃,产物为Mn2O3;700℃时焙烧的氧化剂与还原剂物质的量比为_____________ 。
(3)“酸歧化”的离子方程式为________________ 。
(4)活化MnO2中不能含有铜、铅等重金属元素,在“中和过滤”前需要加入某种盐溶液除去重金属离子,该盐的化学式是___________ 。(已知CuS、PbS、PbSO4均为难溶物)
(5)“第一次焙烧”每产生3molSO2,若完全转化为硫酸,理论上需要再充入空气_____ L。(标准状况下)

已知:蒸发结晶得到MnSO4。
(1)将软锰矿粉泥浆化的目的是
(2)“第一次焙烧”温度是1000℃,生成Mn3O4、SO2和O2,“第二次焙烧”温度为700℃,产物为Mn2O3;700℃时焙烧的氧化剂与还原剂物质的量比为
(3)“酸歧化”的离子方程式为
(4)活化MnO2中不能含有铜、铅等重金属元素,在“中和过滤”前需要加入某种盐溶液除去重金属离子,该盐的化学式是
(5)“第一次焙烧”每产生3molSO2,若完全转化为硫酸,理论上需要再充入空气
您最近一年使用:0次
名校
解题方法
7 .  是一种重要的杀菌消毒剂,可通过上述制取的精制食盐水通过以下流程制备:
是一种重要的杀菌消毒剂,可通过上述制取的精制食盐水通过以下流程制备:
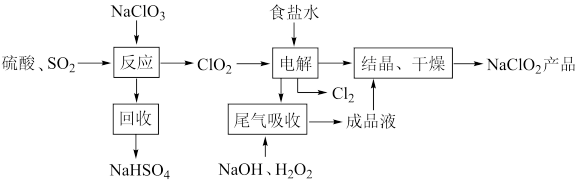
(1) 中
中 的化合价为
的化合价为_______ 。
(2)写出“反应步骤中生成 的化学方程式
的化学方程式_______ 。
(3)“尾气吸收”是吸收“电解”过程排出的少量 ,发生如下反应:
,发生如下反应: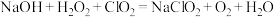
①配平化学方程式,并用单线桥表示电子转移方向和数目_______ 。
②此吸收反应中,氧化产物是_______ ,氧化剂与还原剂的个数比为_______ 。
③比较氧化性:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为_______  。(计算结果保留两位小数)
。(计算结果保留两位小数)
 是一种重要的杀菌消毒剂,可通过上述制取的精制食盐水通过以下流程制备:
是一种重要的杀菌消毒剂,可通过上述制取的精制食盐水通过以下流程制备:
(1)
 中
中 的化合价为
的化合价为(2)写出“反应步骤中生成
 的化学方程式
的化学方程式(3)“尾气吸收”是吸收“电解”过程排出的少量
 ,发生如下反应:
,发生如下反应: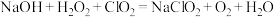
①配平化学方程式,并用单线桥表示电子转移方向和数目
②此吸收反应中,氧化产物是
③比较氧化性:

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为 。(计算结果保留两位小数)
。(计算结果保留两位小数)
您最近一年使用:0次
名校
解题方法
8 .  是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
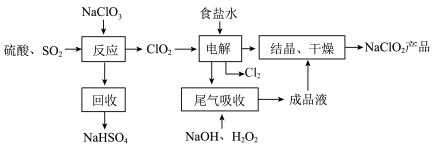
回答下列问题:
(1) 中
中 的化合价为
的化合价为___________ 。
(2)写出“反应”步骤中生成 的化学方程式
的化学方程式___________ 。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 ,要加入的试剂为
,要加入的试剂为___________ ,“电解”中还原产物是___________ 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 。此吸收反应中氧化剂与还原剂的物质的量之比为
。此吸收反应中氧化剂与还原剂的物质的量之比为___________ 。
 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1)
 中
中 的化合价为
的化合价为(2)写出“反应”步骤中生成
 的化学方程式
的化学方程式(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
 ,要加入的试剂为
,要加入的试剂为(4)“尾气吸收”是吸收“电解”过程排出的少量
 。此吸收反应中氧化剂与还原剂的物质的量之比为
。此吸收反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解题方法
9 . 化学技术在铁材料研发改进方面发挥着重要作用。
I.纳米 是一种多功能磁性材料,在高科技领域有特殊的用途,工业上可通过如下过程制得:
是一种多功能磁性材料,在高科技领域有特殊的用途,工业上可通过如下过程制得:
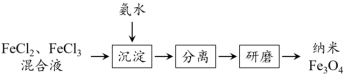
(1)在实验室中,同学们做了如下实验:
①将红热铁丝伸到盛有氯气的集气瓶中制 ,反应的化学方程式为
,反应的化学方程式为___________ 。
②将 通入
通入 溶液制
溶液制 ,观察到的实验现象为
,观察到的实验现象为___________ 。
③将 溶液滴入
溶液滴入 溶液中,观察到产生白色絮状沉淀迅速变为灰绿色,最后转成红褐色。白色和红褐色沉淀的成分分别是
溶液中,观察到产生白色絮状沉淀迅速变为灰绿色,最后转成红褐色。白色和红褐色沉淀的成分分别是___________ 、___________ (填化学式)。
(2)流程中,产生“沉淀”的离子方程式为:___________
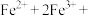 ___________
___________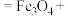 ___________
___________ ___________
___________
(3)同学们认为 和
和 的混合溶液中
的混合溶液中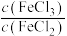 应略小于2,原因是
应略小于2,原因是___________ 。
Ⅱ.某同学查阅资料得知还可以用纳米铁粉与水蒸气反应制得纳米 。
。
(4)纳米铁粉___________ (填“属于”或“不属于”)胶体。
(5)该同学设计了以下方案证明产物为 。
。
①完善表格:ii___________ ;iii___________ 。
②有同学认为该方案不能证明产物为 ,其理由是
,其理由是___________ 。
I.纳米
 是一种多功能磁性材料,在高科技领域有特殊的用途,工业上可通过如下过程制得:
是一种多功能磁性材料,在高科技领域有特殊的用途,工业上可通过如下过程制得:
(1)在实验室中,同学们做了如下实验:
①将红热铁丝伸到盛有氯气的集气瓶中制
 ,反应的化学方程式为
,反应的化学方程式为②将
 通入
通入 溶液制
溶液制 ,观察到的实验现象为
,观察到的实验现象为③将
 溶液滴入
溶液滴入 溶液中,观察到产生白色絮状沉淀迅速变为灰绿色,最后转成红褐色。白色和红褐色沉淀的成分分别是
溶液中,观察到产生白色絮状沉淀迅速变为灰绿色,最后转成红褐色。白色和红褐色沉淀的成分分别是(2)流程中,产生“沉淀”的离子方程式为:
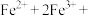 ___________
___________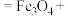 ___________
___________ ___________
___________
(3)同学们认为
 和
和 的混合溶液中
的混合溶液中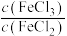 应略小于2,原因是
应略小于2,原因是Ⅱ.某同学查阅资料得知还可以用纳米铁粉与水蒸气反应制得纳米
 。
。(4)纳米铁粉
(5)该同学设计了以下方案证明产物为
 。
。| 编号 | 实验方案 | 实验现象 | 实验结论 | |
| ⅰ | 取反应后的固体,加稀硫酸充分振荡溶解 | / | / | |
| ⅱ | 向 溶液中滴加 溶液中滴加 所得溶液 所得溶液 | ___________ | 溶液中含 | 产物为 |
| ⅲ | 取i所得溶液,滴加___________溶液 | 溶液变血红色 | 溶液中含 | |
②有同学认为该方案不能证明产物为
 ,其理由是
,其理由是
您最近一年使用:0次
名校
10 . 通过 CO2 捕获和转化技术可实现 CO2 资源化利用,其物质转化关系如图所示。
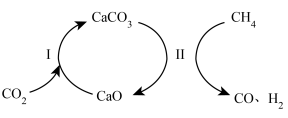
| A.过程Ⅰ属于氧化还原反应 |
| B.过程Ⅱ中的反应为CaCO3+CH4=CaO+2CO+2H2 |
| C.捕获和转化 CO2的过程中,CaO 可以循环利用 |
| D.CO2的捕获和转化有助于减弱温室效应 |
您最近一年使用:0次
2023-12-11更新
|
163次组卷
|
6卷引用:广东省 深圳实验学校高中部2023-2024学年高一上学期化学培优考试 2



