1 . 钯(Pd)是一种不活泼金属,性质与铂相似。含钯催化剂不仅在科研和工业生产中用途广泛,而且用量大,因此从废催化剂中回收钯具有巨大的经济效益。已知某废催化剂的主要成分是钯和活性炭,还含有少量铁、镁、铝、硅、铜等杂质元素,提取海绵钯的工艺流程如下:
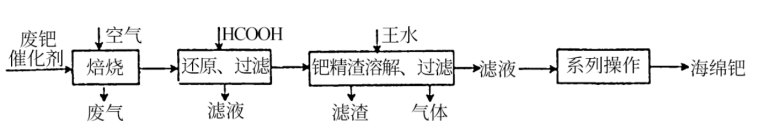
(1)Pd的价电子排布式为4d10,指出它在元素周期表中的位置_______ 。
(2)“焙烧”步骤中,通入的空气一定要足量,理由是_______ 。
(3)写出甲酸还原过程发生反应的化学方程式_______ 。
(4)钯在王水中溶解生成化合物X(由3种元素组成)、种无色有毒的气体Y和水。
①如何配置王水_______ 。
②写出钯与王水反应的化学方程式_______ 。
(5)金属钯具有显著的吸氢性能,其密度为12.0g·cm-3。
①在标准状况下,海绵钯吸收氢气的体积约为其体积的840倍,求海绵钯的吸附容量R=_______ (mL·g-1)、氢气的浓度r=_______ (1molPd吸收氢气的物质的量)。
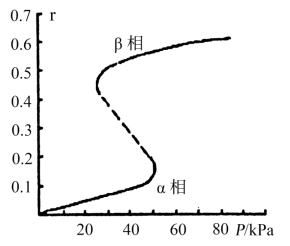
②金属钯中,氢气的r与压强之间的变化关系如图所示,试解释该图的变化趋势_______ 。
(相对原子质量:Pd106.4,理想气体常数R=8.314J·mol-l·K-1)

(1)Pd的价电子排布式为4d10,指出它在元素周期表中的位置
(2)“焙烧”步骤中,通入的空气一定要足量,理由是
(3)写出甲酸还原过程发生反应的化学方程式
(4)钯在王水中溶解生成化合物X(由3种元素组成)、种无色有毒的气体Y和水。
①如何配置王水
②写出钯与王水反应的化学方程式
(5)金属钯具有显著的吸氢性能,其密度为12.0g·cm-3。
①在标准状况下,海绵钯吸收氢气的体积约为其体积的840倍,求海绵钯的吸附容量R=
②金属钯中,氢气的r与压强之间的变化关系如图所示,试解释该图的变化趋势

(相对原子质量:Pd106.4,理想气体常数R=8.314J·mol-l·K-1)
您最近一年使用:0次
名校
解题方法
2 . 金属铁与一定浓度HNO3反应的离子方程式可表示为:aFe+ bNO + cH+ = dFe3++fFe2+ + gNO2↑+ hNO↑+ kH2O。下列关系一定成立的是
+ cH+ = dFe3++fFe2+ + gNO2↑+ hNO↑+ kH2O。下列关系一定成立的是
 + cH+ = dFe3++fFe2+ + gNO2↑+ hNO↑+ kH2O。下列关系一定成立的是
+ cH+ = dFe3++fFe2+ + gNO2↑+ hNO↑+ kH2O。下列关系一定成立的是| A.c+3d+2f= b | B.2b=g+k |
| C.2b=g-k | D.若a=b,则f=g |
您最近一年使用:0次
2021-08-01更新
|
167次组卷
|
2卷引用:2018年广东和广西高中学生化学竞赛试题
3 . 烟花爆竹常常在重大节日庆典中燃放。烟花的主要成分可以分成氧化剂、还原剂、发色剂、黏合剂等。
(1)爆竹的主要成分是黑火药,含有硝酸钾、硫黄和木炭。生成物中有一种单质,该单质分子的电子式是___________ 。
(2)用高氯酸钾代替硝酸钾,用糖类代替木炭和硫黄,可避免硫化钾、二氧化硫等有害物质的排放。请写出高氯酸钾(KClO4)与葡萄糖(C6H12O6)反应的化学方程式:___________ 。
(3)烟花中的发光剂,可用短周期金属的粉末,其燃烧时会发出白炽的强光。写出该金属的化学符号___________ 。
(4)烟花中还含有发色剂,利用焰色反应可使烟花放出五彩缤纷的色彩。焰色反应的原理是___________ 。
(1)爆竹的主要成分是黑火药,含有硝酸钾、硫黄和木炭。生成物中有一种单质,该单质分子的电子式是
(2)用高氯酸钾代替硝酸钾,用糖类代替木炭和硫黄,可避免硫化钾、二氧化硫等有害物质的排放。请写出高氯酸钾(KClO4)与葡萄糖(C6H12O6)反应的化学方程式:
(3)烟花中的发光剂,可用短周期金属的粉末,其燃烧时会发出白炽的强光。写出该金属的化学符号
(4)烟花中还含有发色剂,利用焰色反应可使烟花放出五彩缤纷的色彩。焰色反应的原理是
您最近一年使用:0次
4 . 土壤中的硫循环如图所示,回答下列问题。
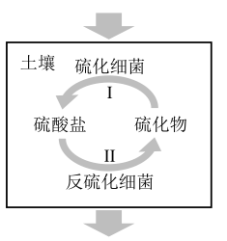
(1)土壤中的硫酸盐部分来自于降水,写出SO2转化为酸雨的化学方程式:___________ 。
(2) I中,土壤中的黄铁矿(FeS2)会转化成硫酸亚铁和硫酸,写出化学方程式:___________ 。
(3)某种反硫化细菌在过程II中要消耗乳酸,乳酸的作用是___________ 。
(4)某些硫酸盐溶液向地下深层渗透,遇到难溶硫化物时,缓慢转变为更难溶的硫化物。用离子方程式表示CuSO4遇ZnS的变化:___________ 。

(1)土壤中的硫酸盐部分来自于降水,写出SO2转化为酸雨的化学方程式:
(2) I中,土壤中的黄铁矿(FeS2)会转化成硫酸亚铁和硫酸,写出化学方程式:
(3)某种反硫化细菌在过程II中要消耗乳酸,乳酸的作用是
(4)某些硫酸盐溶液向地下深层渗透,遇到难溶硫化物时,缓慢转变为更难溶的硫化物。用离子方程式表示CuSO4遇ZnS的变化:
您最近一年使用:0次
5 . 根据条件书写化学反应方程式。
(1)工业上从碳酸氢铵和镁硼石[Mg2B2O4(OH)2]在水溶液中反应制备硼酸______ 。
(2)从乏燃料提取钚元素的过程中,利用亚硝酸钠在强酸溶液中将 Pu3+氧化为 Pu4+_____ 。
(3)NaBH4 与氯化镍(摩尔比 2:1)在水溶液中反应,可得到两种硼化物:硼化镍和硼酸(摩尔比 1:3)_____ 。
(4)通过 KMnO4和H2O2在KF-HF质中反应获得化学法制 F2 的原料 K2MnF6_____
(5)磷化氢与甲醛的硫酸溶液反应,产物仅为硫酸鏻(盐)_____ 。
(1)工业上从碳酸氢铵和镁硼石[Mg2B2O4(OH)2]在水溶液中反应制备硼酸
(2)从乏燃料提取钚元素的过程中,利用亚硝酸钠在强酸溶液中将 Pu3+氧化为 Pu4+
(3)NaBH4 与氯化镍(摩尔比 2:1)在水溶液中反应,可得到两种硼化物:硼化镍和硼酸(摩尔比 1:3)
(4)通过 KMnO4和H2O2在KF-HF质中反应获得化学法制 F2 的原料 K2MnF6
(5)磷化氢与甲醛的硫酸溶液反应,产物仅为硫酸鏻(盐)
您最近一年使用:0次
6 . 最近,我国某高校一研究小组将0.383gAgCl,0.160gSe和0.21gNaOH装入充满蒸馏水的反应釜中加热到115°C,10小时后冷至室温,用水洗净可溶物后,得到难溶于水的金属色晶体A.在显微镜下观察,发现A的单晶竟是六角微型管(如下图所示),有望开发为特殊材料。现代物理方法证实A由银和硒两种元素组成,Se的质量几近原料的2/3;A的理论产量约0.39g。
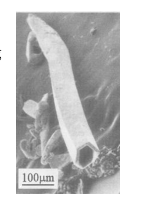
(1)写出合成A的化学方程式_______ ,标明A是什么_________ 。
(2)溶于水的物质有:_______ 。

(1)写出合成A的化学方程式
(2)溶于水的物质有:
您最近一年使用:0次
7 . 烟道气中的NOx是主要的大气污染物之一,为了监测某工厂烟道气中NOx含量,采集标准状况下50.00mL烟道气经除尘、干燥后缓慢通入适量酸化的H2O2的溶液中,使NOx完全被氧化为NO ,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO
,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO 的还原产物全为NO,且NO全部从溶液中逸出)
的还原产物全为NO,且NO全部从溶液中逸出)
(1)写出NO被H2O2氧化为NO 的离子方程式
的离子方程式_______
(2)与量取的20.00mL溶液中NO 反应的Fe2+为
反应的Fe2+为_______ mol?若FeSO4标准溶液部分变质,会使NOx含量测定结果如何_______ (答偏高、偏低或者无影响)
(3)标准状况下该工程烟道气中NOx(折合为NO2)的含量为每立方米_______ 毫克?
 ,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO
,除去多余的H2O2并加水稀释至100.00mL。量取20.00mL该溶液,加入30.00mL0.01000mol/LFeSO4标准溶液(过量),充分反应后,用0.001000mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液10.00mL。(假设NO 的还原产物全为NO,且NO全部从溶液中逸出)
的还原产物全为NO,且NO全部从溶液中逸出)(1)写出NO被H2O2氧化为NO
 的离子方程式
的离子方程式(2)与量取的20.00mL溶液中NO
 反应的Fe2+为
反应的Fe2+为(3)标准状况下该工程烟道气中NOx(折合为NO2)的含量为每立方米
您最近一年使用:0次
8 . 四氧化三锰主要用于电子工业,是生产软磁铁氧体的原料之一。
(1)四氧化三锰的制法有焙烧法和还原法两类。在还原法中,先将水锰矿(主要成分MnOOH)焙烧成三氧化二锰,再于250~500℃用甲烷还原生成四氧化三锰。请写出上述二步反应的化学方程式_______ 。
(2)通常所说的四氧化三锰中,锰的价态实际上既有二价,也有三价和四价。在某研究工作中,要求得知四氧化三锰中不同价态锰的比值,采用的测定方法步骤如下:
i.称取3份质量相同的试样。第一份以硫酸铵-硫酸溶液选择性溶解试样中的二价锰,过滤洗涤后,滤液用氨水中和并。用氨一氯化铵缓冲溶液调至pH10,加入必要的试剂和指示剂,用EDTA标准溶液(a1mol·L-1)滴定至终点,耗去b1mL。
ii.第二份试样中,准确加入过量的草酸钠标准溶液(a2mol·L-1,b2mL)和适量硫酸,加热使试样全部溶解,立即用高锰酸钾标准溶液(a3mol·L-1)滴定剩余的还原剂至终点,耗去b3mL。
iii.第三份试样中,同样加入过量的草酸钠标准溶液和适量硫酸,加热使全部溶解。冷却后用氨水中和并用氨-氯化铵缓冲溶液调至pH10,加入必要的试剂和指示剂,用EDTA标准溶液滴定至终点,耗去b4mL。
①写出步骤ii溶解试样时,不同价态锰的氧化物同草酸之间反应的化学方程式_______ ;写出用高锰酸钾滴定剩余还原剂的化学方程式_______ 。
②用a1、a2、a3、b1、b2、b3和b4写出试样中二价、三价和四价锰含量(分别用X、Y、Z表示)的计算式_______ ,单位用mmol表示。
(1)四氧化三锰的制法有焙烧法和还原法两类。在还原法中,先将水锰矿(主要成分MnOOH)焙烧成三氧化二锰,再于250~500℃用甲烷还原生成四氧化三锰。请写出上述二步反应的化学方程式
(2)通常所说的四氧化三锰中,锰的价态实际上既有二价,也有三价和四价。在某研究工作中,要求得知四氧化三锰中不同价态锰的比值,采用的测定方法步骤如下:
i.称取3份质量相同的试样。第一份以硫酸铵-硫酸溶液选择性溶解试样中的二价锰,过滤洗涤后,滤液用氨水中和并。用氨一氯化铵缓冲溶液调至pH10,加入必要的试剂和指示剂,用EDTA标准溶液(a1mol·L-1)滴定至终点,耗去b1mL。
ii.第二份试样中,准确加入过量的草酸钠标准溶液(a2mol·L-1,b2mL)和适量硫酸,加热使试样全部溶解,立即用高锰酸钾标准溶液(a3mol·L-1)滴定剩余的还原剂至终点,耗去b3mL。
iii.第三份试样中,同样加入过量的草酸钠标准溶液和适量硫酸,加热使全部溶解。冷却后用氨水中和并用氨-氯化铵缓冲溶液调至pH10,加入必要的试剂和指示剂,用EDTA标准溶液滴定至终点,耗去b4mL。
①写出步骤ii溶解试样时,不同价态锰的氧化物同草酸之间反应的化学方程式
②用a1、a2、a3、b1、b2、b3和b4写出试样中二价、三价和四价锰含量(分别用X、Y、Z表示)的计算式
您最近一年使用:0次
解题方法
9 . 钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,有“光明使者”的美誉。钨在自然界主要以钨(VI)酸盐的形式存在。有开采价值的钨矿石是白钨矿和黑钨矿。白钨矿的主要成分是钨酸钙(CaWO4);黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成(Fe,Mn)WO4。黑钨矿传统冶炼工艺的第一阶段是碱熔法:
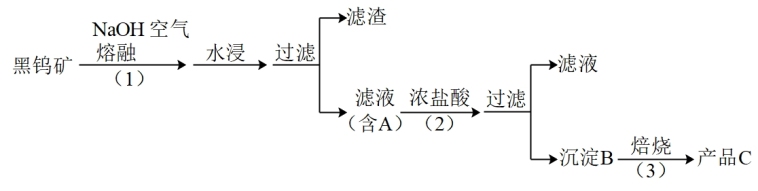
其中A、B、C都是钨的化合物。
(1)写出上述流程中A、B、C的化学式:A_______ 、B_______ 、C_______ ,以及步骤(1)、(2)、(3)中发生反应的化学方程式(1)_______ 、(2)_______ 、(3)_______ 。
(2)钨冶炼工艺的第二阶段则是用碳、氢等还原剂把氧化钨还原为金属钨。对钨的纯度要求不高时,可用碳作还原剂。
①写出用碳还原氧化钨制取金属钨的化学方程式_______ 。
②用下表所给的298.15K的数据计算上述反应的标准自由能变化。推出该反应在什么温度条件下能自发进行_______ 。(假设表中数据不随温度变化)
(3)为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而必须用氢气作还原剂,为什么_______ ?写出用氢气还原氧化钨的化学方程式_______ 。
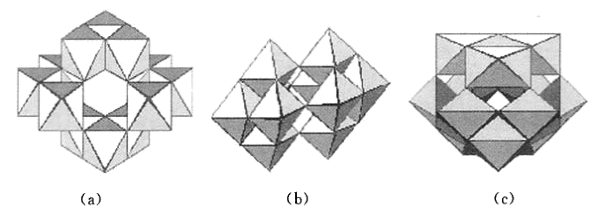
(4)在酸化钨酸盐的过程中,钨酸根WO 可能在不同程度上缩合形成多钨酸根。多钨酸根的组成常因溶液的酸度不同而不同,它们的结构都由含1个中心W原子和6个配位0原子的钨氧八面体WO6通过共顶或共边的方式形成。在为数众多的多钨酸根中,性质和结构了解得比较清楚的是仲钨酸根[H2W12O42]10-和偏钨酸根[H2Wl2O40]6-。在下面3张结构图中,哪一张是仲钨酸根的结构?简述判断理由
可能在不同程度上缩合形成多钨酸根。多钨酸根的组成常因溶液的酸度不同而不同,它们的结构都由含1个中心W原子和6个配位0原子的钨氧八面体WO6通过共顶或共边的方式形成。在为数众多的多钨酸根中,性质和结构了解得比较清楚的是仲钨酸根[H2W12O42]10-和偏钨酸根[H2Wl2O40]6-。在下面3张结构图中,哪一张是仲钨酸根的结构?简述判断理由_______ 。
(5)仲钨酸的肼盐在热分解时会发生内在氧化还原反应,我国钨化学研究的奠基人顾翼东先生采用这一反应制得了蓝色的非整比的钨氧化物WO3-x。这种蓝色氧化钨具有比表面大、易还原的优点,在制钨粉时温度容易控制,目前冶炼拉制钨丝的金属钨都用蓝色氧化钨为原料。经分析,得知蓝色氧化钨中钨的质量分数为0.7985。
①计算WO3-x中的x值_______ 。
②一般认为,蓝色氧化钨的颜色和非整比暗示了在化合物中存在五价和六价2种价态的钨。试计算蓝色氧化钨中这2种价态的钨原子数比_______ 。(相对原子质量:W-183.84;O-16.00)

其中A、B、C都是钨的化合物。
(1)写出上述流程中A、B、C的化学式:A
(2)钨冶炼工艺的第二阶段则是用碳、氢等还原剂把氧化钨还原为金属钨。对钨的纯度要求不高时,可用碳作还原剂。
①写出用碳还原氧化钨制取金属钨的化学方程式
②用下表所给的298.15K的数据计算上述反应的标准自由能变化。推出该反应在什么温度条件下能自发进行
| 物质 |  (kJ·mol-1) (kJ·mol-1) |  (J·mol-1·K-1) (J·mol-1·K-1) |
| W(s) WO3(s) C(石墨) CO(g) CO2(g) H2(g) H2O(g) H2O(l) | 0 -842.87 0 -110.52 -393.51 0 -241.82 -285.31 | 32.64 75.90 5.74 197.56 213.64 130.57 188.72 69.90 |
(4)在酸化钨酸盐的过程中,钨酸根WO
 可能在不同程度上缩合形成多钨酸根。多钨酸根的组成常因溶液的酸度不同而不同,它们的结构都由含1个中心W原子和6个配位0原子的钨氧八面体WO6通过共顶或共边的方式形成。在为数众多的多钨酸根中,性质和结构了解得比较清楚的是仲钨酸根[H2W12O42]10-和偏钨酸根[H2Wl2O40]6-。在下面3张结构图中,哪一张是仲钨酸根的结构?简述判断理由
可能在不同程度上缩合形成多钨酸根。多钨酸根的组成常因溶液的酸度不同而不同,它们的结构都由含1个中心W原子和6个配位0原子的钨氧八面体WO6通过共顶或共边的方式形成。在为数众多的多钨酸根中,性质和结构了解得比较清楚的是仲钨酸根[H2W12O42]10-和偏钨酸根[H2Wl2O40]6-。在下面3张结构图中,哪一张是仲钨酸根的结构?简述判断理由
(5)仲钨酸的肼盐在热分解时会发生内在氧化还原反应,我国钨化学研究的奠基人顾翼东先生采用这一反应制得了蓝色的非整比的钨氧化物WO3-x。这种蓝色氧化钨具有比表面大、易还原的优点,在制钨粉时温度容易控制,目前冶炼拉制钨丝的金属钨都用蓝色氧化钨为原料。经分析,得知蓝色氧化钨中钨的质量分数为0.7985。
①计算WO3-x中的x值
②一般认为,蓝色氧化钨的颜色和非整比暗示了在化合物中存在五价和六价2种价态的钨。试计算蓝色氧化钨中这2种价态的钨原子数比
您最近一年使用:0次
解题方法
10 . 化合物X是产量大、应用广的二元化合物,大量用作漂白剂、饮水处理剂、消毒剂等。年产量达300万吨的氯酸钠是生产X的原料,92%用于生产X-在酸性水溶液中用盐酸、二氧化硫或草酸还原。此外,将亚氯酸钠固体装柱,通入用空气稀释的氯气氧化,也可生产X。X有极性和顺磁性,不形成二聚体,在碱性溶液里可发生歧化反应。
(1)写出X的分子式__________ 和共轭π键( 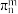 )
)___________
(2)分别写出上述用草酸还原和用氯气氧化生产X的反应方程式___________
(3)写出上述X歧化反应的化学方程式___________
(1)写出X的分子式
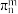 )
)(2)分别写出上述用草酸还原和用氯气氧化生产X的反应方程式
(3)写出上述X歧化反应的化学方程式
您最近一年使用:0次



