解题方法
1 . 白色固体A,熔点182℃,摩尔质量76.12g∙mol-1,可代替氰化物用于提炼金的新工艺。A的合成方法有:
i.142°C下加热硫氰酸铵;
ii.CS2与氨反应;
iii.CaCN2和(NH4)2S水溶液反应(放出氨气)。
常温下,A在水溶液中可发生异构化反应,部分转化成B.酸性溶液中,A在氧化剂(如Fe3+、H2O2和O2)存在下能溶解金,形成取sp杂化的Au(I)配合物。
(1)画出A的结构式_______ 。
(2)分别写出合成A的方法ii、iii中化学反应的方程式______ 、________ 。
(3)画出B的结构式_______ 。
(4)写出A在硫酸铁存在下溶解金的离子方程式________ 。
(5)A和Au(I)形成的配合物中配位原子是________ 。
(6)在提炼金时,A可被氧化成C:2A→C+2e-;C能提高金的溶解速率。画出C的结构式______ 。写出C和Au反应的方程式_________ 。
i.142°C下加热硫氰酸铵;
ii.CS2与氨反应;
iii.CaCN2和(NH4)2S水溶液反应(放出氨气)。
常温下,A在水溶液中可发生异构化反应,部分转化成B.酸性溶液中,A在氧化剂(如Fe3+、H2O2和O2)存在下能溶解金,形成取sp杂化的Au(I)配合物。
(1)画出A的结构式
(2)分别写出合成A的方法ii、iii中化学反应的方程式
(3)画出B的结构式
(4)写出A在硫酸铁存在下溶解金的离子方程式
(5)A和Au(I)形成的配合物中配位原子是
(6)在提炼金时,A可被氧化成C:2A→C+2e-;C能提高金的溶解速率。画出C的结构式
您最近一年使用:0次
2 . 根据条件书写化学反应方程式。
(1)工业上用碳酸氢铵和镁硼石[Mg2B2O4(OH)2]在水溶液中反应制备硼酸________ 。
(2)从乏燃料提取钚元素的过程中,利用亚硝酸钠在强酸溶液中将Pu3+氧化为Pu4+,放出笑气________ 。
(3)NaBH4 与氯化镍(摩尔比2:1)在水溶液中反应,可得到两种硼化物:硼化镍和硼酸(摩尔比1:3)________ 。
(4)通过KMnO4和H2O2在KF-HF介质中反应获得化学法制F2的原料K2MnF6________ 。
(5)磷化氬与甲醛的硫酸溶液反应,产物仅为硫酸鏻(盐)________ 。
(1)工业上用碳酸氢铵和镁硼石[Mg2B2O4(OH)2]在水溶液中反应制备硼酸
(2)从乏燃料提取钚元素的过程中,利用亚硝酸钠在强酸溶液中将Pu3+氧化为Pu4+,放出笑气
(3)NaBH4 与氯化镍(摩尔比2:1)在水溶液中反应,可得到两种硼化物:硼化镍和硼酸(摩尔比1:3)
(4)通过KMnO4和H2O2在KF-HF介质中反应获得化学法制F2的原料K2MnF6
(5)磷化氬与甲醛的硫酸溶液反应,产物仅为硫酸鏻(盐)
您最近一年使用:0次
3 . 写出下列各化学反应的方程式。
(1)将热的硝酸铅溶液滴入热的铬酸钾溶液产生碱式铬酸铅沉淀[ Pb2( OH)2CrO4]_______ 。
(2)向含氰化氢的废水中加入铁粉和K2CO3制备黄血盐[K4Fe(CN)6·3H2O]_______ 。
(3)酸性溶液中,黄血盐用KMnO4处理,被彻底氧化,产生NO 和CO2
和CO2_______ 。
(4)在水中,Ag2SO4与单质S作用,沉淀变为Ag2S分离,所得溶液中加碘水不褪色_______ 。
(1)将热的硝酸铅溶液滴入热的铬酸钾溶液产生碱式铬酸铅沉淀[ Pb2( OH)2CrO4]
(2)向含氰化氢的废水中加入铁粉和K2CO3制备黄血盐[K4Fe(CN)6·3H2O]
(3)酸性溶液中,黄血盐用KMnO4处理,被彻底氧化,产生NO
 和CO2
和CO2(4)在水中,Ag2SO4与单质S作用,沉淀变为Ag2S分离,所得溶液中加碘水不褪色
您最近一年使用:0次
4 . 金属A常用于铁的防护。A与氯气反应,生成易挥发的液态物质B,B和过量A反应生成具有还原性的物质C ,C可以还原Fe3+;B和格氏试剂( C6H5MgBr)反应生成D(含元素A碳和氢)。D和B反应得到E,E水解、聚合成链状的F并放出HCl。向B的盐酸溶液中通入H,S,得到金黄色沉淀G(俗名“金粉”), G溶于硫化铵溶液得到 H。向C的盐酸溶液中通入 H2S,得到黑色沉淀I,I可溶于多硫化铵溶液但不溶于硫化铵溶液。写出A~ I的化学式A_____ B______ C______ D______ E______ F_____ G____ H______ I _____ 。
您最近一年使用:0次
解题方法
5 . 保险粉(Na2S2O4·2H2O)是重要的化工产品,用途广泛,可用来除去废水(pH~8) 中的Cr(VI),所得含硫产物中硫以S(IV)存在。写出反应的离子方程式____ 。
您最近一年使用:0次
名校
6 . +5价V在不同pH下微粒的化学式不同,其微粒与pH关系如表所示。
另外,V价态不同在溶液中颜色不同,如V2+(紫色)、V3+(绿色)、VO2+(蓝色)、VO (黄色)、VO
(黄色)、VO (无色)、V5O
(无色)、V5O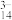 (红棕色)等。下列说法正确的是
(红棕色)等。下列说法正确的是
| 含钒元素的不同微粒 | VO | VO | V2O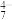 | VO |
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
 (黄色)、VO
(黄色)、VO (无色)、V5O
(无色)、V5O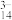 (红棕色)等。下列说法正确的是
(红棕色)等。下列说法正确的是A.VO 转化为V2O 转化为V2O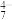 的离子反应为2VO 的离子反应为2VO +H2O=V2O +H2O=V2O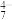 +2H+ +2H+ |
B.含VO 的溶液中滴加氨水有NH4VO3沉淀产生,该过程V元素被还原 的溶液中滴加氨水有NH4VO3沉淀产生,该过程V元素被还原 |
C.酸性VO 滴加烧碱溶液,溶液显红棕色时离子反应为5VO 滴加烧碱溶液,溶液显红棕色时离子反应为5VO +8OH-=V5O +8OH-=V5O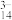 +4H2O +4H2O |
| D.紫色VSO4溶液中滴加酸性高锰酸钾溶液,溶液颜色出现绿色→蓝色→黄色,两个过程均失去1mol电子 |
您最近一年使用:0次
2021-04-14更新
|
978次组卷
|
12卷引用:第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题
第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题河南省洛阳市宜阳县第一高级中学2023-2024学年高一下学期竞赛选拔赛化学试题湖北师大附中2021届高三下学期教学质量测评化学试题(已下线)2021年高考化学押题预测卷(山东卷)02(含考试版、答题卡、参考答案、全解全析)湖北省华大新高考联盟2021-2022学年高三下学期开学考试化学试题浙江省绍兴市2022届高三选考科目适应性考试(二模)化学试题陕西省西安市长安区第一中学2021-2022学年高一下学期期末考试化学(理科)试题陕西省西安市长安区第一中学2021-2022学年高一下学期期末考试化学(理科)试题黑龙江省富锦市第一中学2022-2023学年高二下学期期末考试化学试题湖北省武汉市第六中学2023-2024学年高三上学期第一次月考化学试题河南省济源市第四中学2023-2024学年高一上学期11月月考化学试题河南省周口恒大中学2023-2024学年高三下学期4月期中考试化学试题
解题方法
7 . 废旧印刷电路板是一种电子废弃物,某化学小组利用该电子废弃物回收铜和制取胆矾,实验流程简图如下:

已知:①步骤I涉及的反应为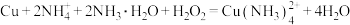
②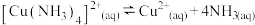
请回答:
(1)步骤I中, 作用是作为反应物和
作用是作为反应物和_______ ,步骤I的分离操作名称为_______ 。
(2)①步骤Ⅱ涉及的离子反应方程式为_______ 。
②步骤Ⅱ可以分解为以下实验步骤,正确的操作顺序是_______ (用相应的编号填写)
a.把混合液加入分液漏斗中,并盖好玻璃塞
b.检验分液漏斗旋塞芯和玻璃塞是否漏水
c.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔
d.倒转漏斗用力振荡,并不断放气,振荡完毕,把分液漏斗放正在铁架台的铁圈中
e.将分液漏斗上口倒出上层溶液
f.旋开活塞,用烧杯接收溶液
③步骤Ⅱ中,影响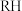 对铜元素萃取率的主要因素有
对铜元素萃取率的主要因素有_______
A.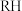 的浓度 B.压强 C.温度 D.铜氨溶液的
的浓度 B.压强 C.温度 D.铜氨溶液的 值
值
(3)步骤Ⅳ,以石墨作电极电解 溶液。阴极析出铜,阳极产物是
溶液。阴极析出铜,阳极产物是_______ 。
(4)步骤V,制取胆矾的主要步骤是_______ (填字母,按操作顺序写)
a.过滤 b.蒸发浓缩,冷却结晶 c.蒸发结晶 d.加入少量 e.洗涤 f.烘干 g.低温干燥
e.洗涤 f.烘干 g.低温干燥
(5)上述实验流程中可以循环使用的物质有_______

已知:①步骤I涉及的反应为
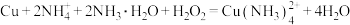
②
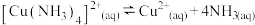
请回答:
(1)步骤I中,
 作用是作为反应物和
作用是作为反应物和(2)①步骤Ⅱ涉及的离子反应方程式为
②步骤Ⅱ可以分解为以下实验步骤,正确的操作顺序是
a.把混合液加入分液漏斗中,并盖好玻璃塞
b.检验分液漏斗旋塞芯和玻璃塞是否漏水
c.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔
d.倒转漏斗用力振荡,并不断放气,振荡完毕,把分液漏斗放正在铁架台的铁圈中
e.将分液漏斗上口倒出上层溶液
f.旋开活塞,用烧杯接收溶液
③步骤Ⅱ中,影响
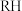 对铜元素萃取率的主要因素有
对铜元素萃取率的主要因素有A.
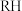 的浓度 B.压强 C.温度 D.铜氨溶液的
的浓度 B.压强 C.温度 D.铜氨溶液的 值
值(3)步骤Ⅳ,以石墨作电极电解
 溶液。阴极析出铜,阳极产物是
溶液。阴极析出铜,阳极产物是(4)步骤V,制取胆矾的主要步骤是
a.过滤 b.蒸发浓缩,冷却结晶 c.蒸发结晶 d.加入少量
 e.洗涤 f.烘干 g.低温干燥
e.洗涤 f.烘干 g.低温干燥(5)上述实验流程中可以循环使用的物质有
您最近一年使用:0次
8 . 以 和
和 制备
制备 的过程中出现一种灰绿色物质X。称取此物质
的过程中出现一种灰绿色物质X。称取此物质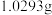 ,用稀盐酸溶解完全后,定量转移到
,用稀盐酸溶解完全后,定量转移到 容量瓶中,以水稀释至刻度,摇匀,得样品液。
容量瓶中,以水稀释至刻度,摇匀,得样品液。
①移取样品液 于锥形瓶中,加入
于锥形瓶中,加入 ,用
,用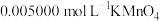 ,溶液滴定至终点,消耗
,溶液滴定至终点,消耗 溶液
溶液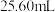 。
。
②移取样品液 于碘量瓶中,加适量水及
于碘量瓶中,加适量水及 后,在暗处放置5分钟。加水
后,在暗处放置5分钟。加水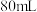 。立即以
。立即以 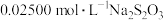 溶液滴定至浅黄色,再加入淀粉溶液滴定至蓝色消失。消耗
溶液滴定至浅黄色,再加入淀粉溶液滴定至蓝色消失。消耗 ,溶液
,溶液 。
。
③移取样品液 于小烧杯中,滴入
于小烧杯中,滴入 至
至 左右,缓慢加入过量的
左右,缓慢加入过量的 溶液。静置一定时间后,过滤、烘干、灰化,在
溶液。静置一定时间后,过滤、烘干、灰化,在 下灼烧至恒重,称得固体物净重
下灼烧至恒重,称得固体物净重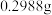 。
。
根据实验结果和相关方法测定后,发现X的化学式可以表示为:n×氧化物·m×盐·y×氢氧化物,且 是最小正整数比。
是最小正整数比。
请回答下列问题:
(1)根据上述实验,计算并推出X的化学式____ (以氧化物·盐·氢氧化物形式表示)。
(2)写出 和
和 反应生成X的化学方程式
反应生成X的化学方程式____ 。
 和
和 制备
制备 的过程中出现一种灰绿色物质X。称取此物质
的过程中出现一种灰绿色物质X。称取此物质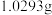 ,用稀盐酸溶解完全后,定量转移到
,用稀盐酸溶解完全后,定量转移到 容量瓶中,以水稀释至刻度,摇匀,得样品液。
容量瓶中,以水稀释至刻度,摇匀,得样品液。①移取样品液
 于锥形瓶中,加入
于锥形瓶中,加入 ,用
,用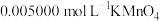 ,溶液滴定至终点,消耗
,溶液滴定至终点,消耗 溶液
溶液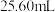 。
。②移取样品液
 于碘量瓶中,加适量水及
于碘量瓶中,加适量水及 后,在暗处放置5分钟。加水
后,在暗处放置5分钟。加水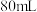 。立即以
。立即以 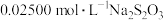 溶液滴定至浅黄色,再加入淀粉溶液滴定至蓝色消失。消耗
溶液滴定至浅黄色,再加入淀粉溶液滴定至蓝色消失。消耗 ,溶液
,溶液 。
。③移取样品液
 于小烧杯中,滴入
于小烧杯中,滴入 至
至 左右,缓慢加入过量的
左右,缓慢加入过量的 溶液。静置一定时间后,过滤、烘干、灰化,在
溶液。静置一定时间后,过滤、烘干、灰化,在 下灼烧至恒重,称得固体物净重
下灼烧至恒重,称得固体物净重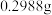 。
。根据实验结果和相关方法测定后,发现X的化学式可以表示为:n×氧化物·m×盐·y×氢氧化物,且
 是最小正整数比。
是最小正整数比。请回答下列问题:
(1)根据上述实验,计算并推出X的化学式
(2)写出
 和
和 反应生成X的化学方程式
反应生成X的化学方程式
您最近一年使用:0次
9 .  与盐酸反应有黄绿色气体生成,离子方程式正确的是
与盐酸反应有黄绿色气体生成,离子方程式正确的是
 与盐酸反应有黄绿色气体生成,离子方程式正确的是
与盐酸反应有黄绿色气体生成,离子方程式正确的是A. |
B. |
C.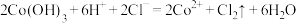 |
D. |
您最近一年使用:0次
名校
解题方法
10 . 书写反应方程式(提示:要求系数为最简整数比;(1)和(2)中自然条件复杂,合理选择即可)。
(1)关于地球的演化,目前主要的观点是,原始地球上没有氧气,在无氧或氧气含量很低时,原核生物可利用自然存在的有机质(用CH2O表示)和某些无机物反应获得能量。例如, 和MnO2可分别作为上述过程的氧化剂,前者生成黄色浑浊物,二者均放出无色无味气体。
和MnO2可分别作为上述过程的氧化剂,前者生成黄色浑浊物,二者均放出无色无味气体。
①写出 参与的释能反应的离子方程式
参与的释能反应的离子方程式______ 。
②写出MnO2参与的释能反应的离子方程式______ 。
(2)约27亿年前光合作用开始发生,随着这一过程的进行,地球上氧气不断积累,经过漫长的演变终达到如今的含量。氧气的形成和积累,导致地球上自然物质的分布发生变化。
①溶解在海洋中的Fe2+被氧化转变成针铁矿α-FeO(OH)而沉积,写出离子方程式______ 。
②与铁的沉积不同,陆地上的MoS2被氧化而导致钼溶于海洋而析出单质硫,写出离子方程式______ 。
(3)2020年8月4日晚,贝鲁特港口发生了举世震惊的大爆炸,现场升起红棕色蘑菇云,破坏力巨大。目前认定大爆炸为该港口存储的约2750吨硝酸铵的分解。另外,亚硝酸胺受热亦发生分解甚至爆炸,若小心控制则可用在需要充气的过程如乒乓球的制造之中。
①写出硝酸铵分解出红棕色气体的反应方程式______ 。
②写出亚硝酸铵受热分解用于充气的反应方程式______ 。
(1)关于地球的演化,目前主要的观点是,原始地球上没有氧气,在无氧或氧气含量很低时,原核生物可利用自然存在的有机质(用CH2O表示)和某些无机物反应获得能量。例如,
 和MnO2可分别作为上述过程的氧化剂,前者生成黄色浑浊物,二者均放出无色无味气体。
和MnO2可分别作为上述过程的氧化剂,前者生成黄色浑浊物,二者均放出无色无味气体。①写出
 参与的释能反应的离子方程式
参与的释能反应的离子方程式②写出MnO2参与的释能反应的离子方程式
(2)约27亿年前光合作用开始发生,随着这一过程的进行,地球上氧气不断积累,经过漫长的演变终达到如今的含量。氧气的形成和积累,导致地球上自然物质的分布发生变化。
①溶解在海洋中的Fe2+被氧化转变成针铁矿α-FeO(OH)而沉积,写出离子方程式
②与铁的沉积不同,陆地上的MoS2被氧化而导致钼溶于海洋而析出单质硫,写出离子方程式
(3)2020年8月4日晚,贝鲁特港口发生了举世震惊的大爆炸,现场升起红棕色蘑菇云,破坏力巨大。目前认定大爆炸为该港口存储的约2750吨硝酸铵的分解。另外,亚硝酸胺受热亦发生分解甚至爆炸,若小心控制则可用在需要充气的过程如乒乓球的制造之中。
①写出硝酸铵分解出红棕色气体的反应方程式
②写出亚硝酸铵受热分解用于充气的反应方程式
您最近一年使用:0次
2021-03-22更新
|
393次组卷
|
2卷引用:2020年第34届中国化学会奥林匹克化学竞赛初赛试题



