1 . 高锰酸钾是一种典型的强氧化剂。完成下列填空:
Ⅰ:在用 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生的反应如下:
和CuS的混合物时,发生的反应如下:
①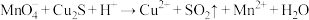 (未配平)
(未配平)
②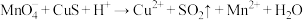 (未配平)
(未配平)
(1)下列关于反应①的说法中错误的是___________ (填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24L(标况下) ,转移电子的物质的量是0.8mol
,转移电子的物质的量是0.8mol
d.还原性的强弱关系是: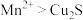
Ⅱ:在稀硫酸中, 与也能发生氧化还原反应。
与也能发生氧化还原反应。
(2)配平 与
与 反应的离子方程式:
反应的离子方程式:___________

(3)欲配制480mL0.1mol/L 溶液,需称取
溶液,需称取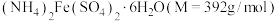 的质量为
的质量为___________ g,需要的玻璃仪器有___________ 。
Ⅲ:实验室可由软锰矿(主要成分为 )制备
)制备 ,方法如下:高温下使软锰矿与过量
,方法如下:高温下使软锰矿与过量 和
和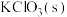 反应,生成
反应,生成 (锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,
(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液, 转化为
转化为 和
和 ;再滤去沉淀
;再滤去沉淀 ,浓缩结晶得到
,浓缩结晶得到 晶体。请回答:
晶体。请回答:
(4)用软锰矿制备 的化学方程式是:
的化学方程式是:___________ 。
(5) 转化为
转化为 的反应中氧化剂和还原剂的物质的量之比为
的反应中氧化剂和还原剂的物质的量之比为___________ 。
Ⅰ:在用
 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生的反应如下:
和CuS的混合物时,发生的反应如下:①
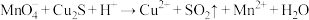 (未配平)
(未配平)②
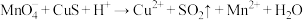 (未配平)
(未配平)(1)下列关于反应①的说法中错误的是
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24L(标况下)
 ,转移电子的物质的量是0.8mol
,转移电子的物质的量是0.8mold.还原性的强弱关系是:
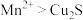
Ⅱ:在稀硫酸中,
 与也能发生氧化还原反应。
与也能发生氧化还原反应。(2)配平
 与
与 反应的离子方程式:
反应的离子方程式:
(3)欲配制480mL0.1mol/L
 溶液,需称取
溶液,需称取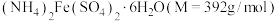 的质量为
的质量为Ⅲ:实验室可由软锰矿(主要成分为
 )制备
)制备 ,方法如下:高温下使软锰矿与过量
,方法如下:高温下使软锰矿与过量 和
和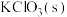 反应,生成
反应,生成 (锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,
(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液, 转化为
转化为 和
和 ;再滤去沉淀
;再滤去沉淀 ,浓缩结晶得到
,浓缩结晶得到 晶体。请回答:
晶体。请回答:(4)用软锰矿制备
 的化学方程式是:
的化学方程式是:(5)
 转化为
转化为 的反应中氧化剂和还原剂的物质的量之比为
的反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
解题方法
2 . 若做实验时不小心粘上高锰酸钾,皮肤上的斑要很久才能消除,而用 的稀溶液在稀硫酸条件下洗涤,可以马上消除,发生反应的化学方程式为
的稀溶液在稀硫酸条件下洗涤,可以马上消除,发生反应的化学方程式为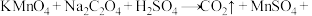

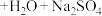 (未配平),下列关于此反应的叙述正确的是
(未配平),下列关于此反应的叙述正确的是
 的稀溶液在稀硫酸条件下洗涤,可以马上消除,发生反应的化学方程式为
的稀溶液在稀硫酸条件下洗涤,可以马上消除,发生反应的化学方程式为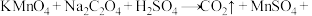

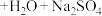 (未配平),下列关于此反应的叙述正确的是
(未配平),下列关于此反应的叙述正确的是A.当有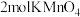 参加反应时,该反应转移10 mol电子 参加反应时,该反应转移10 mol电子 |
B.该反应右边方框内的产物是 |
C.该反应的氧化剂是 |
D.配平后, 的化学计量数是10 的化学计量数是10 |
您最近一年使用:0次
3 . 羟胺(H2NOH)是一种常见的化工原料,常用于农药制备。实际生产中,羟胺一般会过量加入以保证反应充分进行。因此,羟胺在废水中或多或少都会有残留。通常需要将废水中的羟胺氧化,才能再进行下一步处置。取25.00mL废水样品,加入过量Fe(III)充分反应(反应1),放出笑气,用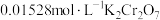 测定产生的Fe(II)(反应2),消耗14.48mL。
测定产生的Fe(II)(反应2),消耗14.48mL。
(1)写出反应1和反应2的方程式___________ 、___________ 。
(2)计算该废水样品中羟胺的浓度___________ 。( )
)
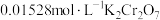 测定产生的Fe(II)(反应2),消耗14.48mL。
测定产生的Fe(II)(反应2),消耗14.48mL。(1)写出反应1和反应2的方程式
(2)计算该废水样品中羟胺的浓度
 )
)
您最近一年使用:0次
解题方法
4 . 在铋系高温超导材料的探索中,得到样品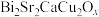 ,其中Cu可能存在的价态为+2和+3,Bi的可能价态为+3和+5.设计如下实验测定两种元素的平均氧化态。
,其中Cu可能存在的价态为+2和+3,Bi的可能价态为+3和+5.设计如下实验测定两种元素的平均氧化态。
实验A:将102.3mg样品(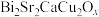 ,式量为760.4+16.00x)溶于100.0mL含有
,式量为760.4+16.00x)溶于100.0mL含有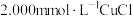 的
的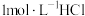 溶液中,以库仑滴定法测定过量的
溶液中,以库仑滴定法测定过量的 ,结果为0.1085mmol。
,结果为0.1085mmol。
实验B:将94.6mg样品溶解于 的酸性溶液中。以库仑滴定法测定过量的
的酸性溶液中。以库仑滴定法测定过量的 ,结果为0.0577mmol。
,结果为0.0577mmol。
(1)写出实验A中样品溶解时涉及氧化还原反应的所有方程式___________ 。
(2)写出实验B中样品溶解时涉及氧化还原反应的所有方程式___________ 。
(3)求算样品中Bi和Cu的氧化数,确定化学式中x的值___________ 。
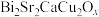 ,其中Cu可能存在的价态为+2和+3,Bi的可能价态为+3和+5.设计如下实验测定两种元素的平均氧化态。
,其中Cu可能存在的价态为+2和+3,Bi的可能价态为+3和+5.设计如下实验测定两种元素的平均氧化态。实验A:将102.3mg样品(
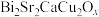 ,式量为760.4+16.00x)溶于100.0mL含有
,式量为760.4+16.00x)溶于100.0mL含有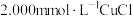 的
的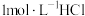 溶液中,以库仑滴定法测定过量的
溶液中,以库仑滴定法测定过量的 ,结果为0.1085mmol。
,结果为0.1085mmol。实验B:将94.6mg样品溶解于
 的酸性溶液中。以库仑滴定法测定过量的
的酸性溶液中。以库仑滴定法测定过量的 ,结果为0.0577mmol。
,结果为0.0577mmol。(1)写出实验A中样品溶解时涉及氧化还原反应的所有方程式
(2)写出实验B中样品溶解时涉及氧化还原反应的所有方程式
(3)求算样品中Bi和Cu的氧化数,确定化学式中x的值
您最近一年使用:0次
解题方法
5 . 化学方程式书写:
(1)氧化银(Ⅰ)被过氧化氢还原______ 。
(2)四氟合金酸(Ⅲ)银遇冷水后,分解出一酸一碱一盐(盐是常见的可溶性盐)______ 。
(3)二氯亚砜与二氧化铅反应制备二氯化铅______ 。
(4)由三氟化氮、氟气及五氟化砷反应制备四氟铵盐______ 。
(5)氯化亚锡在盐酸溶液中还原氯化汞,得到抗磁性的一价汞盐沉淀和六氯合锡酸______ 。
(1)氧化银(Ⅰ)被过氧化氢还原
(2)四氟合金酸(Ⅲ)银遇冷水后,分解出一酸一碱一盐(盐是常见的可溶性盐)
(3)二氯亚砜与二氧化铅反应制备二氯化铅
(4)由三氟化氮、氟气及五氟化砷反应制备四氟铵盐
(5)氯化亚锡在盐酸溶液中还原氯化汞,得到抗磁性的一价汞盐沉淀和六氯合锡酸
您最近一年使用:0次
6 . 能正确表示下列反应的离子方程式是
A.用碳酸钠溶液处理水垢中的硫酸钙: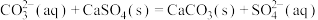 |
B.用足量氨水吸收二氧化硫: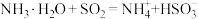 |
C.向草酸溶液中滴加酸性高锰酸钾溶液: |
D.将等物质的量浓度的氢氧化钡溶液和硫酸氢铵溶液以体积比1∶2混合: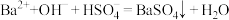 |
您最近一年使用:0次
7 . 下列反应方程式书写错误的是
A.制备 |
B.制备铁粉: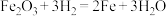 |
C.过氧化钠与 反应: 反应: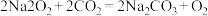 |
D.碳酸氢钙溶液与少量NaOH反应: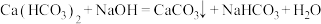 |
您最近一年使用:0次
8 . Ⅰ.氧化铁是重要工业颜料,用废铁屑制备氧化铁的流程如图:
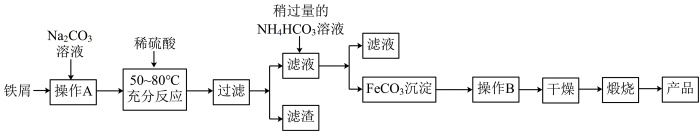
回答下列问题:
(1)检验“操作B”是否彻底的操作为_______ 。
(2)写出加入稍过量的NH4HCO3溶液得到FeCO3的离子方程式:_______ 。
(3)写出在空气中充分加热煅烧FeCO3的化学方程式:_______ 。
Ⅱ.上述流程中,若煅烧不充分,最终产品中会含有少量的FeO杂质。某同学为测定产品中Fe2O3的含量,进行如下实验:
a.称取样品8.00 g,加入足量稀H2SO4溶解,并加水稀释至100 mL;
b.量取25.00 mL待测溶液于锥形瓶中;
c.用酸化的0. 010 00 mol·L-1KMnO4标准液滴定至终点;
d.重复操作b、c 2~3次,得出消耗KMnO4溶液体积的平均值为20.00 mL。
(4)确定滴定达到终点的操作及现象为_______ 。
(5)上述样品的质量分数为_______ 。
(6)下列操作会导致样品中Fe2O3的质量分数测定结果偏低的有_______(填字母) 。

回答下列问题:
(1)检验“操作B”是否彻底的操作为
(2)写出加入稍过量的NH4HCO3溶液得到FeCO3的离子方程式:
(3)写出在空气中充分加热煅烧FeCO3的化学方程式:
Ⅱ.上述流程中,若煅烧不充分,最终产品中会含有少量的FeO杂质。某同学为测定产品中Fe2O3的含量,进行如下实验:
a.称取样品8.00 g,加入足量稀H2SO4溶解,并加水稀释至100 mL;
b.量取25.00 mL待测溶液于锥形瓶中;
c.用酸化的0. 010 00 mol·L-1KMnO4标准液滴定至终点;
d.重复操作b、c 2~3次,得出消耗KMnO4溶液体积的平均值为20.00 mL。
(4)确定滴定达到终点的操作及现象为
(5)上述样品的质量分数为
(6)下列操作会导致样品中Fe2O3的质量分数测定结果偏低的有_______(填字母) 。
| A.未干燥锥形瓶 |
| B.盛装标准液的滴定管没有用标准液润洗 |
| C.滴定开始时平视刻度线读数,滴定结束时仰视刻度线读数 |
| D.量取待测液的滴定管没有润洗 |
您最近一年使用:0次
9 . 乳酸亚铁 常用作缺铁性贫血的补铁剂,能溶于水。
常用作缺铁性贫血的补铁剂,能溶于水。
(1)一般由乳酸钙与氯化亚铁两水溶液混合制得,通过重结晶提纯。
①写出制备乳酸亚铁的离子方程式___________ 。
②1mol乳酸亚铁受热至75℃和170℃时失水,失水质量分别为___________ g、___________ g。
③画出乳酸亚铁的空间立体结构___________ 。
(2)乳酸亚铁还原性的检验
①取乳酸亚铁溶于水,加入酸性高锰酸钾溶液,搅拌后紫色慢慢褪去,溶液变成棕黄色。1mol乳酸亚铁消耗了0.2mol ,化学方程式为
,化学方程式为___________ 。
②1mol乳酸亚铁溶液与5%的双氧水反应,反应剧烈且消耗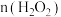 大于1.5mol。控制反应速率后,多次实验,发现消耗
大于1.5mol。控制反应速率后,多次实验,发现消耗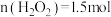 。消耗
。消耗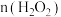 大于1.5mol的原因:
大于1.5mol的原因:___________ 、___________ 。
③双氧水与乳酸亚铁的反应速率远大于酸性高锰酸钾,为了进一步探寻原因,实验设计如下:___________ 。
 常用作缺铁性贫血的补铁剂,能溶于水。
常用作缺铁性贫血的补铁剂,能溶于水。(1)一般由乳酸钙与氯化亚铁两水溶液混合制得,通过重结晶提纯。
①写出制备乳酸亚铁的离子方程式
②1mol乳酸亚铁受热至75℃和170℃时失水,失水质量分别为
③画出乳酸亚铁的空间立体结构
(2)乳酸亚铁还原性的检验
①取乳酸亚铁溶于水,加入酸性高锰酸钾溶液,搅拌后紫色慢慢褪去,溶液变成棕黄色。1mol乳酸亚铁消耗了0.2mol
 ,化学方程式为
,化学方程式为②1mol乳酸亚铁溶液与5%的双氧水反应,反应剧烈且消耗
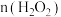 大于1.5mol。控制反应速率后,多次实验,发现消耗
大于1.5mol。控制反应速率后,多次实验,发现消耗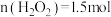 。消耗
。消耗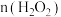 大于1.5mol的原因:
大于1.5mol的原因:③双氧水与乳酸亚铁的反应速率远大于酸性高锰酸钾,为了进一步探寻原因,实验设计如下:
您最近一年使用:0次
名校
10 . I.某温度时,在0.5L密闭容器中,某一可逆反应的A、B气体物质的量随时间变化的曲线如下图所示,由图中数据分析可得:
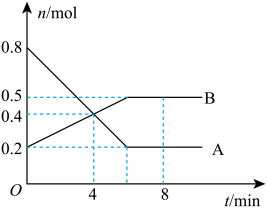
(1)该反应的化学方程式为___________ 。
(2)第4min时,正、逆反应速率的大小关系为v正___________ (填“>” “<”或“=”)v逆
(3)0~ 4min内,用B的浓度变化来表示该反应的平均反应速率为___________ mol ·L-1·min-1。
(4)平衡时混合气体中B的体积分数为___________ 。
II.某同学根据外界条件对化学反应速率影响的原理,设计了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如下表,请结合表中信息,回答有关问题:
(5)写出上述反应的离子方程式___________ 。
(6)若实验探究温度对该反应速率的影响,则a=___________ 采用比较实验的序号是___________ (填实验序号)

(1)该反应的化学方程式为
(2)第4min时,正、逆反应速率的大小关系为v正
(3)0~ 4min内,用B的浓度变化来表示该反应的平均反应速率为
(4)平衡时混合气体中B的体积分数为
II.某同学根据外界条件对化学反应速率影响的原理,设计了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如下表,请结合表中信息,回答有关问题:
| 实验序号 | 反应温度(°C) | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
| A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| B | 20 | 5 | 0.1 | 10 | 0.1 | a |
| C | 25 | 10 | 0.1 | 5 | 0.1 | 5 |
| D | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
(6)若实验探究温度对该反应速率的影响,则a=
您最近一年使用:0次
2023-05-16更新
|
339次组卷
|
2卷引用:广东省揭阳市普宁市勤建学校2022-2023学年高一下学期学科竞赛化学试题



