名校
1 . 工业制备硝酸的过程中,会产生氮的氧化物等空气污染物。为减少环境污染,需要用氢氧化钠溶液吸收尾气,反应的化学方程式为 ,则
,则 的化学式为
的化学式为
 ,则
,则 的化学式为
的化学式为A. | B. | C. | D.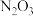 |
您最近一年使用:0次
名校
解题方法
2 . 取一定量的酸性 溶液依次进行下列实验,有关现象记录如下:
溶液依次进行下列实验,有关现象记录如下:
(1)能不能用盐酸酸化 溶液,为什么?
溶液,为什么?_______ 。
(2)酸性 溶液滴加适量
溶液滴加适量 ,紫红色褪去,并有无色气泡产生;反应的离子方程式为
,紫红色褪去,并有无色气泡产生;反应的离子方程式为_______ 。
再加入适量的固体 ,固体溶解,溶液又变为紫红色。
,固体溶解,溶液又变为紫红色。
(3) 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
 溶液依次进行下列实验,有关现象记录如下:
溶液依次进行下列实验,有关现象记录如下:(1)能不能用盐酸酸化
 溶液,为什么?
溶液,为什么?(2)酸性
 溶液滴加适量
溶液滴加适量 ,紫红色褪去,并有无色气泡产生;反应的离子方程式为
,紫红色褪去,并有无色气泡产生;反应的离子方程式为再加入适量的固体
 ,固体溶解,溶液又变为紫红色。
,固体溶解,溶液又变为紫红色。(3)
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为
您最近一年使用:0次
名校
3 . 高铁酸钾( )是一种新型、高效、多功能绿色水处理剂。
)是一种新型、高效、多功能绿色水处理剂。

资料:① 为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降,与水反应放出氧气。
为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降,与水反应放出氧气。
② 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
③ 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用。
胶体,可除去水中细微的悬浮物,有净水作用。
(1)A为氯气发生装置,发生反应的化学方程式为_______ 。
(2)用“双线桥”表示上述化学方程式中电子转移的情况_______ 。
(3)装置C中制备 时,发生反应的离子方程式为
时,发生反应的离子方程式为_______ 。
(4)B中盛放的是_______ 溶液。D中发生反应的离子方程式为_______ 。
(5) 与水反应的化学方程式为
与水反应的化学方程式为_______ 。
 )是一种新型、高效、多功能绿色水处理剂。
)是一种新型、高效、多功能绿色水处理剂。
资料:①
 为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降,与水反应放出氧气。
为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降,与水反应放出氧气。②
 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。③
 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用。
胶体,可除去水中细微的悬浮物,有净水作用。(1)A为氯气发生装置,发生反应的化学方程式为
(2)用“双线桥”表示上述化学方程式中电子转移的情况
(3)装置C中制备
 时,发生反应的离子方程式为
时,发生反应的离子方程式为(4)B中盛放的是
(5)
 与水反应的化学方程式为
与水反应的化学方程式为
您最近一年使用:0次
名校
4 . SnCl2粗品中往往含有少量的SnCl4。SnSO4是一种重要的可溶性硫酸盐,广泛应用于镀锡工业,其制备路线如下:
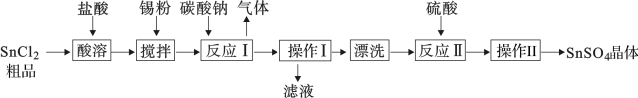
回答下列问题:
(1)SnSO4中Sn的化合价为___________ 。
(2)加入锡粉搅拌时可能发生的化学反应为___________ 。
(3)操作I的名称是___________ ,在实验室进行操作II的步骤有___________ 、___________ 过滤、洗涤、干燥。
(4)滤液中溶质主要成分是___________ 。证明其中所含金属阳离子的方法是___________ 。

回答下列问题:
(1)SnSO4中Sn的化合价为
(2)加入锡粉搅拌时可能发生的化学反应为
(3)操作I的名称是
(4)滤液中溶质主要成分是
您最近一年使用:0次
名校
5 . H5IO6是白色晶体,易溶于水,在强酸溶液中能与Mn2+发生反应:_______Mn2++_______H5IO6=_______MnO +_______IO
+_______IO +_______H++_______H2O
+_______H++_______H2O
(1)配平上述离子反应_______ 。
(2)根据以上离子方程式判断,H5IO6是_______ (填“易”或“难”,下同)电离物质,HIO3是_______ 电离物质。
(3)上述反应中,被氧化的元素是_______ (填元素符号),当1molMn2+参加反应时,转移电子的物质的量为_______ 。
 +_______IO
+_______IO +_______H++_______H2O
+_______H++_______H2O(1)配平上述离子反应
(2)根据以上离子方程式判断,H5IO6是
(3)上述反应中,被氧化的元素是
您最近一年使用:0次



