解题方法
1 . 以高硫铝土矿(主要成分为 、
、 ,还含有少量
,还含有少量 )为原料,生产
)为原料,生产 并获得
并获得 的部分工艺流程如图所示:
的部分工艺流程如图所示:
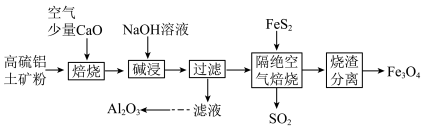
回答下列问题:
(1) “焙烧”时为使原料快速、充分反应,可采取的措施有____________________ (答出2条);加入少量 的目的是
的目的是____________________ ,此过程 最终生成的产物是
最终生成的产物是__________ (填名称)。
(2)“碱浸”时发生反应的离子方程式为____________________ 。
(3)若在实验室进行“过滤”操作,使用的玻璃仪器有____________________ 。
(4)“隔绝空气焙烧”时,反应的化学方程式是____________________ 。
(5)根据 的性质,“烧渣分离”可用
的性质,“烧渣分离”可用__________ 法。
 、
、 ,还含有少量
,还含有少量 )为原料,生产
)为原料,生产 并获得
并获得 的部分工艺流程如图所示:
的部分工艺流程如图所示:
回答下列问题:
(1) “焙烧”时为使原料快速、充分反应,可采取的措施有
 的目的是
的目的是 最终生成的产物是
最终生成的产物是(2)“碱浸”时发生反应的离子方程式为
(3)若在实验室进行“过滤”操作,使用的玻璃仪器有
(4)“隔绝空气焙烧”时,反应的化学方程式是
(5)根据
 的性质,“烧渣分离”可用
的性质,“烧渣分离”可用
您最近一年使用:0次
名校
2 . 氯气是重要的化工原料。如图是实验室制取纯净、干燥氯气的装置图。_________ 。
(2)②的作用是_________ ,③中盛放的试剂是_________ 。
(3)⑤中反应的离子方程式是_________ 。
(4)“地康法”制取氯气的反应原理如下所示:_________ 。
②已知催化剂需参与反应改变反应路径,是前一反应的反应物,后续反应的生成物。则该反应的催化剂是_________ 。
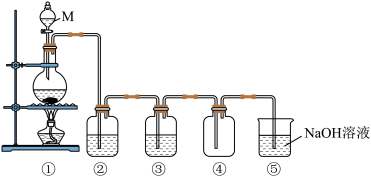
(2)②的作用是
(3)⑤中反应的离子方程式是
(4)“地康法”制取氯气的反应原理如下所示:
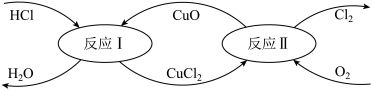
②已知催化剂需参与反应改变反应路径,是前一反应的反应物,后续反应的生成物。则该反应的催化剂是
您最近一年使用:0次
2024-03-23更新
|
37次组卷
|
2卷引用:辽宁普通高中2023-2024学年高一下学期开学考试化学试题
名校
3 . 水合肼(N2H4·H2O)是一种无色透明、具有腐蚀性和强还原性的碱性液体。利用尿素法生产原理为:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCl。回答下列问题:
实验一:制取水合肼(实验装置如图所示)

(1)①直形冷凝管冷却水的进水口为___________ (用“a”或“b”作答)。
②反应过程中需控制温度,同时将A中溶液缓慢滴入三颈烧瓶,若滴速过快则会导致产品产率降低。仪器A中盛装的溶液是___________ (填字母)。
a.NaOH和NaClO溶液 b.CO(NH2)2溶液
用化学方程式解释产率降低的原因:___________ 。
③充分反应后,加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分
实验二:测定馏分中水合肼(N2H4·H2O)含量
(2)称取馏分0.50g配成250mL待测溶液,取25mL待测溶液加入20.00mL0.1000mol/L单质碘的溶液,再加入适量NaHCO3固体调节pH,待水合肼完全转化为N2后,加盐酸调节溶液pH并加入少量淀粉溶液,立即用0.0200mol/LNa2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液的体积为20.00mL。(已知:N2H4·H2O+2I2=N2↑+4HI+H2O,I2+2S2O =2I-+S4O
=2I-+S4O 。)
。)
①滴定时,Na2S2O3溶液盛放在___________ (填“酸式”或“碱式”)滴定管中,本实验滴定终点的现象为___________ 。
②若滴定管用蒸馏水洗涤后,未润洗直接盛放Na2S2O3溶液,最终测得水合肼的纯度会___________ (填“偏低”、“偏高”或“无影响”)。
③馏分中水合肼(N2H4·H2O)的纯度为___________ 。
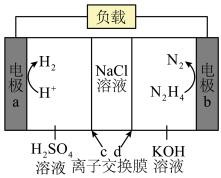
(3)我国科学家以肼(N2H4)为原料设计的新型电池能同时实现H₂制备和海水淡化,装置如图。写出b的电极反应方程式___________ ,离子交换膜c是___________ (填“阴”或“阳”)离子交换膜。
(4)抽滤如图所示,与用普通漏斗过滤相比,抽滤的优点___________ ;其最佳操作顺序是___________ ,确认抽干(填标号)。
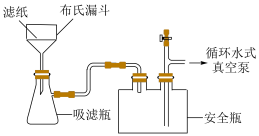
a.打开循环水式真空泵 b.加入少量蒸馏水润湿滤纸 c.转移固液混合物
实验一:制取水合肼(实验装置如图所示)

(1)①直形冷凝管冷却水的进水口为
②反应过程中需控制温度,同时将A中溶液缓慢滴入三颈烧瓶,若滴速过快则会导致产品产率降低。仪器A中盛装的溶液是
a.NaOH和NaClO溶液 b.CO(NH2)2溶液
用化学方程式解释产率降低的原因:
③充分反应后,加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分
实验二:测定馏分中水合肼(N2H4·H2O)含量
(2)称取馏分0.50g配成250mL待测溶液,取25mL待测溶液加入20.00mL0.1000mol/L单质碘的溶液,再加入适量NaHCO3固体调节pH,待水合肼完全转化为N2后,加盐酸调节溶液pH并加入少量淀粉溶液,立即用0.0200mol/LNa2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液的体积为20.00mL。(已知:N2H4·H2O+2I2=N2↑+4HI+H2O,I2+2S2O
 =2I-+S4O
=2I-+S4O 。)
。)①滴定时,Na2S2O3溶液盛放在
②若滴定管用蒸馏水洗涤后,未润洗直接盛放Na2S2O3溶液,最终测得水合肼的纯度会
③馏分中水合肼(N2H4·H2O)的纯度为
(3)我国科学家以肼(N2H4)为原料设计的新型电池能同时实现H₂制备和海水淡化,装置如图。写出b的电极反应方程式

(4)抽滤如图所示,与用普通漏斗过滤相比,抽滤的优点

a.打开循环水式真空泵 b.加入少量蒸馏水润湿滤纸 c.转移固液混合物
您最近一年使用:0次
名校
解题方法
4 . 碱式氯化镁(MgOHCl)常用作塑料添加剂,工业上制备方法较多,装置C中CuO的质量为8.0g。

请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为:___________ 。
(2)装置D中生成沉淀,发生反应的离子方程式为___________ 。
(3)反应过程中持续通入N2的作用有两点:一是:将装置A中产生的氨气完全导出,二是:___________ 。
(4)若测得碱石灰的质量增加了ag,则得到碱式氯化镁的质量为___________ g。
(5)反应完毕,装置C中的氧化铜全部由黑色变为红色,称其质量为6.8g,该反应中转移电子的物质的量为___________ mol,写出装置C中发生的化学反应方程式 ___________ 。

请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为:
(2)装置D中生成沉淀,发生反应的离子方程式为
(3)反应过程中持续通入N2的作用有两点:一是:将装置A中产生的氨气完全导出,二是:
(4)若测得碱石灰的质量增加了ag,则得到碱式氯化镁的质量为
(5)反应完毕,装置C中的氧化铜全部由黑色变为红色,称其质量为6.8g,该反应中转移电子的物质的量为
您最近一年使用:0次
解题方法
5 . 含氮化合物对环境、生产和人类活动有很大影响。
(1)NH 具有还原性。饱和NaNO2(aq)与饱和NH4Cl(aq)混合加热,会产生无色无味气体,写出该过程的化学方程式:
具有还原性。饱和NaNO2(aq)与饱和NH4Cl(aq)混合加热,会产生无色无味气体,写出该过程的化学方程式:___________ ,请设计一个实验方案检验某固体中的阳离子为NH :
:___________ 。
(2)NF3为无色、无味的气体,在潮湿的环境中易变质生成HF、NO、HNO3,写出反应的化学方程式:___________ ;该反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol·L-1,c(HNO3)=1.0mol·L-1.取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为___________ L。
(4)某课题组用间接电解法除NO,其原理如图所示:
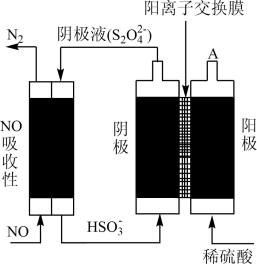
①电解过程中透过阳离子交换膜的离子是___________ 。
②写出电解池阴极的电极反应式:___________ 。
(1)NH
 具有还原性。饱和NaNO2(aq)与饱和NH4Cl(aq)混合加热,会产生无色无味气体,写出该过程的化学方程式:
具有还原性。饱和NaNO2(aq)与饱和NH4Cl(aq)混合加热,会产生无色无味气体,写出该过程的化学方程式: :
:(2)NF3为无色、无味的气体,在潮湿的环境中易变质生成HF、NO、HNO3,写出反应的化学方程式:
(3)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol·L-1,c(HNO3)=1.0mol·L-1.取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
(4)某课题组用间接电解法除NO,其原理如图所示:

①电解过程中透过阳离子交换膜的离子是
②写出电解池阴极的电极反应式:
您最近一年使用:0次
6 . 填空:
(1)用高锰酸钾(KMnO4)测定室内甲醛含量,发生反应如下,配平该方程式:______________ 。






配制KMnO4溶液,定容的操作方法为_______________________ 。
(2)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是__________ (填化学方程式)。
(3)写出Na2SO4和NaCl混合溶液中 的检验方法:
的检验方法:___________________ 。
(4)从硫酸亚铁溶液中获得硫酸亚铁晶体FeSO4•7H2O的实验操作为__________ 、__________ 、过滤、冰水洗涤、烘干。取27.8g FeSO4•7H2O隔绝空气加热至不同温度,剩余固体的质量变化如图所示。
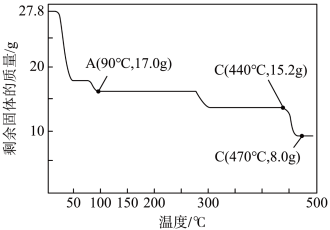
分析数据,写出90℃残留物的化学式:__________ ;440~470℃时固体物质发生反应的化学方程式是________________________ 。
(1)用高锰酸钾(KMnO4)测定室内甲醛含量,发生反应如下,配平该方程式:






配制KMnO4溶液,定容的操作方法为
(2)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是
(3)写出Na2SO4和NaCl混合溶液中
 的检验方法:
的检验方法:(4)从硫酸亚铁溶液中获得硫酸亚铁晶体FeSO4•7H2O的实验操作为

分析数据,写出90℃残留物的化学式:
您最近一年使用:0次
7 . HNO3是极其重要的化工原料,在工业、农业、医药、军事等领域有着广泛的应用,现代工业上常用氨催化氧化制硝酸的流程示意图如下:
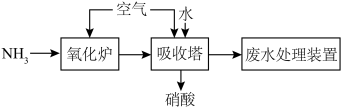
(1)写出“氧化炉”中氨催化氧化的化学方程式:________________________ 。
(2)工业上常用碱液来吸收NOx,有关的化学反应为:
①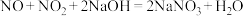 ;
;
② 。
。
现有一定条件下0.2molNO2和0.1molNO的混合气体恰好被200mLNaOH溶液完全吸收,则NaOH溶液的物质的量浓度为____________ mol/L。
(3)已知氨氮废水中氮元素多以 和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为
和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为_______________________________________________ 。
(4)《本草纲目拾遗》记载“强水性最烈,能蚀五金”,请写出稀强水与铜反应的离子方程式:__________________________ 。
(5)长期存放的浓硝酸呈黄色是因为其分解生成的_____________ 溶于硝酸中,实验室常将浓硝酸保存在
__________ 试剂瓶中,并放在__________ 处。

(1)写出“氧化炉”中氨催化氧化的化学方程式:
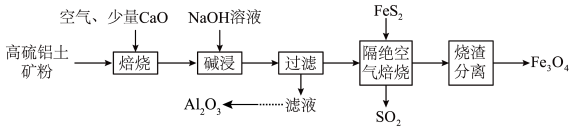
(2)工业上常用碱液来吸收NOx,有关的化学反应为:
①
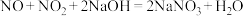 ;
;②
 。
。现有一定条件下0.2molNO2和0.1molNO的混合气体恰好被200mLNaOH溶液完全吸收,则NaOH溶液的物质的量浓度为
(3)已知氨氮废水中氮元素多以
 和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为
和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为(4)《本草纲目拾遗》记载“强水性最烈,能蚀五金”,请写出稀强水与铜反应的离子方程式:
(5)长期存放的浓硝酸呈黄色是因为其分解生成的
您最近一年使用:0次
8 . 我国河南、广西和贵州等省份高硫铝土矿储量较高,其主要成分为Al2O3、Fe2O3,还含有少量SiO2、FeS2。现以高硫铝土矿为原料生产Al2O3和Fe3O4的部分工艺流程如下所示。
(1)加入少量CaO的主要作用为_____________ 。
(2)配平“焙烧”过程中发生反应的化学方程式:______________ 。




(3)向“过滤”得到的滤液中通入过量CO2,含金属元素的阴离子发生反应的离子方程式为___________________________ 。
(4)“隔绝空气焙烧”过程生成Fe3O4和SO2,发生反应的化学方程式为____________ 。
(5)“烧渣分离”若采取物理方法可以使用___________ (填物质名称)分离。
(6)纯度检验:将少量产品溶于稀硫酸中,再滴入酸性KMnO4溶液,若酸性KMnO4溶液褪色,___________ (填“能”或“不能”)说明产品中含有FeO,理由是________________________________________ 。
(7)“焙烧”的过程中采用多层逆流焙烧,优点是_____________ (任答一点)。

(1)加入少量CaO的主要作用为
(2)配平“焙烧”过程中发生反应的化学方程式:




(3)向“过滤”得到的滤液中通入过量CO2,含金属元素的阴离子发生反应的离子方程式为
(4)“隔绝空气焙烧”过程生成Fe3O4和SO2,发生反应的化学方程式为
(5)“烧渣分离”若采取物理方法可以使用
(6)纯度检验:将少量产品溶于稀硫酸中,再滴入酸性KMnO4溶液,若酸性KMnO4溶液褪色,
(7)“焙烧”的过程中采用多层逆流焙烧,优点是
您最近一年使用:0次
9 . 硫的含氯化合物有多种。
(1)亚硫酰氯(SOCl2)是一种重要的化工原料,遇水剧烈反应生成两种酸性物质,相关反应的化学方程式为___________ ;SOCl2中硫原子的杂化方式为___________ 。亚硫酰氯(SOCl2)在140℃以上时易分解,分解产物为S2Cl2、一种无色刺激性气味气体A和单质气体B,写出反应的化学方程式:___________ 。
(2)二氯化二硫(S2Cl2)可作硫化剂、氯化剂,常温下是一种黄红色液体,沸点为137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得。选用以下装置制取少量S2C12(加热及夹持装置略):
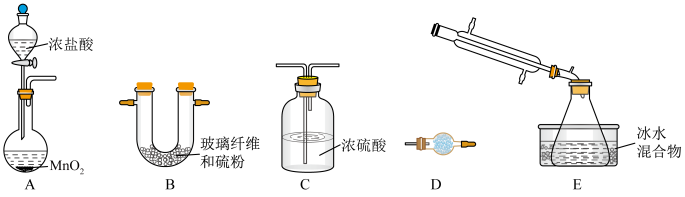
①A中发生反应的化学方程式为___________ 。
②B中玻璃纤维的作用是___________ 。
③D装置的作用为___________ 。
(3)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。

①W溶液可以是下列溶液中的___________ (填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为___________ (用含V、m的代数式表示)。
(1)亚硫酰氯(SOCl2)是一种重要的化工原料,遇水剧烈反应生成两种酸性物质,相关反应的化学方程式为
(2)二氯化二硫(S2Cl2)可作硫化剂、氯化剂,常温下是一种黄红色液体,沸点为137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得。选用以下装置制取少量S2C12(加热及夹持装置略):

①A中发生反应的化学方程式为
②B中玻璃纤维的作用是
③D装置的作用为
(3)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。

①W溶液可以是下列溶液中的
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
解题方法
10 . 离子反应能够体现出物质间反应的实质。下列反应的离子方程式书写正确的是
A.硫酸亚铁溶液滴入酸性高锰酸钾溶液中: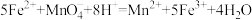 |
B.足量NH3通入氯化铝溶液中: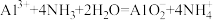 |
C.向Na2S2O3溶液中加入稀硫酸: |
D.向含有1 mol NH4Al(SO4)2的溶液中加入2 mol Ba(OH)2: |
您最近一年使用:0次



