1 . 五氯化锑(SbCl5)主要用作氟化工的催化剂、纺织工业织物的阻燃剂、染料工业的中间体。实验室根据反应 ,利用如下装置制备SbCl5 (加热及夹持装置略)。
,利用如下装置制备SbCl5 (加热及夹持装置略)。
实验室制备SbCl5的步骤如下:
ⅰ.保持80℃的条件,在盛有SbCl3的三颈烧瓶中通入Cl2,反应生成SbCl5;
ⅱ.将三颈烧瓶中的反应混合物转移到双颈烧瓶中;
ⅲ.减压蒸馏,收集目标物质。
回答下列问题:
(1)写出用K2MnO4和浓盐酸制备Cl2的离子方程式___________ ,其中体现还原性和酸性的HCl的物质的量之比为___________ 。
(2)实验装置中,两个冷凝管___________ (填“能”或“不能”)交换使用,步骤ⅰ中对三颈烧瓶进行加热的最佳方式是___________ 加热。
(3)写出图示实验装置存在的一处弊端:___________ 。
(4)步骤ⅱ将反应后混合液转移至双颈烧瓶中的方法:在b处连接减压装置,使三颈烧瓶中的液体流入双颈烧瓶。进行该操作前,需___________ (填活塞1和2的开、关的情况)。
(5)步骤ⅲ采用减压蒸馏,而不是常压蒸馏的原因是___________ ;调节减压装置至1.86kPa,收集___________ ℃左右的馏分。减压蒸馏时,玻璃毛细管的作用有___________ (填字母)。
a.防止暴沸 b.搅拌 c.连通大气,保持常压
 ,利用如下装置制备SbCl5 (加热及夹持装置略)。
,利用如下装置制备SbCl5 (加热及夹持装置略)。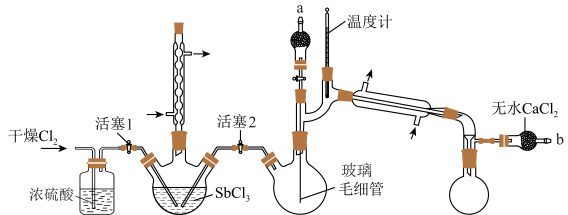
| 物质 | 熔点/℃ | 沸点/℃ | 性质 |
| SbCl3 | 73.4 | 223(101.3kPa) | 均极易水解 |
| SbCl5 | 2.8 | 176(101.3kPa,140℃)时分解 | |
| 68(1.86kPa)、79(2.90kPa) |
ⅰ.保持80℃的条件,在盛有SbCl3的三颈烧瓶中通入Cl2,反应生成SbCl5;
ⅱ.将三颈烧瓶中的反应混合物转移到双颈烧瓶中;
ⅲ.减压蒸馏,收集目标物质。
回答下列问题:
(1)写出用K2MnO4和浓盐酸制备Cl2的离子方程式
(2)实验装置中,两个冷凝管
(3)写出图示实验装置存在的一处弊端:
(4)步骤ⅱ将反应后混合液转移至双颈烧瓶中的方法:在b处连接减压装置,使三颈烧瓶中的液体流入双颈烧瓶。进行该操作前,需
(5)步骤ⅲ采用减压蒸馏,而不是常压蒸馏的原因是
a.防止暴沸 b.搅拌 c.连通大气,保持常压
您最近一年使用:0次
解题方法
2 . 广泛用于火箭、原子能、电子工业等领域。以矿石(主要成分是Be2SiO4,含少量MnO等)为原料制备Be的工艺流程如图所示。
(1)“烧结”之前,将铍矿石粉碎成粉末,其目的是_____ 。
(2)“除锰”时发生反应的离子方程式为_____ 。“除锰”时温度不宜过高,原因是_____ 。
(3)制备无水 过程如下:将
过程如下:将 溶于盐酸,蒸发浓缩、冷却结晶得到
溶于盐酸,蒸发浓缩、冷却结晶得到 ;加热
;加热 和
和 的混合物得到无水
的混合物得到无水 ,该化学方程式为
,该化学方程式为_____ 。也可以用 固体替代
固体替代 ,
, 的作用是
的作用是_____ 。
(4)1828年德国化学家维勒用金属钾还原熔融的氯化铍而得到 。若将这个反应设计成原电池,则在电池的
。若将这个反应设计成原电池,则在电池的_____ (填“正”或“负”)极得到Be。
(5)铍和铝的化学性质相似,下列叙述错误的是_____ (填字母)。
A.铍是一种轻金属,能与冷水反应
B.常温下,BeCl2溶液的pH<7
C.氧化铍的熔点高、耐酸碱腐蚀

(1)“烧结”之前,将铍矿石粉碎成粉末,其目的是
(2)“除锰”时发生反应的离子方程式为
(3)制备无水
 过程如下:将
过程如下:将 溶于盐酸,蒸发浓缩、冷却结晶得到
溶于盐酸,蒸发浓缩、冷却结晶得到 ;加热
;加热 和
和 的混合物得到无水
的混合物得到无水 ,该化学方程式为
,该化学方程式为 固体替代
固体替代 ,
, 的作用是
的作用是(4)1828年德国化学家维勒用金属钾还原熔融的氯化铍而得到
 。若将这个反应设计成原电池,则在电池的
。若将这个反应设计成原电池,则在电池的(5)铍和铝的化学性质相似,下列叙述错误的是
A.铍是一种轻金属,能与冷水反应
B.常温下,BeCl2溶液的pH<7
C.氧化铍的熔点高、耐酸碱腐蚀
您最近一年使用:0次
解题方法
3 .  (
(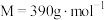 )是一种白色固体,微溶于水,不溶于醇,溶于高氯酸,可用作防臭剂、药物和食品添加剂。实验室采用如下方法制备
)是一种白色固体,微溶于水,不溶于醇,溶于高氯酸,可用作防臭剂、药物和食品添加剂。实验室采用如下方法制备
 并测定其纯度:
并测定其纯度:
Ⅰ.制备
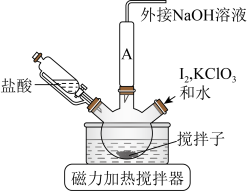
ⅰ.如图连接装置,向三颈烧瓶中依次加入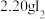 、
、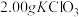 和
和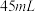 水,然后控制均匀速度滴加少量浓度为
水,然后控制均匀速度滴加少量浓度为 的盐酸,加热搅拌至反应完全,反应过程中有黄绿色气体产生,同时生成
的盐酸,加热搅拌至反应完全,反应过程中有黄绿色气体产生,同时生成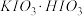 。
。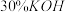 溶液,然后逐滴加入
溶液,然后逐滴加入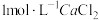 溶液,不断搅拌,生成
溶液,不断搅拌,生成 沉淀;
沉淀;
ⅲ.将混合物冷却后抽滤、依次水洗、醇洗,晾干后得产品;
Ⅱ.测定 产品纯度
产品纯度
ⅳ.称取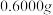 产品于烧杯中,加入
产品于烧杯中,加入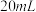 一定浓度
一定浓度 溶液(高氯酸不参与反应),将所得溶液冷却后转移至
溶液(高氯酸不参与反应),将所得溶液冷却后转移至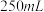 容量瓶中,定容;
容量瓶中,定容;
ⅴ.移取 溶液,加入
溶液,加入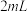 一定浓度
一定浓度 溶液和
溶液和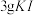 (过量),加
(过量),加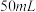 水,用
水,用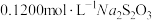 标准液(发生反应:
标准液(发生反应: )滴定至浅黄色,滴加指示剂,继续滴定至终点,重复测定2次,平均消耗标准液体积
)滴定至浅黄色,滴加指示剂,继续滴定至终点,重复测定2次,平均消耗标准液体积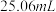 ;
;
ⅵ.做空白实验,平均消耗标准液体积 。
。
回答下列问题:
(1)装置中A处应安装的仪器为________ (填名称);三颈烧瓶的容积最适合的是________ (填选项字母);
A.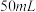 B.
B.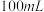 C.
C.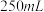 D.
D.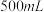
(2)滴加盐酸的仪器选用了恒压滴液漏斗,与分液漏斗相比该仪器的优点为________ ;
(3)步骤ⅰ中,生成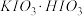 的化学方程式为
的化学方程式为________________ ;
(4)步骤ⅱ中,能够生成 的原因为
的原因为________________ ;
(5)步骤ⅲ中,醇洗的目的是________________ ;
(6)步骤ⅴ中,滴加的指示剂为________ ;滴定终点溶液颜色变化为________ ;
(7) 产品纯度为
产品纯度为________ %(保留两位有效数字)。
 (
(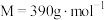 )是一种白色固体,微溶于水,不溶于醇,溶于高氯酸,可用作防臭剂、药物和食品添加剂。实验室采用如下方法制备
)是一种白色固体,微溶于水,不溶于醇,溶于高氯酸,可用作防臭剂、药物和食品添加剂。实验室采用如下方法制备 并测定其纯度:
并测定其纯度:Ⅰ.制备

ⅰ.如图连接装置,向三颈烧瓶中依次加入
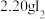 、
、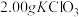 和
和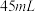 水,然后控制均匀速度滴加少量浓度为
水,然后控制均匀速度滴加少量浓度为 的盐酸,加热搅拌至反应完全,反应过程中有黄绿色气体产生,同时生成
的盐酸,加热搅拌至反应完全,反应过程中有黄绿色气体产生,同时生成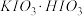 。
。
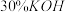 溶液,然后逐滴加入
溶液,然后逐滴加入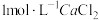 溶液,不断搅拌,生成
溶液,不断搅拌,生成 沉淀;
沉淀;ⅲ.将混合物冷却后抽滤、依次水洗、醇洗,晾干后得产品;
Ⅱ.测定
 产品纯度
产品纯度ⅳ.称取
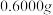 产品于烧杯中,加入
产品于烧杯中,加入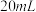 一定浓度
一定浓度 溶液(高氯酸不参与反应),将所得溶液冷却后转移至
溶液(高氯酸不参与反应),将所得溶液冷却后转移至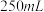 容量瓶中,定容;
容量瓶中,定容;ⅴ.移取
 溶液,加入
溶液,加入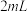 一定浓度
一定浓度 溶液和
溶液和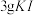 (过量),加
(过量),加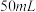 水,用
水,用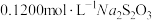 标准液(发生反应:
标准液(发生反应: )滴定至浅黄色,滴加指示剂,继续滴定至终点,重复测定2次,平均消耗标准液体积
)滴定至浅黄色,滴加指示剂,继续滴定至终点,重复测定2次,平均消耗标准液体积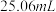 ;
;ⅵ.做空白实验,平均消耗标准液体积
 。
。回答下列问题:
(1)装置中A处应安装的仪器为
A.
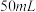 B.
B.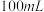 C.
C.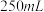 D.
D.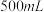
(2)滴加盐酸的仪器选用了恒压滴液漏斗,与分液漏斗相比该仪器的优点为
(3)步骤ⅰ中,生成
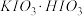 的化学方程式为
的化学方程式为(4)步骤ⅱ中,能够生成
 的原因为
的原因为(5)步骤ⅲ中,醇洗的目的是
(6)步骤ⅴ中,滴加的指示剂为
(7)
 产品纯度为
产品纯度为
您最近一年使用:0次
2024·陕西榆林·三模
名校
4 .  (三氯化六氨合钴,
(三氯化六氨合钴,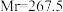 )是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备
)是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备 。
。
已知:①在 时,
时, 恰好完全沉淀为
恰好完全沉淀为 ;
;
②不同温度下 在水中的溶解度如图所示;
在水中的溶解度如图所示; 易潮解,Co(Ⅲ)的氧化性强于
易潮解,Co(Ⅲ)的氧化性强于 。
。
制备步骤如下:
Ⅰ. 的制备:用金属钴与氯气反应制备
的制备:用金属钴与氯气反应制备 ,实验中利用如图装置(连接处橡胶管省略)进行制备。
,实验中利用如图装置(连接处橡胶管省略)进行制备。 锥形瓶内加入
锥形瓶内加入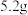 研细的
研细的 、
、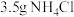 和
和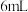 水,加热溶解后加入
水,加热溶解后加入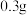 活性炭作催化剂。
活性炭作催化剂。
Ⅲ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下并缓慢加入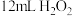 溶液。
溶液。
Ⅳ.在60℃下反应一段时间后,经过___________、过滤、洗涤、干燥等操作,得到橙黄色的 晶体
晶体 。
。
请回答下列问题:
(1)仪器a的名称为___________ 。
(2)用图中的装置组合制备 ,仪器的连接顺序为
,仪器的连接顺序为___________ 。装置B的作用是___________ 。
(3)制备三氯化六氨合钴的反应方程式为___________ 。
(4)在制备 时,加入浓氨水前,需在步骤Ⅱ中加入
时,加入浓氨水前,需在步骤Ⅱ中加入 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因___________ 。
(5)步骤Ⅲ中在加入 溶液时,控制温度在10℃以下缓慢加入的目的是
溶液时,控制温度在10℃以下缓慢加入的目的是___________ 。
(6)在步骤Ⅳ中过滤、洗涤、干燥之前的操作为___________ 、___________ 。
(7)制得 产品的产率为
产品的产率为___________ %(精确到0.1%)。
 (三氯化六氨合钴,
(三氯化六氨合钴,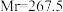 )是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备
)是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备 。
。已知:①在
 时,
时, 恰好完全沉淀为
恰好完全沉淀为 ;
;②不同温度下
 在水中的溶解度如图所示;
在水中的溶解度如图所示;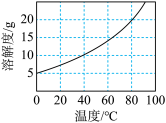
 易潮解,Co(Ⅲ)的氧化性强于
易潮解,Co(Ⅲ)的氧化性强于 。
。制备步骤如下:
Ⅰ.
 的制备:用金属钴与氯气反应制备
的制备:用金属钴与氯气反应制备 ,实验中利用如图装置(连接处橡胶管省略)进行制备。
,实验中利用如图装置(连接处橡胶管省略)进行制备。
 锥形瓶内加入
锥形瓶内加入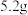 研细的
研细的 、
、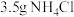 和
和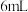 水,加热溶解后加入
水,加热溶解后加入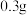 活性炭作催化剂。
活性炭作催化剂。Ⅲ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下并缓慢加入
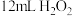 溶液。
溶液。Ⅳ.在60℃下反应一段时间后,经过___________、过滤、洗涤、干燥等操作,得到橙黄色的
 晶体
晶体 。
。请回答下列问题:
(1)仪器a的名称为
(2)用图中的装置组合制备
 ,仪器的连接顺序为
,仪器的连接顺序为(3)制备三氯化六氨合钴的反应方程式为
(4)在制备
 时,加入浓氨水前,需在步骤Ⅱ中加入
时,加入浓氨水前,需在步骤Ⅱ中加入 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因(5)步骤Ⅲ中在加入
 溶液时,控制温度在10℃以下缓慢加入的目的是
溶液时,控制温度在10℃以下缓慢加入的目的是(6)在步骤Ⅳ中过滤、洗涤、干燥之前的操作为
(7)制得
 产品的产率为
产品的产率为
您最近一年使用:0次
5 . 高铁酸钾( )是一种暗紫色固体,在低温和碱性环境中稳定存在,在中性或酸性溶液中易发生分解反应,释放出氧气,同时产生一种絮凝剂。高铁酸钾(
)是一种暗紫色固体,在低温和碱性环境中稳定存在,在中性或酸性溶液中易发生分解反应,释放出氧气,同时产生一种絮凝剂。高铁酸钾( )可用于自来水杀菌消毒和净化,一种由磁铁矿(主要成份为
)可用于自来水杀菌消毒和净化,一种由磁铁矿(主要成份为 ,还含有少量的MgO、
,还含有少量的MgO、 、
、 等)制备高铁酸钾的过程如下图所示:
等)制备高铁酸钾的过程如下图所示: )难溶于醇等有机溶剂。
)难溶于醇等有机溶剂。
②25℃部分难溶物的溶度积如下:
回答下列问题:
(1)酸溶后得到的滤渣的主要成分___________ 。
(2)加入 氧化过程主要发生的离子方程式
氧化过程主要发生的离子方程式___________ ,
 的用量远大于理论值,原因可能是
的用量远大于理论值,原因可能是___________ 。
(3)滤液1中含有的主要金属阳离子为___________ 。
(4)氧化过滤过程产生 ,写出该过程的离子方程式
,写出该过程的离子方程式___________ ,根据制备过程可知,该温度下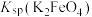
___________ 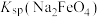 (填“<”或“>”)。
(填“<”或“>”)。
(5) 粗产品含有
粗产品含有 、KCl等杂质,用
、KCl等杂质,用___________ 方法进行分离提纯。其提纯步骤为:将一定量的 粗产品溶于冷的3 mol/L KOH溶液中过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置、过滤,洗涤2~3次,在真空干燥箱中干燥。洗涤过程中可以选用
粗产品溶于冷的3 mol/L KOH溶液中过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置、过滤,洗涤2~3次,在真空干燥箱中干燥。洗涤过程中可以选用___________ (填字母)。
a.蒸馏水 b.乙醇 c.氢氧化钠溶液
(6)产品纯度测定,可采用亚铬酸盐滴定法,滴定时有关反应的离子方程式为:
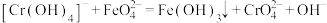


现称取a g高铁酸钾( )(摩尔质量为M g/mol)样品溶于过量的碱性亚铬酸盐
)(摩尔质量为M g/mol)样品溶于过量的碱性亚铬酸盐 溶液中,充分反应后过滤,滤液在250 mL容量瓶中定容,每次取25.00 mL于锥形瓶中加入稀硫酸酸化,滴入二苯胺磺酸钠做指示剂,用c mol/L
溶液中,充分反应后过滤,滤液在250 mL容量瓶中定容,每次取25.00 mL于锥形瓶中加入稀硫酸酸化,滴入二苯胺磺酸钠做指示剂,用c mol/L 标准溶液滴定至终点,消耗标准溶液V mL。该产品中高铁酸钾(
标准溶液滴定至终点,消耗标准溶液V mL。该产品中高铁酸钾( )的纯度为
)的纯度为___________ %。
 )是一种暗紫色固体,在低温和碱性环境中稳定存在,在中性或酸性溶液中易发生分解反应,释放出氧气,同时产生一种絮凝剂。高铁酸钾(
)是一种暗紫色固体,在低温和碱性环境中稳定存在,在中性或酸性溶液中易发生分解反应,释放出氧气,同时产生一种絮凝剂。高铁酸钾( )可用于自来水杀菌消毒和净化,一种由磁铁矿(主要成份为
)可用于自来水杀菌消毒和净化,一种由磁铁矿(主要成份为 ,还含有少量的MgO、
,还含有少量的MgO、 、
、 等)制备高铁酸钾的过程如下图所示:
等)制备高铁酸钾的过程如下图所示: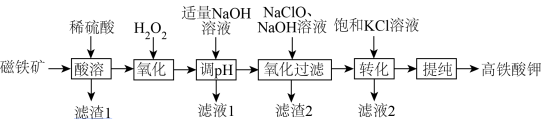
 )难溶于醇等有机溶剂。
)难溶于醇等有机溶剂。②25℃部分难溶物的溶度积如下:
 |  |  |  |
 |  |  |  |
(1)酸溶后得到的滤渣的主要成分
(2)加入
 氧化过程主要发生的离子方程式
氧化过程主要发生的离子方程式 的用量远大于理论值,原因可能是
的用量远大于理论值,原因可能是(3)滤液1中含有的主要金属阳离子为
(4)氧化过滤过程产生
 ,写出该过程的离子方程式
,写出该过程的离子方程式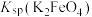
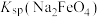 (填“<”或“>”)。
(填“<”或“>”)。(5)
 粗产品含有
粗产品含有 、KCl等杂质,用
、KCl等杂质,用 粗产品溶于冷的3 mol/L KOH溶液中过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置、过滤,洗涤2~3次,在真空干燥箱中干燥。洗涤过程中可以选用
粗产品溶于冷的3 mol/L KOH溶液中过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置、过滤,洗涤2~3次,在真空干燥箱中干燥。洗涤过程中可以选用a.蒸馏水 b.乙醇 c.氢氧化钠溶液
(6)产品纯度测定,可采用亚铬酸盐滴定法,滴定时有关反应的离子方程式为:
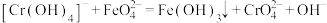


现称取a g高铁酸钾(
 )(摩尔质量为M g/mol)样品溶于过量的碱性亚铬酸盐
)(摩尔质量为M g/mol)样品溶于过量的碱性亚铬酸盐 溶液中,充分反应后过滤,滤液在250 mL容量瓶中定容,每次取25.00 mL于锥形瓶中加入稀硫酸酸化,滴入二苯胺磺酸钠做指示剂,用c mol/L
溶液中,充分反应后过滤,滤液在250 mL容量瓶中定容,每次取25.00 mL于锥形瓶中加入稀硫酸酸化,滴入二苯胺磺酸钠做指示剂,用c mol/L 标准溶液滴定至终点,消耗标准溶液V mL。该产品中高铁酸钾(
标准溶液滴定至终点,消耗标准溶液V mL。该产品中高铁酸钾( )的纯度为
)的纯度为
您最近一年使用:0次
名校
6 . 某工业废催化剂主要成份为: 和
和 ,还有少量的
,还有少量的 和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示:
和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示:_______ (填化学式)。
(2)水浸渣的主要成份是_______ (填化学式)。
(3)“沉淀”的化学式_______ 。生成该沉淀的化学方程式_______ 。
(4)“沉钒”中需要加入过量的浓 ,结合离子方程式说明原因是
,结合离子方程式说明原因是_______ 。写出生成 的化学方程式
的化学方程式_______ 。
(5)淀粉水解液中_______ (填化学式)起还原作用,用焦亚硫酸钠( )溶液代替淀粉水解液效果相同,写出反应的离子方程式
)溶液代替淀粉水解液效果相同,写出反应的离子方程式_______ 。
(6)利用生物燃料电池原理研究室温下氨的合成,电池工作时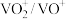 在电极与酶之间传递电子,示意图如图所示。
在电极与酶之间传递电子,示意图如图所示。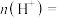
_______ mol。
 和
和 ,还有少量的
,还有少量的 和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示:
和FeO,利用该废催化剂回收Cr和V的简化工业流程如下图所示: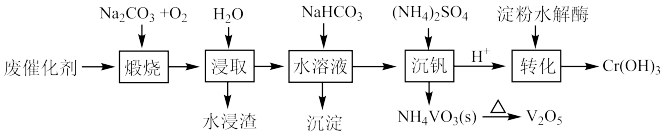
(2)水浸渣的主要成份是
(3)“沉淀”的化学式
(4)“沉钒”中需要加入过量的浓
 ,结合离子方程式说明原因是
,结合离子方程式说明原因是 的化学方程式
的化学方程式(5)淀粉水解液中
 )溶液代替淀粉水解液效果相同,写出反应的离子方程式
)溶液代替淀粉水解液效果相同,写出反应的离子方程式(6)利用生物燃料电池原理研究室温下氨的合成,电池工作时
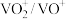 在电极与酶之间传递电子,示意图如图所示。
在电极与酶之间传递电子,示意图如图所示。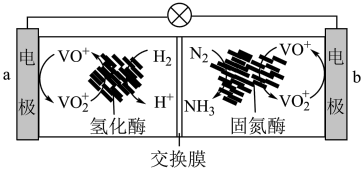
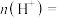
您最近一年使用:0次
7 . 亚氯酸钠是一种高效漂白剂和氧化剂,常用于纸浆和纤维的漂白、饮水净化和污水处理等。温度高于60℃时, 会分解成
会分解成 和NaCl。某化学实验探究小组设计如图实验制备亚氯酸钠(
和NaCl。某化学实验探究小组设计如图实验制备亚氯酸钠( )晶体。
)晶体。
①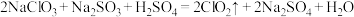 。
。
② 极易溶于水而不与水反应,几乎不发生水解,沸点11℃。
极易溶于水而不与水反应,几乎不发生水解,沸点11℃。
③ 饱和溶液在低于38℃时析出
饱和溶液在低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 。
。
(1)C装置仪器名称是___________ ,它的作用是___________ 。
(2)B中使用浓硫酸而不用稀硫酸的原因是___________ 。
(3)向B中加入浓硫酸的操作方法是___________ 。
(4) 气体与装置D中混合溶液反应生成
气体与装置D中混合溶液反应生成 ,生成
,生成 的离子方程式为
的离子方程式为___________ 。
(5)反应后,经___________ 等步骤可从装置D的溶液获得 晶体。干燥时通常要求低温晾干,温度过高可能导致产品中混有的杂质是
晶体。干燥时通常要求低温晾干,温度过高可能导致产品中混有的杂质是___________ 。
(6)测定样品中 的纯度(假设杂质不参与反应)。测定时进行如下实验:准确称取0.200 g的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应:
的纯度(假设杂质不参与反应)。测定时进行如下实验:准确称取0.200 g的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应: ,将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液做指示剂,用0.1 mol⋅L
,将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液做指示剂,用0.1 mol⋅L
 标准液滴定至终点,测得消耗标准溶液体积的平均值为20.00 mL(已知:
标准液滴定至终点,测得消耗标准溶液体积的平均值为20.00 mL(已知: )。
)。
所称取的样品中 的质量分数为
的质量分数为___________ 。
 会分解成
会分解成 和NaCl。某化学实验探究小组设计如图实验制备亚氯酸钠(
和NaCl。某化学实验探究小组设计如图实验制备亚氯酸钠( )晶体。
)晶体。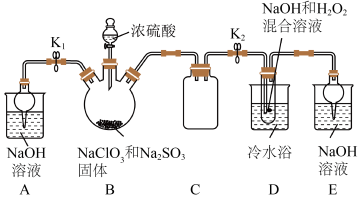
①
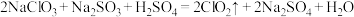 。
。②
 极易溶于水而不与水反应,几乎不发生水解,沸点11℃。
极易溶于水而不与水反应,几乎不发生水解,沸点11℃。③
 饱和溶液在低于38℃时析出
饱和溶液在低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 。
。(1)C装置仪器名称是
(2)B中使用浓硫酸而不用稀硫酸的原因是
(3)向B中加入浓硫酸的操作方法是
(4)
 气体与装置D中混合溶液反应生成
气体与装置D中混合溶液反应生成 ,生成
,生成 的离子方程式为
的离子方程式为(5)反应后,经
 晶体。干燥时通常要求低温晾干,温度过高可能导致产品中混有的杂质是
晶体。干燥时通常要求低温晾干,温度过高可能导致产品中混有的杂质是(6)测定样品中
 的纯度(假设杂质不参与反应)。测定时进行如下实验:准确称取0.200 g的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应:
的纯度(假设杂质不参与反应)。测定时进行如下实验:准确称取0.200 g的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应: ,将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液做指示剂,用0.1 mol⋅L
,将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液做指示剂,用0.1 mol⋅L
 标准液滴定至终点,测得消耗标准溶液体积的平均值为20.00 mL(已知:
标准液滴定至终点,测得消耗标准溶液体积的平均值为20.00 mL(已知: )。
)。所称取的样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
解题方法
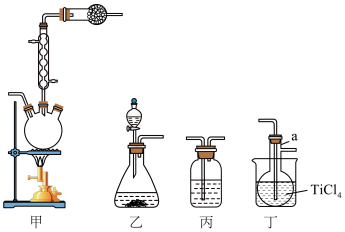
8 . 钛在医疗领域的应用非常广泛,如:制人造关节、主动心瓣等。实验室利用含杂质的二氧化钛做原料制取高纯度的二氧化钛,装置如图(夹持装置已略去)。
已知:① ;
;
② 为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应,能溶于有机溶剂,易挥发,与HCl不发生反应;
为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应,能溶于有机溶剂,易挥发,与HCl不发生反应;
③ 的盐酸溶液可吸收CO而生成黑色颗粒Pd;
的盐酸溶液可吸收CO而生成黑色颗粒Pd;
④ 在盐酸溶液中的存在形式为
在盐酸溶液中的存在形式为 。
。
a.制备
_______ (填序号)。
①先给陶瓷管通电加热,一段时间后,再打开分液漏斗活塞
②先打开分液漏斗活塞,一段时间后,再给陶瓷管通电加热
③先将陶瓷管断电停止加热,一段时间后,再关闭分液漏斗活塞
④先关闭分液漏斗活塞,一段时间后,再将陶瓷管断电停止加热
(2)装置B中盛放的试剂是_______ (填名称)。
(3)该实验设计存在的缺陷是_______ 、_______
(4)用 的盐酸溶液吸收CO的离子方程式为
的盐酸溶液吸收CO的离子方程式为_______ 。
(5)所得的 可用Mg制Ti,该过程可在
可用Mg制Ti,该过程可在_______ (填序号)氛围保护下进行。
①氮气 ②氩气 ③水蒸气 ④氧气
b. 气相氧化法制备
气相氧化法制备
_______ 。
(7)实验装置按从左到右的连接顺序为_______ 。
(8)写出装置甲三颈烧瓶内发生反应的化学方程式_______ 。
已知:①
 ;
;②
 为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应,能溶于有机溶剂,易挥发,与HCl不发生反应;
为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应,能溶于有机溶剂,易挥发,与HCl不发生反应;③
 的盐酸溶液可吸收CO而生成黑色颗粒Pd;
的盐酸溶液可吸收CO而生成黑色颗粒Pd;④
 在盐酸溶液中的存在形式为
在盐酸溶液中的存在形式为 。
。a.制备

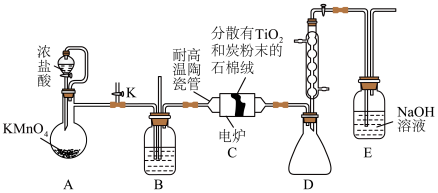
①先给陶瓷管通电加热,一段时间后,再打开分液漏斗活塞
②先打开分液漏斗活塞,一段时间后,再给陶瓷管通电加热
③先将陶瓷管断电停止加热,一段时间后,再关闭分液漏斗活塞
④先关闭分液漏斗活塞,一段时间后,再将陶瓷管断电停止加热
(2)装置B中盛放的试剂是
(3)该实验设计存在的缺陷是
(4)用
 的盐酸溶液吸收CO的离子方程式为
的盐酸溶液吸收CO的离子方程式为(5)所得的
 可用Mg制Ti,该过程可在
可用Mg制Ti,该过程可在①氮气 ②氩气 ③水蒸气 ④氧气
b.
 气相氧化法制备
气相氧化法制备
(7)实验装置按从左到右的连接顺序为
(8)写出装置甲三颈烧瓶内发生反应的化学方程式
您最近一年使用:0次
9 .  (钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1%
(钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1% 、19.5%Fe和3.4%
、19.5%Fe和3.4% )为原料制备钒酸铋,并回收
)为原料制备钒酸铋,并回收 制备食品抗氧化剂
制备食品抗氧化剂 的流程如下:
的流程如下: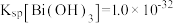 ,
,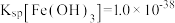 ;当金属离子浓度
;当金属离子浓度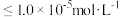 时,认为该离子已沉淀完全。请回答下列问题:
时,认为该离子已沉淀完全。请回答下列问题:
(1)“焙烧”中采用高压空气的目的是_______ , 转化成
转化成 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(2)浸渣的主要成分是_______ (填化学式)。
(3)“酸浸”得到的浸液中 ,则“除铁”调节pH的范围为
,则“除铁”调节pH的范围为_______ 。
(4)“合成”过程中将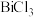 溶液和
溶液和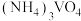 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为_______ (答一条)。
(5)向饱和碳酸钠溶液中通入过量 可制得
可制得 ,发生反应的化学方程式为
,发生反应的化学方程式为_______ 。 易变质生成
易变质生成 ,设计简单实验证明产品是否变质:
,设计简单实验证明产品是否变质:_______ 。(已知: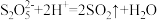 )
)
(6)某工厂用20吨该辉铋矿,最终得到18.468吨 ,则该过程中Bi的损耗率为
,则该过程中Bi的损耗率为______ %。
 (钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1%
(钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1% 、19.5%Fe和3.4%
、19.5%Fe和3.4% )为原料制备钒酸铋,并回收
)为原料制备钒酸铋,并回收 制备食品抗氧化剂
制备食品抗氧化剂 的流程如下:
的流程如下:
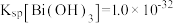 ,
,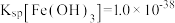 ;当金属离子浓度
;当金属离子浓度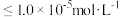 时,认为该离子已沉淀完全。请回答下列问题:
时,认为该离子已沉淀完全。请回答下列问题:(1)“焙烧”中采用高压空气的目的是
 转化成
转化成 发生反应的化学方程式为
发生反应的化学方程式为(2)浸渣的主要成分是
(3)“酸浸”得到的浸液中
 ,则“除铁”调节pH的范围为
,则“除铁”调节pH的范围为(4)“合成”过程中将
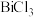 溶液和
溶液和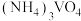 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为(5)向饱和碳酸钠溶液中通入过量
 可制得
可制得 ,发生反应的化学方程式为
,发生反应的化学方程式为 易变质生成
易变质生成 ,设计简单实验证明产品是否变质:
,设计简单实验证明产品是否变质: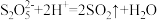 )
)(6)某工厂用20吨该辉铋矿,最终得到18.468吨
 ,则该过程中Bi的损耗率为
,则该过程中Bi的损耗率为
您最近一年使用:0次
10 . 二氧化钒( )是一种新型热敏材料,+4价的钒化合物在弱酸性条件下易被氧化,实验室以
)是一种新型热敏材料,+4价的钒化合物在弱酸性条件下易被氧化,实验室以 为原料合成用于制备
为原料合成用于制备 的氧钒(
的氧钒( )碱式碳酸铵晶体。过程如下:
)碱式碳酸铵晶体。过程如下:
(1)步骤i中生成 的同时还产生一种无色无污染的气体,所发生反应的化学方程式为
的同时还产生一种无色无污染的气体,所发生反应的化学方程式为___________ 。只用浓盐酸与 反应也能制备
反应也能制备 溶液,从安全与环保角度分析,该反应不被推广的主要原因是
溶液,从安全与环保角度分析,该反应不被推广的主要原因是___________ 。
(2)步骤ii可用如图仪器组装完成。___________ (用各接口字母表示)。
②B装置的作用是___________ 。
③反应结束后,将三颈烧瓶置于干燥器中一段时间,可得到紫红色晶体,然后抽滤洗涤,先用饱和 溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和
溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和 溶液洗涤除去的阴离子主要是
溶液洗涤除去的阴离子主要是___________ ,用无水乙醇洗涤的目的是___________ 。
(3)测定氧钒( )碱式碳酸铵晶体粗产品中钒的含量。
)碱式碳酸铵晶体粗产品中钒的含量。
称量a g样品于锥形瓶中,用20mL蒸馏水与30mL混酸溶解后,加0.02mol/L 溶液至稍过量,充分反应后继续加1%
溶液至稍过量,充分反应后继续加1%  溶液至稍过量。再用尿素除去过量的
溶液至稍过量。再用尿素除去过量的 ,滴入几滴铁氰化钾{
,滴入几滴铁氰化钾{ }溶液,最后用c mol/L
}溶液,最后用c mol/L  标准溶液滴定至终点,消耗体积为b mL。滴定反应为:
标准溶液滴定至终点,消耗体积为b mL。滴定反应为: 。
。
① 溶液的作用是
溶液的作用是___________ 。
②粗产品中钒的质量分数的表达式为___________ 。
 )是一种新型热敏材料,+4价的钒化合物在弱酸性条件下易被氧化,实验室以
)是一种新型热敏材料,+4价的钒化合物在弱酸性条件下易被氧化,实验室以 为原料合成用于制备
为原料合成用于制备 的氧钒(
的氧钒( )碱式碳酸铵晶体。过程如下:
)碱式碳酸铵晶体。过程如下:
(1)步骤i中生成
 的同时还产生一种无色无污染的气体,所发生反应的化学方程式为
的同时还产生一种无色无污染的气体,所发生反应的化学方程式为 反应也能制备
反应也能制备 溶液,从安全与环保角度分析,该反应不被推广的主要原因是
溶液,从安全与环保角度分析,该反应不被推广的主要原因是(2)步骤ii可用如图仪器组装完成。
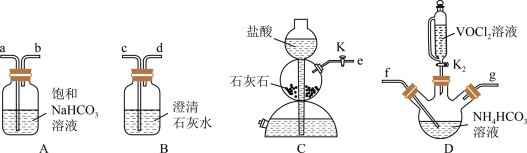
②B装置的作用是
③反应结束后,将三颈烧瓶置于干燥器中一段时间,可得到紫红色晶体,然后抽滤洗涤,先用饱和
 溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和
溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和 溶液洗涤除去的阴离子主要是
溶液洗涤除去的阴离子主要是(3)测定氧钒(
 )碱式碳酸铵晶体粗产品中钒的含量。
)碱式碳酸铵晶体粗产品中钒的含量。称量a g样品于锥形瓶中,用20mL蒸馏水与30mL混酸溶解后,加0.02mol/L
 溶液至稍过量,充分反应后继续加1%
溶液至稍过量,充分反应后继续加1%  溶液至稍过量。再用尿素除去过量的
溶液至稍过量。再用尿素除去过量的 ,滴入几滴铁氰化钾{
,滴入几滴铁氰化钾{ }溶液,最后用c mol/L
}溶液,最后用c mol/L  标准溶液滴定至终点,消耗体积为b mL。滴定反应为:
标准溶液滴定至终点,消耗体积为b mL。滴定反应为: 。
。①
 溶液的作用是
溶液的作用是②粗产品中钒的质量分数的表达式为
您最近一年使用:0次



