名校
解题方法
1 . 工业上用铝土矿(主要成份是 ,还含有
,还含有 、
、 )提取氧化铝做冶炼铝的原料(纯净的
)提取氧化铝做冶炼铝的原料(纯净的 ),某研究性学习小组设计了如图提取流程:
),某研究性学习小组设计了如图提取流程:
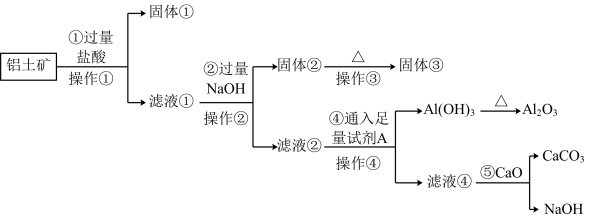
请回答下列问题:
(1)操作①的名称是_______ ,操作③用到的仪器有酒精灯、三脚架、泥三角、_______ 。
(2)写出加入过量 溶液发生反应的主要离子方程式:
溶液发生反应的主要离子方程式:________ 。
(3)流程中的 最好选用
最好选用________ ,发生反应的离子方程式为________ 。
(4)写出反应⑤的化学反应方程式______ ,上述流程中可以循环利用的物质为____ (填化学式)。
(5)有一种含铁、硅等元素的矿石,其主要成分的化学式为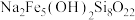 ,该物质中+2价铁与+3价铁的物质的量之比为
,该物质中+2价铁与+3价铁的物质的量之比为______ 。将 该矿石用足量
该矿石用足量______ (填盐酸或硫酸)溶解后,加入过量铜粉使溶液中的铁元素全部变为 ,过滤后滤液用
,过滤后滤液用 的
的 酸性溶液与
酸性溶液与 反应,用去
反应,用去 溶液。该矿石中铁元素的质量分数为
溶液。该矿石中铁元素的质量分数为_______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 ,还含有
,还含有 、
、 )提取氧化铝做冶炼铝的原料(纯净的
)提取氧化铝做冶炼铝的原料(纯净的 ),某研究性学习小组设计了如图提取流程:
),某研究性学习小组设计了如图提取流程:
请回答下列问题:
(1)操作①的名称是
(2)写出加入过量
 溶液发生反应的主要离子方程式:
溶液发生反应的主要离子方程式:(3)流程中的
 最好选用
最好选用(4)写出反应⑤的化学反应方程式
(5)有一种含铁、硅等元素的矿石,其主要成分的化学式为
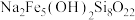 ,该物质中+2价铁与+3价铁的物质的量之比为
,该物质中+2价铁与+3价铁的物质的量之比为 该矿石用足量
该矿石用足量 ,过滤后滤液用
,过滤后滤液用 的
的 酸性溶液与
酸性溶液与 反应,用去
反应,用去 溶液。该矿石中铁元素的质量分数为
溶液。该矿石中铁元素的质量分数为 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-03-03更新
|
212次组卷
|
3卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期中测试化学试题
名校
解题方法
2 . 某小组利用如图所示装置制备并收集TiCl4(夹持装置略去),并测定由TiCl4制备的纳米xTiO2•yH2O的组成。
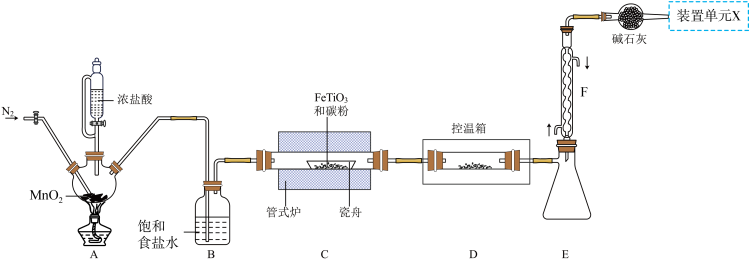
已知:
I. TiCl4高温时能与O2反应,极易水解,能溶于CCl4;
Ⅱ.瓷舟中主反应生成TiCl4、FeCl3(容易二聚成Fe2Cl6)和一种氧化物(有毒气体),还有少量副产物CCL4;
Ⅲ.相关物质的熔沸点如表:
(1)TiCl4摩尔质量大于FeCl3,但沸点却低于FeCl3的原因是_______ 。
(2)写出A中反应的化学方程式_______ ;上述装置存在一处缺陷,会导致TiCl4产率降低,改进的方法是_______ 。
(3)将管式炉加热至900℃时,瓷舟中主要反应的化学方程式为_______ 。
(4)装置E、F的作用为_______ 。
(5)设计实验测定纳米xTiO2•yH2O组成。
已知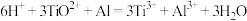 ,
,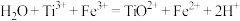
(可选试剂:水、稀硫酸、稀硝酸、氢氧化钠溶液、Al粉、0.1000 的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
①取样称重:称取4.675g样品。②酸溶:用足量稀硫酸溶解。
③还原:加入过量Al粉还原至Al粉不再溶解,过滤取滤液定容。定容为500mL,取20.00mL。
④滴定:用0.1000 的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
的NH4Fe(SO4)2标准溶液滴定,标准溶液装在_______ 滴定管(填“酸式”、“碱式”),用_______ 做指示剂,平均消耗标准溶液20.00mL,则xTiO2•yH2O的化学式为_______ 。

已知:
I. TiCl4高温时能与O2反应,极易水解,能溶于CCl4;
Ⅱ.瓷舟中主反应生成TiCl4、FeCl3(容易二聚成Fe2Cl6)和一种氧化物(有毒气体),还有少量副产物CCL4;
Ⅲ.相关物质的熔沸点如表:
TiCl4 | FeCl3 | CCl4 | |
熔点/℃ |
| 306 |
|
沸点/℃ | 136.4 | 315 | 76.8 |
(1)TiCl4摩尔质量大于FeCl3,但沸点却低于FeCl3的原因是
(2)写出A中反应的化学方程式
(3)将管式炉加热至900℃时,瓷舟中主要反应的化学方程式为
(4)装置E、F的作用为
(5)设计实验测定纳米xTiO2•yH2O组成。
已知
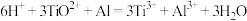 ,
,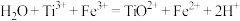
(可选试剂:水、稀硫酸、稀硝酸、氢氧化钠溶液、Al粉、0.1000
 的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)①取样称重:称取4.675g样品。②酸溶:用足量稀硫酸溶解。
③还原:加入过量Al粉还原至Al粉不再溶解,过滤取滤液定容。定容为500mL,取20.00mL。
④滴定:用0.1000
 的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
您最近一年使用:0次
2024-02-19更新
|
911次组卷
|
3卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题(已下线)2024届广东省华南师范大学附属中学 广雅中学 深圳中学 广东实验中学高三上学期四校联考化学试题广东省云浮市云安区云安中学2023-2024学年高三下学期3月考试化学试题
名校
3 .  是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究
是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究 的氧化能力与介质pH的关系(已知
的氧化能力与介质pH的关系(已知 溶液呈绿色,酸性条件下发生歧化反应生成
溶液呈绿色,酸性条件下发生歧化反应生成 和
和 )。
)。
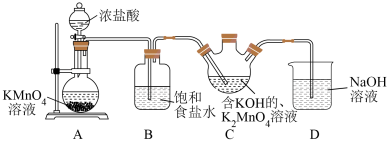
请回答下列问题:
(1)装置A中盛放 溶液的仪器名称为
溶液的仪器名称为___________ ,实验开始前应进行的操作为___________ ,装置D的作用为___________ 。
(2)装置A中浓盐酸在反应中表现出来的性质是___________ 。
(3)由实验推知,A中氧化性:
___________ (填“>”、“<”或“=”) ;若装置C中绿色溶液变为紫红色,
;若装置C中绿色溶液变为紫红色,___________ (填“能”或“不能”)根据此现象判断 的氧化性强于
的氧化性强于 。
。
(4)有关高锰酸钾的实验及现象如表所示。
①已知实验Ⅰ中氧化产物为 ,则实验Ⅰ中发生反应的离子方程式为
,则实验Ⅰ中发生反应的离子方程式为___________ 。
②实验结论:其他条件相同,介质pH越低, 氧化性越
氧化性越___________ (填“强”或“弱”)。
 是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究
是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究 的氧化能力与介质pH的关系(已知
的氧化能力与介质pH的关系(已知 溶液呈绿色,酸性条件下发生歧化反应生成
溶液呈绿色,酸性条件下发生歧化反应生成 和
和 )。
)。
请回答下列问题:
(1)装置A中盛放
 溶液的仪器名称为
溶液的仪器名称为(2)装置A中浓盐酸在反应中表现出来的性质是
(3)由实验推知,A中氧化性:

 ;若装置C中绿色溶液变为紫红色,
;若装置C中绿色溶液变为紫红色, 的氧化性强于
的氧化性强于 。
。(4)有关高锰酸钾的实验及现象如表所示。
| 实验 | 装置 | 试剂R(5 mL含0.1 mol·L  的溶液) 的溶液) | 现象(通入乙烯的体积相等) |
| Ⅰ | 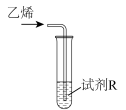 |  溶液 溶液 | 较快产生黑色沉淀 |
| Ⅱ | KOH和 溶液 溶液 | 紫红色溶液较慢变为绿色溶液 | |
| Ⅲ | 稀硫酸和 溶液 溶液 | 紫红色溶液很快变为无色溶液 |
 ,则实验Ⅰ中发生反应的离子方程式为
,则实验Ⅰ中发生反应的离子方程式为②实验结论:其他条件相同,介质pH越低,
 氧化性越
氧化性越
您最近一年使用:0次
2023-10-27更新
|
252次组卷
|
5卷引用:湖南省株洲市第一中学2021届高三第一次模拟检测化学试题
名校
解题方法
4 . 下列离子方程式书写正确的是
A.向四氧化三铁中加入稀盐酸: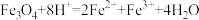 |
B.向 溶液中通入足量的 溶液中通入足量的 : : |
C.将Na放入硫酸铜溶液中: |
D. 溶于水: 溶于水: |
您最近一年使用:0次
2023-01-13更新
|
107次组卷
|
2卷引用:湖南省株洲市第二中学2021-2022学年高一上学期第三次月考化学试题
解题方法
5 .  是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和
是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和 。工业上用硫化碱法制备
。工业上用硫化碱法制备 的反应方程式为:
的反应方程式为: ,实验室用此法制备
,实验室用此法制备 的装置如图所示:
的装置如图所示:

请回答下列问题:
(1)仪器a的名称为_______ 。
(2) 的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开
的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开  ,关闭
,关闭 ,调节
,调节 使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开
使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开  ,关闭
,关闭 、
、 ,原因是
,原因是 _______ ;②将装置C中所得溶液经一系列操作,最后洗涤、干燥,得到 样品。洗涤时为尽可能避免产品损失应选用的试剂是
样品。洗涤时为尽可能避免产品损失应选用的试剂是 _______ 。
a.水 b.乙醇 c.氢氧化钠溶液 d.稀盐酸
制备 的上述装置的明显不足是
的上述装置的明显不足是 _______ 。
(3) 样品纯度的测定:称取
样品纯度的测定:称取 样品,配制成200mL溶液;在锥形瓶中加入
样品,配制成200mL溶液;在锥形瓶中加入

 溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配
溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配  溶液滴定,当
溶液滴定,当 _______ 时达到滴定终点,测得消耗 溶液的体积为
溶液的体积为  ,则样品中硫代硫酸钠的质量分数为
,则样品中硫代硫酸钠的质量分数为 _______  。
。 已知:
已知: 的相对分子质量为158 , 相关反应:
的相对分子质量为158 , 相关反应: ;
; 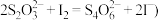
(4) 的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成
的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成 ,反应的离子方程式为
,反应的离子方程式为_______ 。
 是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和
是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和 。工业上用硫化碱法制备
。工业上用硫化碱法制备 的反应方程式为:
的反应方程式为: ,实验室用此法制备
,实验室用此法制备 的装置如图所示:
的装置如图所示:
请回答下列问题:
(1)仪器a的名称为
(2)
 的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开
的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开  ,关闭
,关闭 ,调节
,调节 使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开
使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开  ,关闭
,关闭 、
、 ,原因是
,原因是  样品。洗涤时为尽可能避免产品损失应选用的试剂是
样品。洗涤时为尽可能避免产品损失应选用的试剂是 a.水 b.乙醇 c.氢氧化钠溶液 d.稀盐酸
制备
 的上述装置的明显不足是
的上述装置的明显不足是 (3)
 样品纯度的测定:称取
样品纯度的测定:称取 样品,配制成200mL溶液;在锥形瓶中加入
样品,配制成200mL溶液;在锥形瓶中加入

 溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配
溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配  溶液滴定,当
溶液滴定,当  溶液的体积为
溶液的体积为  ,则样品中硫代硫酸钠的质量分数为
,则样品中硫代硫酸钠的质量分数为  。
。 已知:
已知: 的相对分子质量为158 , 相关反应:
的相对分子质量为158 , 相关反应: ;
; 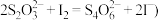
(4)
 的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成
的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
6 . 回答下列问题:
(1)已知Cl2能将 氧化成Br2,现将少量Cl2通入FeBr2的溶液中,反应的离子方程式为
氧化成Br2,现将少量Cl2通入FeBr2的溶液中,反应的离子方程式为
 ,这个事实说明具有还原性的离子还原性强弱为
,这个事实说明具有还原性的离子还原性强弱为________ 。
(2)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力。若误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有________ 性。
(3)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、 、
、 、
、 、
、 、H2O
、H2O
①写出并配平湿法制高铁酸钾的离子反应方程式:________ 。
②每生成 转移
转移_______ mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为______ mol。
(1)已知Cl2能将
 氧化成Br2,现将少量Cl2通入FeBr2的溶液中,反应的离子方程式为
氧化成Br2,现将少量Cl2通入FeBr2的溶液中,反应的离子方程式为
 ,这个事实说明具有还原性的离子还原性强弱为
,这个事实说明具有还原性的离子还原性强弱为(2)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力。若误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有
(3)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、
 、
、 、
、 、
、 、H2O
、H2O①写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成
 转移
转移
您最近一年使用:0次
名校
解题方法
7 . 高铁酸钾(K2FeO4)是优质水处理剂,实验室制取K2FeO4的装置如下图,回答下列问题:
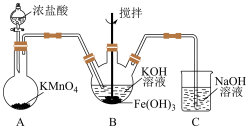
(1)A装置的作用是制取氯气,且反应后高锰酸钾转化为MnCl2。盛浓盐酸的仪器名称为_______ ;A中反应的离子方程式为:_______ ;做还原剂的HCl和表现酸性的HCl的物质的量之比为_______ 。
(2)B中K2FeO4的制备原理为:Cl2+ Fe(OH)3+_______→K2FeO4+KCl+_______。(未配平),请配平该化学方程式并用双线桥标明电子转移情况_______ 。当上述反应消耗标准状况下672mLCl2时,理论上生成K2FeO4质量为_______ 。
(3)装置C的作用是_______ 。
(4)K2FeO4处理水的原理之一是在水中生成Fe3+,Fe3+与水反应生成氢氧化铁胶体后,能吸附水中的悬浮物,该过程称为_______ 。实验室制备该胶体的离子方程式为_______ 。

(1)A装置的作用是制取氯气,且反应后高锰酸钾转化为MnCl2。盛浓盐酸的仪器名称为
(2)B中K2FeO4的制备原理为:Cl2+ Fe(OH)3+_______→K2FeO4+KCl+_______。(未配平),请配平该化学方程式并用双线桥标明电子转移情况
(3)装置C的作用是
(4)K2FeO4处理水的原理之一是在水中生成Fe3+,Fe3+与水反应生成氢氧化铁胶体后,能吸附水中的悬浮物,该过程称为
您最近一年使用:0次
2022-11-22更新
|
167次组卷
|
2卷引用:湖南省株洲市第二中学2021-2022学年高一上学期期中化学试题
名校
8 . I、高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾、次氯酸等还强。工业上制取高铁酸钠的化学方程式是(未配平):Fe(NO3)3+ NaOH + Cl2→ Na2FeO4+ NaNO3+ NaCl + H2O
(1)高铁酸钠中,铁元素的化合价是_______ ;上述制取铁酸钠的反应中,铁元素被_______ (填“还原”或“氧化”)。
(2)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂原因铁元素转化为Fe(OH)3胶体。用饱和氯化铁溶液制备Fe(OH)3胶体方法_______ 。
(3)电子工业常用30%的FeCl3溶液腐蚀覆在绝缘板上的铜箔,制造印刷电路板。
①少量的铜可以完全溶解在FeCl3溶液中,所发生反应的离子方程式为_______ 。
②除去FeCl3溶液中混有的FeCl2可加入或通入_______ 。
A、硝酸 B、稀硫酸 C、氯气 D、氢氧化钠
II、次磷酸(H3PO2)是一种精细磷化工产品,是一元中强酸,具有较强还原性。回答下列问题:
(4)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①利用H3PO2进行化学镀银反应中,氧化剂(Ag+)与还原剂(H3PO2)的物质的量之比为4∶1,则氧化产物为_______ (填化学式)。
②从分类来看,NaH2PO2属于_______ 。
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。配平白磷与Ba(OH)2溶液反应的化学方程式_______ 。
_______P4 +_______Ba(OH)2 + _______H2O —— _______Ba(H2PO2)2+_______PH3↑
(1)高铁酸钠中,铁元素的化合价是
(2)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂原因铁元素转化为Fe(OH)3胶体。用饱和氯化铁溶液制备Fe(OH)3胶体方法
(3)电子工业常用30%的FeCl3溶液腐蚀覆在绝缘板上的铜箔,制造印刷电路板。
①少量的铜可以完全溶解在FeCl3溶液中,所发生反应的离子方程式为
②除去FeCl3溶液中混有的FeCl2可加入或通入
A、硝酸 B、稀硫酸 C、氯气 D、氢氧化钠
II、次磷酸(H3PO2)是一种精细磷化工产品,是一元中强酸,具有较强还原性。回答下列问题:
(4)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①利用H3PO2进行化学镀银反应中,氧化剂(Ag+)与还原剂(H3PO2)的物质的量之比为4∶1,则氧化产物为
②从分类来看,NaH2PO2属于
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。配平白磷与Ba(OH)2溶液反应的化学方程式
_______P4 +_______Ba(OH)2 + _______H2O —— _______Ba(H2PO2)2+_______PH3↑
您最近一年使用:0次
2022-10-31更新
|
145次组卷
|
2卷引用:湖南省邵阳市第二中学2021-2022学年高一上学期第一次月考化学试题
名校
解题方法
9 . I.现有下列物质:①固体氢氧化钡,②石墨棒,③纯醋酸,④液态氯化氢,⑤硫酸氢钾固体,⑥熔融氯化钠,⑦酒精(C2H5OH),⑧碳酸钠粉末。请用序号回答下列问题:
(1)以上物质中能导电的是___________ ;
(2)以上物质中属于电解质的是___________ ;
(3)以上物质中属于非电解质的是___________ 。
II.高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止刻蚀液与下层(砷化镓)反应。
(4)已知:Ga和Al最外层电子数相同,As和N最外层电子数相同。在H2O2与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂个数之比为___________ 。
(5)配平下列方程式____
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
II.高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止刻蚀液与下层(砷化镓)反应。
(4)已知:Ga和Al最外层电子数相同,As和N最外层电子数相同。在H2O2与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂个数之比为
(5)配平下列方程式
Cu+ HNO3(稀)= Cu(NO3)2+ NO↑+ H2O
您最近一年使用:0次
10 . K3[Fe(C2O4)3]•3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。请回答下列问题:
(1)已知K3[Fe(C2O4)3]•3H2O中Fe为+3价,则C的化合价为____ 。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。
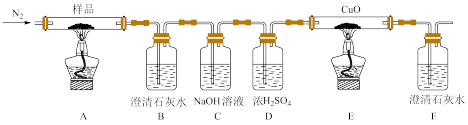
①通入氮气的目的是____ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有____ 、____ 。
③为防止倒吸,停止实验时应进行的操作是___ 。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3。
(3)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀H2SO4酸化,加入适量cmol·L-1KMnO4溶液充分反应,至恰好反应完全,此过程发生的反应是:____ 。
____ +____
+____  +____→____CO2↑+____Mn2++____(请完成配平)。
+____→____CO2↑+____Mn2++____(请完成配平)。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。该晶体中铁的质量分数的表达式为____ 。
(1)已知K3[Fe(C2O4)3]•3H2O中Fe为+3价,则C的化合价为
(2)某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。

①通入氮气的目的是
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③为防止倒吸,停止实验时应进行的操作是
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3。
(3)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀H2SO4酸化,加入适量cmol·L-1KMnO4溶液充分反应,至恰好反应完全,此过程发生的反应是:
____
 +____
+____  +____→____CO2↑+____Mn2++____(请完成配平)。
+____→____CO2↑+____Mn2++____(请完成配平)。②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。该晶体中铁的质量分数的表达式为
您最近一年使用:0次
2022-03-22更新
|
418次组卷
|
3卷引用:湖南省株洲市第二中学2021-2022学年高一上学期第三次月考化学试题

 23.2
23.2

