9-10高三·江苏·阶段练习
名校
1 . 吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断Na2SeO3在人体中的作用是
| A.作氧化剂 | B.作还原剂 |
| C.既作氧化剂又作还原剂 | D.既不作氧化剂又不作还原剂 |
您最近一年使用:0次
2020-06-12更新
|
2128次组卷
|
90卷引用:2011-2012学年北京师大附中高一上学期期末考试化学试卷
(已下线)2011-2012学年北京师大附中高一上学期期末考试化学试卷北京市清华志清中学2018-2019学年高一上学期期中考试化学试题北京市海淀区19中2019-2020学年高一下学期期末考试化学试题(已下线)江苏省2011届高三化学一轮过关测试(3)(已下线)2011届山东省莱州市一中高三上学期阶段测试化学试卷(已下线)2010—2011学年辽宁省营口市高一上学期期末考试化学试卷(已下线)2010—20111学年云南省昆明一中高一上学期期末考试化学试卷(已下线)2010-2011学年山西省临汾一中高一上学期期末考试化学试卷(已下线)2010—2011学年云南省玉溪一中高一期末考试化学试卷(已下线)2010—2011学年浙江杭州师大附属中学高一新疆部)下学期期中考试化学试卷(已下线)2010-2011学年辽宁省丹东市宽甸二中高一(下)阶段教学质量测试化学试卷(已下线)2010—2011学年辽宁省丹东市宽甸二中高一下学期阶段教学质量测试化学试卷(已下线)2012届江西省高安中学高三上学期第二次综合考试化学试卷(已下线)2011-2012学年河南省开封市高一上学期期中考试化学试卷(已下线)2011-2012学年山东省济宁市重点中学高一上学期期中考试化学试卷(已下线)2011-2012学年吉林省吉林市普通中学高一上学期期末考试化学试卷(已下线)2011-2012学年上海市松江二中高一上学期期末考试化学试卷(已下线)2011-2012学年湖南醴陵二中、四中高二下学期期中联考文科化学试卷(已下线)2011-2012学年福建省安溪一中高二下学期期末联考化学试卷(已下线)2012-2013学年陕西省汉中市中学高三上学期模拟考试化学试卷(已下线)2012年苏教版高中化学必修2 1.3从微观结构看物质的多样性练习卷(已下线)2013-2014学年江西省九江一中高一上学期期中考试化学试卷(已下线)2013-2014学年四川省绵阳中学高一上学期第三次月考化学试卷(已下线)2014-2015学年山东临沂商城实验学校高一10月学情调研考试化学卷2015-2016学年河北衡水冀州中学高一上月考三理化学卷2015-2016学年河北省冀州中学高一上第三次月考化学试卷2016届重庆市万州第二高级中学高三11月月考理科综合化学试卷2016-2017学年黑龙江双鸭山一中高一上期中考试化学试卷2016-2017学年江西省九江一中高一上期中化学试卷2016-2017陕西西安长安区一中实验班高一12月考化学卷2016-2017学年福建省四地六校高一下学期第一次联考(3月)化学试卷河北省张家口市第一中学2016-2017学年高一下学期期中考试(实验班、普通班)(理)化学试题江苏省南京市第十三中学2016-2017学年高一上学期期中考试化学试题陕西省城固县第一中学2017-2018学年高一上学期期末考试化学试题(已下线)【走进新高考】(人教版必修一)2.3.2 氧化还原反应——氧化剂和还原剂 同步练习01【全国百强校】重庆市四川外语学院重庆第二外国语学校2018-2019学年高一上学期第二次月考化学试题(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(押题专练)【全国百强校】安徽省合肥市合肥一六八中学2018-2019学年高一(凌志班)上学期期中考试化学试题【全国百强校】湖北省荆州中学2018-2019学年高一上学期期末考试化学试题步步为赢 初高中衔接教材化学暑假作业:第13课时 认识氧化还原反应河北省承德第一中学2019-2020学年高一9月月考化学试题上海市2017-2018学年高一化学第一学期反应原理综合测试题上海市复兴高级中学2018-2019学年高一第一学期期中考试化学试题河南省鲁山县第一高级中学2019-2020学年高一11月月考化学试题湖北省沙市中学2019-2020学年高二上学期期中考试化学(学考)试题吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期第二次月考化学试题四川省成都外国语学校2019-2020学年高一12月月考化学试题四川省成都外国语学校2019-2020学年高一上期第二次月考化学试题云南省临沧市双江县第一中学2019-2020学年高一上学期12月月考化学试题(已下线)【新东方】2019新中心五地019高中化学云南省西双版纳傣族自治州勐腊县第一中学2019-2020学年高一上学期期末考试化学试题江西省抚州市临川第二中学2019-2020学年高一上学期期末考试化学试题云南省普洱市镇沅县第一中学2019—2020学年高一上学期期末考试化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的基本概念河北省衡水中学2019-2020学年高三上学期二调考试化学试题山西省太原市第二十一中学2019-2020高二下学期期中考试化学(文)试题安徽省黄山市祁门县第一中学2019-2020学年高一下学期期中考试化学试题新疆伊犁哈萨克自治州伊宁市第八中学2019-2020学年高一上学期期中考试化学试题(已下线)【南昌新东方】江西省九江一中2013-2014学年高一上学期期中考试化学试题广东省珠海市第二中学2019-2020学年高一上学期期中考试化学试题上海理工大附中2014-2015学年高一上学期期末化学试卷苏教版(2020)高一必修第一册专题3第一单元课时3 氧化还原反应人教版(2019)高一必修第一册 第一章 第三节课时2 氧化剂和还原剂重庆市部分区2019-2020学年高一上学期期末考试化学试题湖南省长沙市周南中学2020-2021学年高一上学期第一次月考化学试题(已下线)【新东方】【2020】【高一上】【第一次月考】【YDC】【化学】天津市第二十一中学2020-2021学年高一上学期期中检测化学试题广西岑溪市2020-2021学年高一上学期期中考试化学试题黑龙江省哈尔滨市第六中学2020-2021学年高一12月月考化学试题安徽省蚌埠田家炳中学2020-2021学年高一12月月考化学试题云南省弥勒市第一中学黄冈校区2020-2021学年高一12月月考化学试题江苏省海安高级中学2020~2021学年高一上学期阶段检测(一)化学试题(已下线)广西南宁市银海三美学校2020-2021学年度上学期高一12月月考化学试题广东省汕尾市2020-2021学年高一上学期期末学业质量监测化学试题青海省湟川中学2019-2020学年高一上学期期中考试化学试题广东华侨中学2020-2021学年高一上学期10月阶段练习化学试题广东省普宁市第二中学2021-2022学年高一上学期第一次月考化学试题吉林省长春市第二十九中学2021-2022学年高一上学期第一次月考化学试题湖北省巴东县第一高级中学2021-2022学年高一上学期第一次教学质量检测化学试题湖北省巴东一中2020-2021学年高一上学期第五次月考化学试题福建省泉州晋江市子江中学2022-2023学年高三8月月考化学试题福建泉州实验中学、安溪一中、养正中学、惠安一中2021-2022高一上学期期中联考化学试题陕西省西安高新第一中学2022-2023学年高一上学期第一次月考 化学试题四川省内江市威远中学校2022-2023学年高一上学期期中考试化学试题福建省莆田第二十五中学2022-2023学年高三上学期期中考试化学试题四川省达州天立学校2022-2023学年高一上学期第一次月考选科摸底测试学试题福建省宁德博雅培文学校2022-2023学年高一上学期线上期末考试化学试题广东省德庆县香山中学2023-2024学年高一上学期9月月考化学试题浙江省台州市黄岩中学2023-2024学年高一上学期10月月考化学试题广东省汕尾市2020-2021学年高一上学期期末学业质量监测化学试题(pdf可编辑版)
2 . 厌氧氨化法(Anammox)是一种新型的氨氮去除技术。下列说法中不正确的是( )。
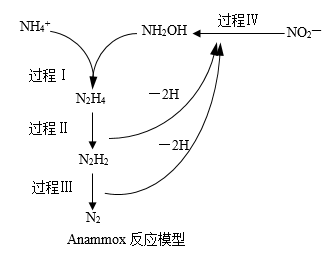

A.1mol 所含的质子总数为10NA 所含的质子总数为10NA |
| B.联氨(N2H4)中含有极性键和非极性键 |
| C.过程Ⅱ属于氧化反应,过程Ⅳ属于还原反应 |
D.过程Ⅰ中,参与反应的 与NH2OH的物质的量之比为1:1 与NH2OH的物质的量之比为1:1 |
您最近一年使用:0次
2020-06-10更新
|
820次组卷
|
20卷引用:北京市大兴区2018高三一模考试理科综合化学试题
北京市大兴区2018高三一模考试理科综合化学试题【全国区级联考】北京市房山区2018届高三第二次(5月)模拟考试理科综合化学试题【区级联考】北京市房山区2019届高三下学期二模考试化学试题【区级联考】北京市房山区2019届高三下学期高考第二次模拟测试理科综合化学试题北京一零一中学2021-2022学年高三上学期 9月开学练习化学试题(已下线)2018年高考题及模拟题汇编 专题04 氧化还原反应(已下线)高考母题题源01 氧化还原反应概念 规律(已下线)学科网2019年高考化学一轮复习讲练测 2.3 氧化还原反应的基本概念 测2020届人教版高三化学二轮复习选择题专攻练——阿伏加德罗常数江西省南昌市新建区第二中学2020届高三下学期第四次线上测试(全国I卷)理综化学试题山东省淄博市部分学校2020届高三6月阶段性诊断考试(二模)化学试题山西省临汾市2020届高考考前适应性考试(三)理综化学试题山西省实验中学2021届高三9月月考化学试题(已下线)小题必刷20 氮及其化合物——2021年高考化学一轮复习小题必刷(通用版)黑龙江省肇东市第四中学校2020届高三下学期4月月考化学试题解题达人.化学选择题(2021全国卷)提升小卷10湖北省麻城市实验高级中学2021-2022学年高三下学期第一次联考化学试题江苏省南京师范大学苏州实验学校2021-2022学年高一上学期12月月考(日新班)化学试题山西省实验中学2020-2021学年高三上学期第一次月考化学试题(已下线)专项特训1 循环转化关系图中的氧化还原反应
3 . 某小组同学探究Cu和H2O2的反应。
【猜想预测】
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
【实验探究】
实验ⅰ:向装有0.5 g Cu的烧杯中加入20 mL 30% H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:________ 。
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2++ 4NH3⇌[ Cu(NH3)4]2+,[ Cu(NH3)4]2+为深蓝色;Cu(OH)2可溶于氨水形成深蓝色溶液。
(2)实验ⅱ中:溶液变蓝的原因是________ (用化学用语解释);经检验产生的气体为氧气,产生氧气的原因是________ 。
(3)对比实验ⅰ和ⅲ,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。
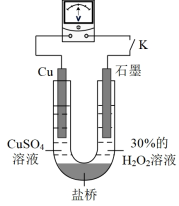
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U形管右侧溶液中滴加氨水后,电压不变。
c.继续向U形管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:_________ 。利用该方法也可证明酸性增强可提高H2O2的氧化性,导致Cu溶解速率加快。
(4)对比实验ⅱ和ⅲ,实验ⅲ中产生氧气速率明显更快,可能的原因是_______ 。
(5)实验ⅲ有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因:________ 。
(6)基于以上实验,影响Cu与H2O2反应速率的因素有________ 。
【猜想预测】
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
【实验探究】
实验ⅰ:向装有0.5 g Cu的烧杯中加入20 mL 30% H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2++ 4NH3⇌[ Cu(NH3)4]2+,[ Cu(NH3)4]2+为深蓝色;Cu(OH)2可溶于氨水形成深蓝色溶液。
| 装置 | 序号 | 试剂a | 现象 |
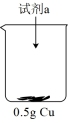 | ⅱ | 20 mL 30% H2O2与4 mL 5 mol/L H2SO4混合液 | Cu表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| ⅲ | 20 mL 30% H2O2与4 mL5 mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(2)实验ⅱ中:溶液变蓝的原因是
(3)对比实验ⅰ和ⅲ,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。

已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U形管右侧溶液中滴加氨水后,电压不变。
c.继续向U形管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:
(4)对比实验ⅱ和ⅲ,实验ⅲ中产生氧气速率明显更快,可能的原因是
(5)实验ⅲ有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因:
(6)基于以上实验,影响Cu与H2O2反应速率的因素有
您最近一年使用:0次
2020-06-06更新
|
339次组卷
|
3卷引用:北京市丰台区2020届高三下学期高三综合练习(二)化学试题
名校
解题方法
4 . 含铬(Ⅵ)废水能诱发致癌,对人类和自然环境有严重的破坏作用。利用Cu2O光催化可以处理含有Cr2O72-的废水。
Ⅰ.制取Cu2O
(1)电解法:利用铜和钛做电极,电解含有NaCl和NaOH的溶液时,反应只消耗了铜和水,体系pH及Cl-浓度维持不变(溶液体积变化忽略不计)。阳极电极反应式是_______ 。
(2)还原法:控制100℃、pH=5的条件时,利用亚硫酸钠与硫酸铜溶液反应可以制得Cu2O,同时产生SO2气体。反应过程中需要不断地加入烧碱,其原因是_______ 。
Ⅱ.利用Cu2O光催化处理含Cr2O72-的废水的研究。
(1)光照射到Cu2O光催化剂上产生光催化反应,Cr2O72-和H2O分别在光催化反应中形成的微电极上发生电极反应,反应原理如图所示。写出Cr2O72-转化Cr3+的电极反应:_______ 。

(2)研究中对Cu2O的作用提出两种假设:
a.Cu2O作光催化剂;b.Cu2O与Cr2O72-发生氧化还原反应。
已知:Cu2O的添加量是2×10-4mol/L,Cr2O72-的初始浓度是1×10-3mol/L;对比实验(pH=3.0且其他条件相同),反应1.5小时结果如图所示。结合试剂用量数据和实验结果可得到的结论是_______ ,依据是_______ 。

(3)溶液的pH对Cr2O72-降解率的影响如图所示。

已知:Cu2O Cu+CuSO4;酸性越大,Cr2O72-被还原率越大。
Cu+CuSO4;酸性越大,Cr2O72-被还原率越大。
①pH分别为2、3、4时,Cr2O72-的降解率最好的是___________ ,其原因是___________ 。
②已知pH=5时,会产生Cr(OH)3沉淀。pH=5时,Cr2O72-的降解率低的原因是___________ 。
Ⅰ.制取Cu2O
(1)电解法:利用铜和钛做电极,电解含有NaCl和NaOH的溶液时,反应只消耗了铜和水,体系pH及Cl-浓度维持不变(溶液体积变化忽略不计)。阳极电极反应式是
(2)还原法:控制100℃、pH=5的条件时,利用亚硫酸钠与硫酸铜溶液反应可以制得Cu2O,同时产生SO2气体。反应过程中需要不断地加入烧碱,其原因是
Ⅱ.利用Cu2O光催化处理含Cr2O72-的废水的研究。
(1)光照射到Cu2O光催化剂上产生光催化反应,Cr2O72-和H2O分别在光催化反应中形成的微电极上发生电极反应,反应原理如图所示。写出Cr2O72-转化Cr3+的电极反应:

(2)研究中对Cu2O的作用提出两种假设:
a.Cu2O作光催化剂;b.Cu2O与Cr2O72-发生氧化还原反应。
已知:Cu2O的添加量是2×10-4mol/L,Cr2O72-的初始浓度是1×10-3mol/L;对比实验(pH=3.0且其他条件相同),反应1.5小时结果如图所示。结合试剂用量数据和实验结果可得到的结论是

(3)溶液的pH对Cr2O72-降解率的影响如图所示。

已知:Cu2O
 Cu+CuSO4;酸性越大,Cr2O72-被还原率越大。
Cu+CuSO4;酸性越大,Cr2O72-被还原率越大。①pH分别为2、3、4时,Cr2O72-的降解率最好的是
②已知pH=5时,会产生Cr(OH)3沉淀。pH=5时,Cr2O72-的降解率低的原因是
您最近一年使用:0次
解题方法
5 . BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图所示。下列说法不正确 的是
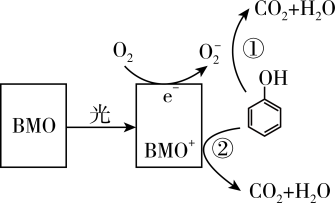

| A.O2-不如O2结构稳定 |
| B.①和②中被降解的苯酚的物质的量之比为1:1 |
| C.降解产物的分子中只含有极性共价键 |
D.该过程的总反应: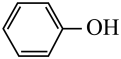 +7O2 +7O2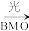 6CO2+3H2O 6CO2+3H2O |
您最近一年使用:0次
名校
解题方法
6 . 中国自古有“信口雌黄”、“雄黄入药”之说。雌黄(As2S3)和雄黄(As4S4)都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。
(1)砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。

①Ⅰ中,氧化剂是______ 。
②Ⅱ中,若1mol As4S4反应转移28mole-,则反应Ⅱ的化学方程式是______ 。
(2)Ⅲ中产物亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液的pH关系如图所示。

①人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是_____ 。
②将KOH溶液滴入亚砷酸溶液,当pH调至11时发生反应的离子方程式是______ 。
③下列说法正确的是______ (填字母序号)。
a.n(H3AsO3):(H2AsO3-)=1:1时,溶液显碱性
b.pH=12时,溶液中c(H2AsO3-)+2c(HAsO32-)+3c(AsO33-)+c(OH-)=c(H+)
c.在K3AsS3溶液中,c(AsO33-)>c(HAsO32-)>c(H2AsO3-)
(3)工业含砷(III)废水常用铁盐处理后排放,其原理是:铁盐混凝剂在溶液中生产Fe(OH)3胶粒,其表面带有正电荷,可吸附含砷化合物。经测定不同pH条件下铁盐对含砷(Ⅲ)化合物的去除率如图所示。pH在5~9之间时,随溶液pH增大,铁盐混凝剂对含砷(Ⅲ)化合物的吸附效果增强。结合(2)和(3)中图示解释可能的原因:_______ 。

(1)砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。

①Ⅰ中,氧化剂是
②Ⅱ中,若1mol As4S4反应转移28mole-,则反应Ⅱ的化学方程式是
(2)Ⅲ中产物亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液的pH关系如图所示。

①人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是
②将KOH溶液滴入亚砷酸溶液,当pH调至11时发生反应的离子方程式是
③下列说法正确的是
a.n(H3AsO3):(H2AsO3-)=1:1时,溶液显碱性
b.pH=12时,溶液中c(H2AsO3-)+2c(HAsO32-)+3c(AsO33-)+c(OH-)=c(H+)
c.在K3AsS3溶液中,c(AsO33-)>c(HAsO32-)>c(H2AsO3-)
(3)工业含砷(III)废水常用铁盐处理后排放,其原理是:铁盐混凝剂在溶液中生产Fe(OH)3胶粒,其表面带有正电荷,可吸附含砷化合物。经测定不同pH条件下铁盐对含砷(Ⅲ)化合物的去除率如图所示。pH在5~9之间时,随溶液pH增大,铁盐混凝剂对含砷(Ⅲ)化合物的吸附效果增强。结合(2)和(3)中图示解释可能的原因:

您最近一年使用:0次
2020-02-23更新
|
193次组卷
|
3卷引用:2016届北京市海淀区高三下学期期中练习理综化学试卷
名校
解题方法
7 . 亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:

| A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2:1 |
| B.若反应①通过原电池来实现,则ClO2是正极产物 |
| C.反应②中的H2O2可用NaClO4代替 |
| D.反应②条件下,ClO2的氧化性大于H2O2 |
您最近一年使用:0次
2020-02-11更新
|
2051次组卷
|
29卷引用:《2020年新高考政策解读与配套资源》模拟试题01-2020年北京新高考化学模拟试题
(已下线)《2020年新高考政策解读与配套资源》模拟试题01-2020年北京新高考化学模拟试题北京市清华附中2019-2020学年高一下学期居家自主学习在线检测化学试题北京市第五中学2021届高三上学期第二次阶段性考试化学试题【省级联考】山东省2020届新高考模拟统考化学试题江苏省镇江市2020届高三上学期期末考试化学试题山东省菏泽市菏泽第一中学2020届高三下学期在线考试化学试题河南省洛阳市2020届高三上学期期末模拟考试化学试题黑龙江省哈尔滨市第三中学2020届高三下学期5月第一次模拟考试(全国II卷)理综化学试题(已下线)第08讲 氧化还原反应的基本概念和规律(精练)——2021年高考化学一轮复习讲练测湖北省宜昌市2019-2020学年高二下学期期末考试化学试题(已下线)第14讲 富集在海水中的元素——卤素(精讲)——2021年高考化学一轮复习讲练测山东省青岛市青岛二中分校2021届高三上学期期中考试化学试题黑龙江省大庆市让胡路区大庆铁人中学2021届高三上学期阶段考试化学试题(已下线)第12讲 富集在海水中的元素——卤素(精讲)-2022年一轮复习讲练测重庆市第七中学校2020-2021学年高三下学期第一次学情检测化学试题重庆市江津中学2021届高三高考全真模拟考试化学试题四川省南充市白塔中学2022届高三第一次月考(9月)化学试题河南省焦作市县级重点中学2021-2022学年高三上学期期中考试化学试题(已下线)第12讲 富集在海水中的元素——卤素(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第10讲 氯及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)江苏南京鼓楼区2021-2022学年高三下学期模拟考试化学试题广东省深圳市新安中学2021-2022学年高三下学期开学测试化学试题河北省石家庄市第四十三中学2022-2023学年高三上学期10月月考化学试题第四章 非金属及其化合物 第18讲 氯及其化合物福建省泉州市第七中学2022-2023学年高一下学期期中考试化学试题(已下线)第1讲 氯及其化合物重庆市第一中学校2023-2024学年高三上学期开学考试化学试题江苏省苏南八校2023-2024学年高二上学期12月联考化学(创新班)试卷(已下线)江苏省南京市、盐城市2024届高三下学期第二次模拟化学试题
名校
8 . 自然界的氮循环如下图所示,下列说法不正确的是( )

| A.①中N2与O2反应生成NO |
| B.②中合成氨属于人工固氮 |
| C.③中氮元素只被氧化 |
| D.氧元素参与了氮循环 |
您最近一年使用:0次
2019-12-26更新
|
815次组卷
|
11卷引用:【区级联考】北京市东城区2017-2018学年高一上学期期末考试化学试题
【区级联考】北京市东城区2017-2018学年高一上学期期末考试化学试题福建省永安一中2019-2020学年高一11月月考化学试题福建省漳平市第一中学2019-2020学年高一上学期第二次月考化学试题湖北省鄂东南联盟2019-2020学年高一下学期期中联考化学试题辽宁省铁岭市调兵山市第二高级中学2019~2020学年高一下学期期末考试化学试题鲁科版(2019)高一必修第一册 综合训练(二)(已下线)专题7 第一单元 氮的固定-高中化学必修第二册苏教版2019人教版2019必修第二册 第五章 第二节 第1课时 氮气与氮的固定 一氧化氮和二氧化氮江苏省扬州市邗江中学2020-2021学年度高一下学期期中考试化学试题安徽省滁州市定远县民族中学2021-2022学年高一下学期期中考试化学试题江苏省扬州市邗江区瓜洲中学2022-2023学年高一下学期3月第一次月考化学试题
9 . 亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:
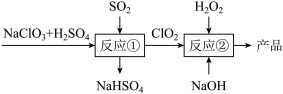
下列说法错误的是( )

下列说法错误的是( )
| A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2:1 |
| B.若反应①通过原电池来实现,则ClO2是正极产物 |
| C.反应②中的H2O2可用NaClO2代替 |
| D.反应②条件下,ClO2的氧化性大于H2O2 |
您最近一年使用:0次
2019-12-05更新
|
437次组卷
|
6卷引用:北京市房山区2020届高三上学期期末考试化学试题
10 . NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是___ ,氧化产物是___ (填写化学式)。
(2)根据上述反应,鉴别NaNO2、NaCl.可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有______ (填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是______ (填编号)。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)化学方程式:10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.若反应过程中转移5mole-,则生成标准状况下N2的体积为______ L。
(1)上述反应中氧化剂是
(2)根据上述反应,鉴别NaNO2、NaCl.可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)化学方程式:10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.若反应过程中转移5mole-,则生成标准状况下N2的体积为
您最近一年使用:0次
2019-11-26更新
|
111次组卷
|
3卷引用:北京师范大学实验中学丰台学校2019-2020学年高三上学期期中考试化学试题



