2022高三·全国·专题练习
解题方法
1 . 亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。查阅资料知:酸性条件下NaNO2具有氧化性。利用所供试剂,设计实验方案验证此信息:_______ (供选用的试剂有NaNO2溶液、FeSO4溶液、稀硫酸、KSCN溶液)
您最近一年使用:0次
解题方法
2 . 化学与生活紧密相关,下列与化学知识有关的描述正确的是
| A.小苏打可用作食品膨松剂,利用其水溶液呈碱性 |
B. 可用于饮用水消毒,利用了其强氧化性 可用于饮用水消毒,利用了其强氧化性 |
C. 用于制作光导纤维,利用了其半导体的特性 用于制作光导纤维,利用了其半导体的特性 |
| D.镁铝合金用于制作航天器外壳,利用了其强还原性 |
您最近一年使用:0次
3 . 某化学兴趣小组为探究高锰酸钾与铜的反应,设计实验如下:
资料:a. 在酸性溶液中不能稳定存在:
在酸性溶液中不能稳定存在: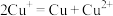
b. 为粉红色沉淀、溶于强酸;
为粉红色沉淀、溶于强酸; 为黑色沉淀、不溶于强酸
为黑色沉淀、不溶于强酸
(1) 被氧化成
被氧化成___________ ,依据是___________ 。
(2)为探究 的还原产物,取A区中溶液
的还原产物,取A区中溶液___________ (填操作和现象),证明有 生成。
生成。
(3)A区中 与
与 反应的离子方程式是
反应的离子方程式是___________ 。
(4)经检验,B区的棕黑色固体是 ,从溶液中离子扩散的角度,结合离子方程式解释B区和C区中的现象:
,从溶液中离子扩散的角度,结合离子方程式解释B区和C区中的现象:___________ 。
(5)小组同学又进行了以下定量实验:
通过计算,分析溶液紫色变浅而未完全褪色的原因:___________ 。
| 实验一 | 现象 |
  酸性溶液 酸性溶液 | 一段时间后,培养皿中由铜片向外侧依次呈现: A区澄清且几乎无色; B区底部覆盖棕黑色固体; C区澄清且紫色变浅 |
 在酸性溶液中不能稳定存在:
在酸性溶液中不能稳定存在: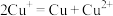
b.
 为粉红色沉淀、溶于强酸;
为粉红色沉淀、溶于强酸; 为黑色沉淀、不溶于强酸
为黑色沉淀、不溶于强酸(1)
 被氧化成
被氧化成(2)为探究
 的还原产物,取A区中溶液
的还原产物,取A区中溶液 生成。
生成。(3)A区中
 与
与 反应的离子方程式是
反应的离子方程式是(4)经检验,B区的棕黑色固体是
 ,从溶液中离子扩散的角度,结合离子方程式解释B区和C区中的现象:
,从溶液中离子扩散的角度,结合离子方程式解释B区和C区中的现象:(5)小组同学又进行了以下定量实验:
| 实验一 | 现象 |
 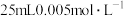  酸性溶液 酸性溶液 | 一段时间后,铜片质量减少了0.02g,溶液中无固体析出、溶液紫色变浅 |
您最近一年使用:0次
4 . H2O2在纸张漂白和废水处理等领域具有重要应用。一定条件下用H2和O2合成H2O2的反应过程示意图如图。下列说法错误的是


| A.O2在催化剂表面得到电子 |
| B.消耗H2和O2物质的量相等 |
| C.H2O2既有氧化性又有还原性 |
| D.H2O2与SO2的漂白原理相同 |
您最近一年使用:0次
5 . 碘及碘化钾是实验室中的常见试剂,含碘废液中碘元素通常以 、
、 、
、 和
和 中的一种或多种形式存在,回收碘具有很好的经济价值。
中的一种或多种形式存在,回收碘具有很好的经济价值。
(1)为检验某实验室酸性废液中是否含 ,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液,
,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液,_______ ,则溶液中含有 。请补充完整该实验方案,实验中可以选用的试剂有:
。请补充完整该实验方案,实验中可以选用的试剂有: 溶液、
溶液、 溶液、淀粉溶液、KSCN溶液、
溶液、淀粉溶液、KSCN溶液、 溶液。
溶液。
(2)一种由含 的废液制取单质碘的流程如下:
的废液制取单质碘的流程如下: 溶液,再加入
溶液,再加入 至沉淀不再增加。
至沉淀不再增加。
Ⅰ.沉碘时有CuI沉淀和 生成,写出该反应的离子方程式:
生成,写出该反应的离子方程式:_______ 。
Ⅱ.若不加入 溶液,仅加入
溶液,仅加入 也可生成CuI沉淀。沉碘时不是仅加入
也可生成CuI沉淀。沉碘时不是仅加入 的原因是
的原因是_______ 。
②氧化、蒸发的装置如图所示。_______ 。
Ⅱ.蒸发出的碘蒸气冷却后易凝固。实验过程中,若发现玻璃导管中有单质碘凝固析出,为防止堵塞,可以采取的方法是_______ 。
(3)若废液中含有 ,可以用
,可以用 进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为
进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为 和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,
和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,_______ 。(已知KI易溶于水;氧化性: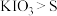 。实验中可以选用的试剂有:
。实验中可以选用的试剂有: 气体、NaOH溶液、稀硫酸)
气体、NaOH溶液、稀硫酸)
(4)某含碘废液中,碘元素以 形式存在,为测定
形式存在,为测定 的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
 溶液滴定
溶液滴定 至恰好完全反应,消耗
至恰好完全反应,消耗 溶液24.00mL。已知测定过程中发生的反应为
溶液24.00mL。已知测定过程中发生的反应为 (未配平)
(未配平)  (未配平)
(未配平)
计算废液中 的物质的量浓度,并写出计算过程
的物质的量浓度,并写出计算过程______ 。
 、
、 、
、 和
和 中的一种或多种形式存在,回收碘具有很好的经济价值。
中的一种或多种形式存在,回收碘具有很好的经济价值。(1)为检验某实验室酸性废液中是否含
 ,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液,
,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液, 。请补充完整该实验方案,实验中可以选用的试剂有:
。请补充完整该实验方案,实验中可以选用的试剂有: 溶液、
溶液、 溶液、淀粉溶液、KSCN溶液、
溶液、淀粉溶液、KSCN溶液、 溶液。
溶液。(2)一种由含
 的废液制取单质碘的流程如下:
的废液制取单质碘的流程如下:
 溶液,再加入
溶液,再加入 至沉淀不再增加。
至沉淀不再增加。Ⅰ.沉碘时有CuI沉淀和
 生成,写出该反应的离子方程式:
生成,写出该反应的离子方程式:Ⅱ.若不加入
 溶液,仅加入
溶液,仅加入 也可生成CuI沉淀。沉碘时不是仅加入
也可生成CuI沉淀。沉碘时不是仅加入 的原因是
的原因是②氧化、蒸发的装置如图所示。
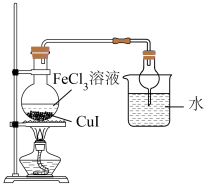
Ⅱ.蒸发出的碘蒸气冷却后易凝固。实验过程中,若发现玻璃导管中有单质碘凝固析出,为防止堵塞,可以采取的方法是
(3)若废液中含有
 ,可以用
,可以用 进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为
进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为 和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,
和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,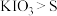 。实验中可以选用的试剂有:
。实验中可以选用的试剂有: 气体、NaOH溶液、稀硫酸)
气体、NaOH溶液、稀硫酸)(4)某含碘废液中,碘元素以
 形式存在,为测定
形式存在,为测定 的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
 溶液滴定
溶液滴定 至恰好完全反应,消耗
至恰好完全反应,消耗 溶液24.00mL。已知测定过程中发生的反应为
溶液24.00mL。已知测定过程中发生的反应为 (未配平)
(未配平)  (未配平)
(未配平)计算废液中
 的物质的量浓度,并写出计算过程
的物质的量浓度,并写出计算过程
您最近一年使用:0次
2023高三·全国·专题练习
6 . 高铁酸钾 被称为“绿色化学试剂”,在酸性至弱碱性条件下不稳定;
被称为“绿色化学试剂”,在酸性至弱碱性条件下不稳定; 溶液呈紫红色,具有强氧化性,与
溶液呈紫红色,具有强氧化性,与 反应时,溶液颜色会逐渐褪去,并出现红褐色沉淀。
反应时,溶液颜色会逐渐褪去,并出现红褐色沉淀。
(1) 可用于自来水处理,其原理是
可用于自来水处理,其原理是_______ 。
(2)电解法可制得 ,装置如图所示,阳极电极反应式为
,装置如图所示,阳极电极反应式为_______ 。若电解质溶液中混有少量 杂质,电解效果会显著降低,其原因是
杂质,电解效果会显著降低,其原因是_______ 。

 被称为“绿色化学试剂”,在酸性至弱碱性条件下不稳定;
被称为“绿色化学试剂”,在酸性至弱碱性条件下不稳定; 溶液呈紫红色,具有强氧化性,与
溶液呈紫红色,具有强氧化性,与 反应时,溶液颜色会逐渐褪去,并出现红褐色沉淀。
反应时,溶液颜色会逐渐褪去,并出现红褐色沉淀。(1)
 可用于自来水处理,其原理是
可用于自来水处理,其原理是(2)电解法可制得
 ,装置如图所示,阳极电极反应式为
,装置如图所示,阳极电极反应式为 杂质,电解效果会显著降低,其原因是
杂质,电解效果会显著降低,其原因是
您最近一年使用:0次
21-22高三上·江苏南通·期末
名校
解题方法
7 . 用化学方法降解水中有机物已成为污水处理领域的重要研究方向。
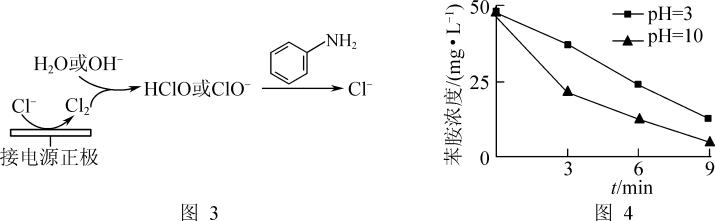
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。
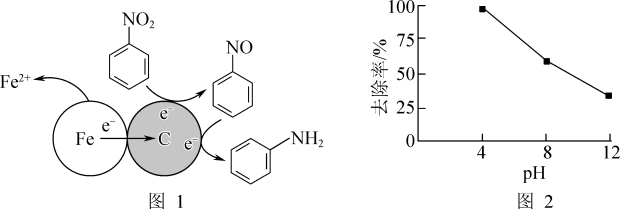
①该物质转化示意图可以描述为_______ 。
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是_______ 。
(2)向含Fe2+和苯胺(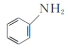 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:_______ 。
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:_______ 。
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是_______ 。[已知氧化性:HClO(H+)>ClO-(OH-)]
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。

①该物质转化示意图可以描述为
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是
(2)向含Fe2+和苯胺(
 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是

您最近一年使用:0次
8 . 某学习小组拟研究FeSO4的分解实验探究,请你利用所学知识帮该小组完成以下实验方案。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2 ;
假设2:FeO、SO3、SO2;
假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是_______ 。
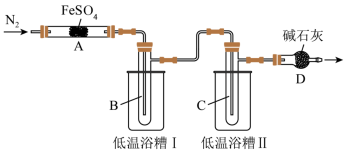
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是_______ ,(只填操作),当A处固体完全分解后通入N2的目的是_______ 。
(3)实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备N2,该反应的离子方程式为_______ 。
(4)低温浴槽Ⅰ收集的物质是_______ (填化学式),低温浴槽Ⅱ控制的温度范围为_______ 。
(5)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
甲组实验中A装置得到固体产物是_______ (填化学式)。
(6)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是_______ 。
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(7)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案_______ (填“1”或“2”)可行。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2 ;
假设2:FeO、SO3、SO2;
假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
| 物质 | SO3 | SO2 | O2 | N2 |
| 熔点/℃ | 16.8 | - 72.4 | -218.4 | -209.9 |
| 沸点/℃ | 44.8 | - 10 | -182.9 | - 195.8 |

回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是
(3)实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备N2,该反应的离子方程式为
(4)低温浴槽Ⅰ收集的物质是
(5)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
| 实验 | A处温度/℃ | FeSO4质量/g | 低温浴槽Ⅰ净增质量/g | 低温浴槽Ⅱ净增质量/g |
| 甲 | T1 | 3.04 | 0.80 | 0.64 |
| 乙 | T2 | 4.56 | 1.60 | 0.64 |
(6)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(7)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案
您最近一年使用:0次
解题方法
9 . 化学需氧量(COD)是指用强氧化剂将1L废水中的还原性物质氧化为二氧化碳和水所消耗的氧化剂的量,并换算成以 为氧化剂时所消耗
为氧化剂时所消耗 的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一、Fenton(
的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一、Fenton( )法能产生
)法能产生 和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
(1)羟基自由基(·OH)的电子式为_______ 。
(2)分别取初始pH=4、COD=80的废水200mL,加入200mL ,改变起始投加
,改变起始投加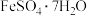 的量,反应相同时间。测得反应后水样COD随
的量,反应相同时间。测得反应后水样COD随 投加量的关系如图所示。当
投加量的关系如图所示。当 投加量超过1
投加量超过1 时,反应后水样COD不降反升的原因可能是
时,反应后水样COD不降反升的原因可能是_______ 。
(3)已知·OH更容易进攻有机物分子中电子云密度较大的基团。1-丁醇比正戊烷更容易受到·OH进攻的原因是_______ 。
(4)在Fenton法的基础上改进的基于硫酸根自由基(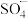 )的氧化技术引起关注。研究发现,一种
)的氧化技术引起关注。研究发现,一种 石墨烯纳米复合材料对催化活化
石墨烯纳米复合材料对催化活化 产生
产生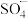 具有很好的效果。
具有很好的效果。 结构为
结构为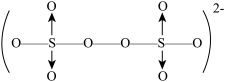 。
。
①与 试剂相比,
试剂相比, 一石墨烯/
一石墨烯/ 的使用范围更广。
的使用范围更广。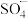 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:_______ 。
②一种制取 一石墨烯纳米复合材料的物种转化关系可表示为(GO表示石墨烯)
一石墨烯纳米复合材料的物种转化关系可表示为(GO表示石墨烯)
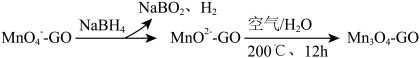
在石墨烯表面制得1mol ,理论上需要消耗
,理论上需要消耗 的物质的量为
的物质的量为_______ mol。
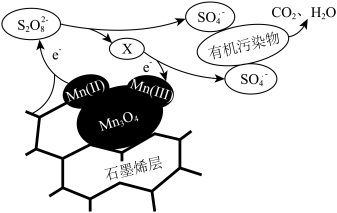
③利用该复合材料催化活化 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为_______ 。
 为氧化剂时所消耗
为氧化剂时所消耗 的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一、Fenton(
的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一、Fenton( )法能产生
)法能产生 和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。(1)羟基自由基(·OH)的电子式为
(2)分别取初始pH=4、COD=80的废水200mL,加入200mL
 ,改变起始投加
,改变起始投加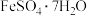 的量,反应相同时间。测得反应后水样COD随
的量,反应相同时间。测得反应后水样COD随 投加量的关系如图所示。当
投加量的关系如图所示。当 投加量超过1
投加量超过1 时,反应后水样COD不降反升的原因可能是
时,反应后水样COD不降反升的原因可能是
(3)已知·OH更容易进攻有机物分子中电子云密度较大的基团。1-丁醇比正戊烷更容易受到·OH进攻的原因是
(4)在Fenton法的基础上改进的基于硫酸根自由基(
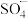 )的氧化技术引起关注。研究发现,一种
)的氧化技术引起关注。研究发现,一种 石墨烯纳米复合材料对催化活化
石墨烯纳米复合材料对催化活化 产生
产生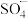 具有很好的效果。
具有很好的效果。 结构为
结构为 。
。①与
 试剂相比,
试剂相比, 一石墨烯/
一石墨烯/ 的使用范围更广。
的使用范围更广。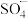 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:②一种制取
 一石墨烯纳米复合材料的物种转化关系可表示为(GO表示石墨烯)
一石墨烯纳米复合材料的物种转化关系可表示为(GO表示石墨烯)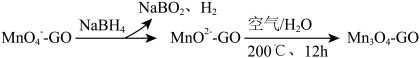
在石墨烯表面制得1mol
 ,理论上需要消耗
,理论上需要消耗 的物质的量为
的物质的量为③利用该复合材料催化活化
 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
您最近一年使用:0次
10 . 目前,汽车尾气系统中均安装了催化转化器,这种方法是处理 的“储存还原技术法”,简称
的“储存还原技术法”,简称 ,工作原理如图所示。下列说法中正确的是
,工作原理如图所示。下列说法中正确的是
 的“储存还原技术法”,简称
的“储存还原技术法”,简称 ,工作原理如图所示。下列说法中正确的是
,工作原理如图所示。下列说法中正确的是
A.在富氧氛围下喷入少量燃油可以生成 、 、 等还原性尾气 等还原性尾气 |
B. 系统中的只有一种催化剂 系统中的只有一种催化剂 |
C.存储阶段,氮元素被氧化,以 的形式被存储起来 的形式被存储起来 |
D.还原阶段,每生成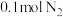 ,转移 ,转移 电子 电子 |
您最近一年使用:0次
2022-12-09更新
|
1064次组卷
|
5卷引用:2022年天津市普通高中学业水平等级性考试化学试题变式题(选择题5-8)
(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(选择题5-8)广东省六校2023届高三第三次联考化学试题广东省六校联盟2022-2023学年高三上学期第三次联考化学试题广东省广州市第二中学等五校2022-2023学年高三上学期12月月考化学试题安徽省马鞍山市第二中学2023-2024学年高二上学期12月阶段检测化学试题



