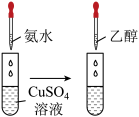
1 . 下列化学反应中:
① (未配平)
(未配平)
②
③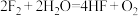
④
⑤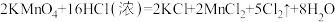
⑥
⑦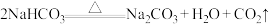
回答下列问题:
(1)上述反应中,既是分解反应,又是氧化还原反应的是___________ (填序号)。
(2)反应①中的氧化剂是___________ ,被氧化的元素是___________ ,用化合价升降法配平①中的反应方程式:___________ 。
(3)反应④中氧化产物和还原产物的质量之比为___________ ;反应⑤中浓盐酸表现出的性质是___________ (填字母)。
A.还原性 B.酸性 C.氧化性 D.挥发性
(4)请用双线桥法标出反应⑥电子转移的方向及数目:___________ ;产生1 mol  时,转移的电子的物质的量为准状况下的气体体积为
时,转移的电子的物质的量为准状况下的气体体积为___________ mol;1 mol  参加反应时,生成标准状况下的气体体积为
参加反应时,生成标准状况下的气体体积为___________ L。
①
 (未配平)
(未配平)②

③
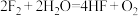
④

⑤
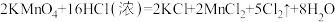
⑥

⑦
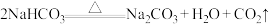
回答下列问题:
(1)上述反应中,既是分解反应,又是氧化还原反应的是
(2)反应①中的氧化剂是
(3)反应④中氧化产物和还原产物的质量之比为
A.还原性 B.酸性 C.氧化性 D.挥发性
(4)请用双线桥法标出反应⑥电子转移的方向及数目:
 时,转移的电子的物质的量为准状况下的气体体积为
时,转移的电子的物质的量为准状况下的气体体积为 参加反应时,生成标准状况下的气体体积为
参加反应时,生成标准状况下的气体体积为
您最近一年使用:0次
名校
2 . 铜及其化合物有着广泛的应用。某实验小组探究 的性质。
的性质。
I.实验准备:
(1)由 固体配制
固体配制 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有_________ (填序号)。
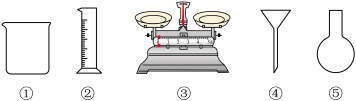
实验任务:探究 溶液分别与
溶液分别与 、
、 溶液的反应
溶液的反应
查阅资料:
已知:a.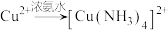 (深蓝色溶液)
(深蓝色溶液)
b. (无色溶液)
(无色溶液) (深蓝色溶液)
(深蓝色溶液)
设计方案并完成实验:
现象分析与验证:
(2)推测实验B产生的无色气体为 ,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到
,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到__________ 。
(3)推测实验B中的白色沉淀为 ,实验验证步骤如下:
,实验验证步骤如下:
①实验B完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量________ ,观察到沉淀溶解,得到无色溶液,此反应的离子方程式为__________ ;露置在空气中一段时间,观察到溶液变为深蓝色。
(4)对比实验A、B,提出假设: 增强了
增强了 的氧化性。
的氧化性。
①若假设合理,实验B反应的离子方程式为
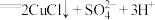 和
和__________ 。
②下述实验C证实了假设合理,装置如图8(两个电极均为碳棒)。实验方案:闭合K,电压表的指针偏转至“X”处;向U形__________ (补全实验操作及现象)。
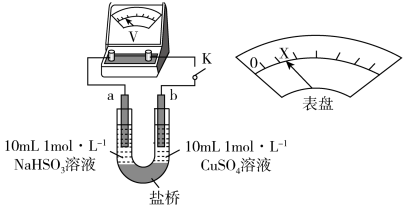
Ⅱ. 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。
(5)硫酸铜溶液呈蓝色的原因是溶液中存在配离子_________ (填化学式)。
(6)常见配合物的形成实验
 的性质。
的性质。I.实验准备:
(1)由
 固体配制
固体配制 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有
实验任务:探究
 溶液分别与
溶液分别与 、
、 溶液的反应
溶液的反应查阅资料:
已知:a.
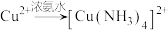 (深蓝色溶液)
(深蓝色溶液)b.
 (无色溶液)
(无色溶液) (深蓝色溶液)
(深蓝色溶液)设计方案并完成实验:
实验 | 装置 | 试剂x | 操作及现象 |
A |
| 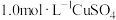 溶液 溶液 | 加入  溶液,得到绿色溶液, 溶液,得到绿色溶液, 未见明显变化。 未见明显变化。 |
B | 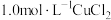 溶液 溶液 | 加入  溶液,得到绿色溶液, 溶液,得到绿色溶液, 时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 |
(2)推测实验B产生的无色气体为
 ,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到
,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到(3)推测实验B中的白色沉淀为
 ,实验验证步骤如下:
,实验验证步骤如下:①实验B完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量
(4)对比实验A、B,提出假设:
 增强了
增强了 的氧化性。
的氧化性。①若假设合理,实验B反应的离子方程式为

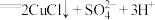 和
和②下述实验C证实了假设合理,装置如图8(两个电极均为碳棒)。实验方案:闭合K,电压表的指针偏转至“X”处;向U形

Ⅱ.
 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。(5)硫酸铜溶液呈蓝色的原因是溶液中存在配离子
(6)常见配合物的形成实验
实验操作 | 实验现象 | 有关离子方程式 |
| 滴加氨水后,试管中首先出现蓝色沉淀,氨水过量后沉淀逐渐 |  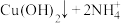   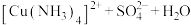 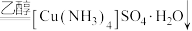 |
您最近一年使用:0次
2023-05-16更新
|
853次组卷
|
2卷引用:广东省茂名市第一中学2022-2023学年高三下学期5月月考化学试题
名校
3 . 按要求填空。
(1)标准状况下,10.8g某气体的体积是8.96L,则此气体的相对分子质量为___________ 。
(2)现有标准状况下CO和 混合气体8.96L,其质量为16g,则此混合气体中,CO气体的体积分数为
混合气体8.96L,其质量为16g,则此混合气体中,CO气体的体积分数为___________ 。
(3)已知16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为___________ 。
(4)维生素C能帮助人体将食物中摄取的、不易吸收的 转变为易吸收的
转变为易吸收的 ,这说明维生素C具有
,这说明维生素C具有___________ 性(填氧化性或还原性)。
(5)已知: 难溶于水,但可溶于醋酸氨溶液中形成无色溶液,生成的
难溶于水,但可溶于醋酸氨溶液中形成无色溶液,生成的 是难电离的物质,其化学方程式为
是难电离的物质,其化学方程式为 。写出该反应的离子方程式:
。写出该反应的离子方程式:___________ 。
(1)标准状况下,10.8g某气体的体积是8.96L,则此气体的相对分子质量为
(2)现有标准状况下CO和
 混合气体8.96L,其质量为16g,则此混合气体中,CO气体的体积分数为
混合气体8.96L,其质量为16g,则此混合气体中,CO气体的体积分数为(3)已知16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
(4)维生素C能帮助人体将食物中摄取的、不易吸收的
 转变为易吸收的
转变为易吸收的 ,这说明维生素C具有
,这说明维生素C具有(5)已知:
 难溶于水,但可溶于醋酸氨溶液中形成无色溶液,生成的
难溶于水,但可溶于醋酸氨溶液中形成无色溶液,生成的 是难电离的物质,其化学方程式为
是难电离的物质,其化学方程式为 。写出该反应的离子方程式:
。写出该反应的离子方程式:
您最近一年使用:0次
解题方法
4 . 化学使生活更美好。下列物质使用时涉及的原理不正确的是
| 选项 | 物质用途 | 性质 |
| A | 聚乳酸用于手术缝合线 | 聚乳酸具有生物相容性和可吸收性 |
| B | 中秋节月饼包装袋中放入小袋铁粉 | 铁粉具有还原性 |
| C | 75%酒精溶液用于消毒 |  具有强氧化性 具有强氧化性 |
| D | 化妆品中添加甘油 | 丙三醇具有较强的吸水性能 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 高铁酸钾 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是| A.氢氧化铁胶体具有碱性,可用于净水 |
B. 具有氧化性,可作为特定环境中的抗氧化剂 具有氧化性,可作为特定环境中的抗氧化剂 |
| C.高铁酸钾能溶于水,水溶液呈紫色,可作氧化剂 |
| D.氧化铁呈红棕色且遮盖效果好,可用作红色颜料 |
您最近一年使用:0次
2023-12-31更新
|
253次组卷
|
2卷引用:江苏省南通市名校联盟2024届高三上学期12月学业质量联合监测化学试卷
名校
解题方法
6 . 科学家发现,自来水用ClO2处理成饮用水更能提升自来水的品质。下列说法不正确的是
| A.ClO2、HClO的消毒原理相同 |
| B.ClO2、Cl2稀溶液用于环境消毒,具有广谱高效的特点 |
| C.ClO2在常温下为气体,在自然环境中最终转化为Cl- |
| D.ClO2、HClO均有强氧化性无还原性 |
您最近一年使用:0次
解题方法
7 . 亚氯酸钠( )是一种高效的消毒剂,其制备流程如下:
)是一种高效的消毒剂,其制备流程如下:
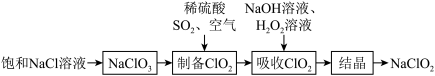
下列说法正确的是
 )是一种高效的消毒剂,其制备流程如下:
)是一种高效的消毒剂,其制备流程如下:
下列说法正确的是
A.电解饱和 制取 制取 过程中,阴极反应式为 过程中,阴极反应式为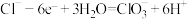 |
B.制备 时,通入空气的目的是将 时,通入空气的目的是将 氧化为 氧化为 ,增强溶液的酸性 ,增强溶液的酸性 |
C. 逸出后,溶液中含有大量的 逸出后,溶液中含有大量的 、 、 、 、 、 、 |
D. 在吸收 在吸收 的过程中体现了还原性 的过程中体现了还原性 |
您最近一年使用:0次
8 . 碘及碘化钾是实验室中的常见试剂,含碘废液中碘元素通常以 、
、 、
、 和
和 中的一种或多种形式存在,回收碘具有很好的经济价值。
中的一种或多种形式存在,回收碘具有很好的经济价值。
(1)为检验某实验室酸性废液中是否含 ,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液,
,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液,_______ ,则溶液中含有 。请补充完整该实验方案,实验中可以选用的试剂有:
。请补充完整该实验方案,实验中可以选用的试剂有: 溶液、
溶液、 溶液、淀粉溶液、KSCN溶液、
溶液、淀粉溶液、KSCN溶液、 溶液。
溶液。
(2)一种由含 的废液制取单质碘的流程如下:
的废液制取单质碘的流程如下: 溶液,再加入
溶液,再加入 至沉淀不再增加。
至沉淀不再增加。
Ⅰ.沉碘时有CuI沉淀和 生成,写出该反应的离子方程式:
生成,写出该反应的离子方程式:_______ 。
Ⅱ.若不加入 溶液,仅加入
溶液,仅加入 也可生成CuI沉淀。沉碘时不是仅加入
也可生成CuI沉淀。沉碘时不是仅加入 的原因是
的原因是_______ 。
②氧化、蒸发的装置如图所示。_______ 。
Ⅱ.蒸发出的碘蒸气冷却后易凝固。实验过程中,若发现玻璃导管中有单质碘凝固析出,为防止堵塞,可以采取的方法是_______ 。
(3)若废液中含有 ,可以用
,可以用 进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为
进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为 和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,
和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,_______ 。(已知KI易溶于水;氧化性: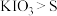 。实验中可以选用的试剂有:
。实验中可以选用的试剂有: 气体、NaOH溶液、稀硫酸)
气体、NaOH溶液、稀硫酸)
(4)某含碘废液中,碘元素以 形式存在,为测定
形式存在,为测定 的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
 溶液滴定
溶液滴定 至恰好完全反应,消耗
至恰好完全反应,消耗 溶液24.00mL。已知测定过程中发生的反应为
溶液24.00mL。已知测定过程中发生的反应为 (未配平)
(未配平)  (未配平)
(未配平)
计算废液中 的物质的量浓度,并写出计算过程
的物质的量浓度,并写出计算过程______ 。
 、
、 、
、 和
和 中的一种或多种形式存在,回收碘具有很好的经济价值。
中的一种或多种形式存在,回收碘具有很好的经济价值。(1)为检验某实验室酸性废液中是否含
 ,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液,
,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液, 。请补充完整该实验方案,实验中可以选用的试剂有:
。请补充完整该实验方案,实验中可以选用的试剂有: 溶液、
溶液、 溶液、淀粉溶液、KSCN溶液、
溶液、淀粉溶液、KSCN溶液、 溶液。
溶液。(2)一种由含
 的废液制取单质碘的流程如下:
的废液制取单质碘的流程如下:
 溶液,再加入
溶液,再加入 至沉淀不再增加。
至沉淀不再增加。Ⅰ.沉碘时有CuI沉淀和
 生成,写出该反应的离子方程式:
生成,写出该反应的离子方程式:Ⅱ.若不加入
 溶液,仅加入
溶液,仅加入 也可生成CuI沉淀。沉碘时不是仅加入
也可生成CuI沉淀。沉碘时不是仅加入 的原因是
的原因是②氧化、蒸发的装置如图所示。
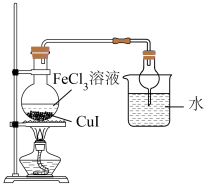
Ⅱ.蒸发出的碘蒸气冷却后易凝固。实验过程中,若发现玻璃导管中有单质碘凝固析出,为防止堵塞,可以采取的方法是
(3)若废液中含有
 ,可以用
,可以用 进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为
进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为 和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,
和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,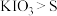 。实验中可以选用的试剂有:
。实验中可以选用的试剂有: 气体、NaOH溶液、稀硫酸)
气体、NaOH溶液、稀硫酸)(4)某含碘废液中,碘元素以
 形式存在,为测定
形式存在,为测定 的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
 溶液滴定
溶液滴定 至恰好完全反应,消耗
至恰好完全反应,消耗 溶液24.00mL。已知测定过程中发生的反应为
溶液24.00mL。已知测定过程中发生的反应为 (未配平)
(未配平)  (未配平)
(未配平)计算废液中
 的物质的量浓度,并写出计算过程
的物质的量浓度,并写出计算过程
您最近一年使用:0次
9 . 铁是应用最广泛的金属,在工农业生产和生活中占有重要的地位。运用铁及其化合物的知识,完成下列问题。
(1)苹果汁中含有 ,它是人们喜欢的一种补铁饮料,现榨苹果汁在空气中由浅绿色变为棕黄色的原因是
,它是人们喜欢的一种补铁饮料,现榨苹果汁在空气中由浅绿色变为棕黄色的原因是___________ 。
(2)中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是___________ (填化学式)。氧化铁俗称铁红,常用作___________ ;氧化铁与氢碘酸反应的离子方程式为___________ 。
(3)电子工业需要用 的
的 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:___________ 。
(4)高铁酸钾( )是一种新型、高效、多功能水处理剂。已知:
)是一种新型、高效、多功能水处理剂。已知:
① 与
与 在强碱性条件下反应可制取
在强碱性条件下反应可制取 ;
;
② 具有强氧化性,在酸性或中性溶液中迅速产生氧气:
具有强氧化性,在酸性或中性溶液中迅速产生氧气: ;
;
制取 的离子方程式为
的离子方程式为______ , 作水处理剂的原因
作水处理剂的原因______ 。
(1)苹果汁中含有
 ,它是人们喜欢的一种补铁饮料,现榨苹果汁在空气中由浅绿色变为棕黄色的原因是
,它是人们喜欢的一种补铁饮料,现榨苹果汁在空气中由浅绿色变为棕黄色的原因是(2)中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是
(3)电子工业需要用
 的
的 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:(4)高铁酸钾(
 )是一种新型、高效、多功能水处理剂。已知:
)是一种新型、高效、多功能水处理剂。已知:①
 与
与 在强碱性条件下反应可制取
在强碱性条件下反应可制取 ;
; ②
 具有强氧化性,在酸性或中性溶液中迅速产生氧气:
具有强氧化性,在酸性或中性溶液中迅速产生氧气: ;
;制取
 的离子方程式为
的离子方程式为 作水处理剂的原因
作水处理剂的原因
您最近一年使用:0次
名校
解题方法
10 . 某化学兴趣小组设计一种从硫矿石(主要成分为硫黄及少量FeS2)中提取硫黄的方法如下:
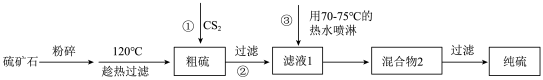
查阅资料:S的熔点为115.2℃; 的沸点为46.2℃。
的沸点为46.2℃。
下列说法错误的是

查阅资料:S的熔点为115.2℃;
 的沸点为46.2℃。
的沸点为46.2℃。下列说法错误的是
| A.单质硫是分子晶体 |
B.过程①中 可用乙醇代替 可用乙醇代替 |
C.过程③的目的是使 挥发,同时使硫从水中析出 挥发,同时使硫从水中析出 |
D.将趁热过滤所得滤渣煅烧: ,反应中每生成1 mol ,反应中每生成1 mol  ,转移电子的物质的量为5.5 mol ,转移电子的物质的量为5.5 mol |
您最近一年使用:0次
2023-03-08更新
|
478次组卷
|
3卷引用:湖南省邵阳市邵东市2022-2023学年高三下学期3月月考化学试题



 溶液
溶液