广东省百校2022-2023年高三上学期11月联考化学试题
广东
高三
阶段练习
2022-12-06
342次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、有机化学基础、化学反应原理、化学实验基础、物质结构与性质
广东省百校2022-2023年高三上学期11月联考化学试题
广东
高三
阶段练习
2022-12-06
342次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、有机化学基础、化学反应原理、化学实验基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
较易(0.85)
解题方法
1. 中国文化博大精深。下列文物保存时需要防潮防霉变的是
| 选项 | A | B | C | D |
| 文物 |
|
|
|
|
| 名称 | 翠玉白菜 | 简牍 | 清雍正款霁红釉瓷碗 | 萧何月下追韩信梅瓶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-27更新
|
257次组卷
|
3卷引用:广东省百校2022-2023年高三上学期11月联考化学试题
单选题
|
适中(0.65)
解题方法
2. 化学使生活更美好。下列物质使用时涉及的原理不正确的是
| 选项 | 物质用途 | 性质 |
| A | 聚乳酸用于手术缝合线 | 聚乳酸具有生物相容性和可吸收性 |
| B | 中秋节月饼包装袋中放入小袋铁粉 | 铁粉具有还原性 |
| C | 75%酒精溶液用于消毒 |  具有强氧化性 具有强氧化性 |
| D | 化妆品中添加甘油 | 丙三醇具有较强的吸水性能 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
3. 我国科技成果令世界瞩目。下列说法不正确的是
| A.“天眼”的结构中含有大量钢,钢的硬度低于纯铁 |
| B.“神舟十四号”返回舱外壳用的烧蚀材料酚醛树脂属于有机高分子材料 |
| C.“辽宁舰”的船体镶嵌锌块,利用的是牺牲阳极保护法 |
| D.“祝融号”火星车的太阳能电池材料主要成分是硅 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
4. 科学家以 、
、 、氨水为原料,合成乙醇梭菌蛋白。下列化学用语不正确的是
、氨水为原料,合成乙醇梭菌蛋白。下列化学用语不正确的是
 、
、 、氨水为原料,合成乙醇梭菌蛋白。下列化学用语不正确的是
、氨水为原料,合成乙醇梭菌蛋白。下列化学用语不正确的是A. 的电子式: 的电子式: | B. 的结构式: 的结构式: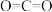 |
C. 的球棍模型: 的球棍模型: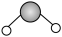 | D.乙醇的结构简式: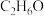 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
5. 实验是化学的灵魂。下列实验装置或操作正确的是
| A | B | C | D |
 | 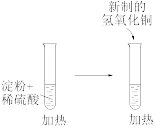 | 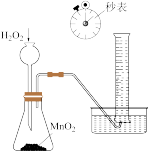 | 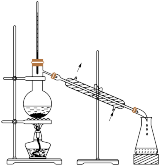 |
| 收集氨气 | 检验淀粉水解产物 | 测量 分解速率 分解速率 | 分离水和苯的混合液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
6. 某酰胺类化合物的分子结构如图。下列说法不正确的是
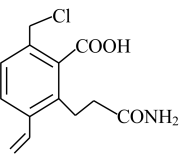

| A.分子中所有碳原子可能共平面 |
| B.分子中含有手性碳原子 |
| C.该物质既有酸性又有碱性 |
| D.该物质可发生加成反应、取代反应 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
您最近一年使用:0次
2021-11-03更新
|
746次组卷
|
4卷引用:广东省佛山顺德市2021-2022学年高三一模化学试题
单选题
|
适中(0.65)
解题方法
8. 利用下图装置进行电镀实验。电镀液为0.1mol/LCuSO4和过量1mol/L氨水混合液。实验发现:一段时间后阴极表面有致密红色固体。下列说法不正确的是
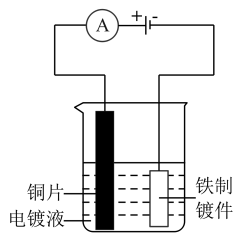

A.欲检验电镀液中是否有Fe元素,可从阴极区取少量溶液于试管中,再滴入2滴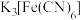 溶液 溶液 |
B. 存在配位键,配体是 存在配位键,配体是 ,配位数是4 ,配位数是4 |
| C.实验前可用盐酸除掉铁制镀件上的油污 |
D. 生成 生成 , , 小, 小, 缓慢析出,镀层更致密 缓慢析出,镀层更致密 |
您最近一年使用:0次
单选题
|
适中(0.65)
9. 有“锂”走遍天下,锂在电池中应用广泛。下列说法正确的是
A. 溶液中含有 溶液中含有 个 个 |
B. 晶体中含有 晶体中含有 个 个 |
C. 与水反应,可得到 与水反应,可得到 |
D. 在 在 中完全燃烧,生成 中完全燃烧,生成 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
10. 下列指定反应的离子方程式书写正确的是
A.FeO遇到稀硝酸: |
B.少量 通入漂白液: 通入漂白液: |
C.向 溶液中加入少量 溶液中加入少量 溶液: 溶液: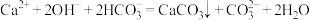 |
D.泡沫灭火器原理: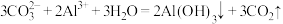 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
11. 聚合物前驱体转化法在陶瓷材料制备领域有重要应用价值,一种聚合物前驱体结构如图所示(R1、R2表示烃基)。W、X、Y、Z为原子序数依次增大的短周期元素,X、Z同主族,W的核外电子总数等于Y的最外层电子数。下列说法不正确的是
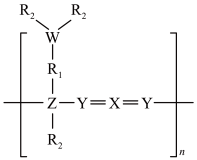
A.原子半径: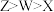 |
B.简单氢化物沸点: |
C.最高价含氧酸的酸性: |
D.Z的氧化物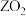 为共价晶体 为共价晶体 |
您最近一年使用:0次
2022-11-27更新
|
1317次组卷
|
5卷引用:广东省百校2022-2023年高三上学期11月联考化学试题
广东省百校2022-2023年高三上学期11月联考化学试题(已下线)热点情景汇编-专题九 物质结构与性质(已下线)【知识图鉴】单元讲练测选择性必修2第1章03巩固练江西省丰城中学2022-2023学年高二下学期开学考试化学试题广东省东莞市石竹实验学校2023-2024学年高二上学期10月月考化学试题
12. 根据实验目的,下列实验及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 比较 和 和 的水解常数 的水解常数 | 分别测等浓度的 和 和 溶液的pH,后者大于前者 溶液的pH,后者大于前者 | 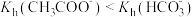 |
| B | 比较Cl、Br、I的非金属性 | 向NaBr溶液中加过量氯水,再加入淀粉KI溶液,先变橙色,后变蓝色 | 非金属性: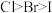 |
| C | 探究温度对化学平衡的影响 | 加热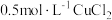 溶液,溶液变为黄绿色,再冷却,溶液由黄绿色变为蓝绿色 溶液,溶液变为黄绿色,再冷却,溶液由黄绿色变为蓝绿色 | 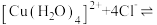 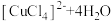 是吸热反应 是吸热反应 |
| D | 证明某钠盐的成分 | 向该钠盐中滴加浓盐酸,并将产生的气体通入品红溶液,品红褪色 | 该钠盐一定为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
13. 苯甲酸钠(PhCOONa)是一种常用食品防腐剂。已知25℃,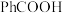 的
的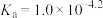 。下列有关PhCOONa溶液说法不正确的是
。下列有关PhCOONa溶液说法不正确的是
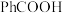 的
的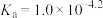 。下列有关PhCOONa溶液说法不正确的是
。下列有关PhCOONa溶液说法不正确的是| A. PhCOONa溶液呈碱性 |
B.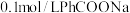 溶液中: 溶液中: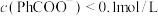 |
C. 25℃, 的 的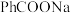 和 和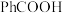 的混合溶液中: 的混合溶液中: |
D.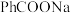 溶液加水稀释时,溶液中 溶液加水稀释时,溶液中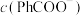 减小 减小 |
您最近一年使用:0次
14. 某温度下,在一恒容密闭容器中进行如下两个反应并达到平衡:
反应I:
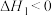
反应II: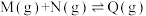

如图是部分组分浓度随时间变化曲线,平衡时M、N浓度相等。该温度下,下列说法不正确的是
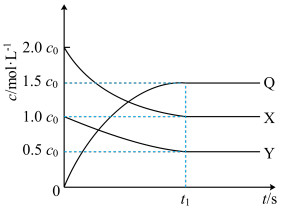
反应I:

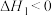
反应II:
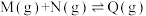

如图是部分组分浓度随时间变化曲线,平衡时M、N浓度相等。该温度下,下列说法不正确的是

A.初始浓度: |
| B.活化能一定有:反应I>反应II |
C.反应I的平衡常数: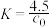 |
D.平衡时的转化率: |
您最近一年使用:0次
单选题
|
适中(0.65)
15. 利用Sonogashira反应机理合成苯乙炔的基本过程如图,其中,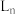 表示配体
表示配体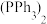
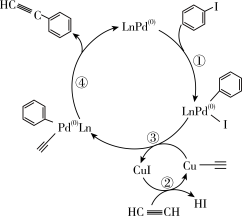
下列叙述错误的是
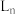 表示配体
表示配体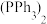

下列叙述错误的是
A.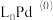 和CuI共同作为该过程的催化剂 和CuI共同作为该过程的催化剂 |
| B.该反应中存在极性键的断裂和形成 |
| C.步骤④过程中,Pd元素被还原 |
| D.该过程的总反应为加成反应 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
16. 全固体薄膜锂离子可充电电池的工作原理是: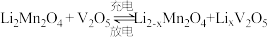 ,下图分别表示全固体薄膜锂离子电池的充放电工作原理。下列说法不正确的是
,下图分别表示全固体薄膜锂离子电池的充放电工作原理。下列说法不正确的是
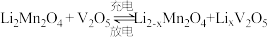 ,下图分别表示全固体薄膜锂离子电池的充放电工作原理。下列说法不正确的是
,下图分别表示全固体薄膜锂离子电池的充放电工作原理。下列说法不正确的是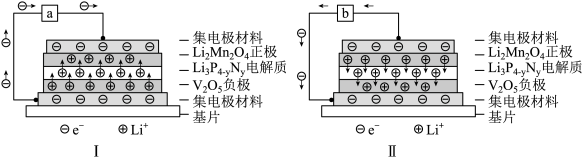
| A.锂离子电池具有质量小、体积小、储存和输出能量大等优点 |
| B.图II为电池放电时的原理图,b处可连接灯泡 |
C.充电时 从 从 材料中脱嵌,经由电解质嵌入到 材料中脱嵌,经由电解质嵌入到 负极中 负极中 |
D.放电时的正极反应式: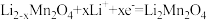 |
您最近一年使用:0次
2022-11-27更新
|
477次组卷
|
4卷引用:广东省百校2022-2023年高三上学期11月联考化学试题
广东省百校2022-2023年高三上学期11月联考化学试题(已下线)仿真卷02-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)浙江省部分学校2025届高三高考模拟化学试题08江西省上饶市广丰区私立康桥中学2024-2025学年高三上学期9月第一次月考化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
17. 为更好地利用化学变化中的物质变化和能量变化,在化学研究和工业生产中还需要关注化学反应的快慢和进行程度等。
(1)研究小组向 溶液中加入
溶液中加入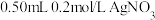 溶液,产生AgCl沉淀,静置,得到AgCl滤液;在AgCl滤液中放入5cm长的镁条后,立即有无色气泡产生,气体可燃,滤液中逐渐出现白色浑浊。
溶液,产生AgCl沉淀,静置,得到AgCl滤液;在AgCl滤液中放入5cm长的镁条后,立即有无色气泡产生,气体可燃,滤液中逐渐出现白色浑浊。
【发现问题】对比发现,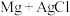 滤液反应比
滤液反应比 反应速率快。研究小组对此实验现象产生的原因进行了探究。
反应速率快。研究小组对此实验现象产生的原因进行了探究。
【查阅资料】 类体积较小的阴离子,能够“钻入”
类体积较小的阴离子,能够“钻入” 膜,达到使其溶解的效果,称作“离子钻入效应”,
膜,达到使其溶解的效果,称作“离子钻入效应”,
【提出猜想】
猜想一: 钻入
钻入 膜形成孔径,增大了
膜形成孔径,增大了 和
和 的接触面积,加快了
的接触面积,加快了 的反应速率;
的反应速率;
猜想二:在“离子钻入效应”基础上, 置换
置换 形成许多微小的
形成许多微小的 原电池,使
原电池,使 反应速率进一步加快。
反应速率进一步加快。
【实验设计】用砂纸擦去镁条表面氧化膜,取表面积和质量相同的镁条(5cm),用浓度分别为 、
、 、
、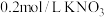 溶液,按照下表进行系列实验,若有沉淀,先将沉淀过滤后,将滤液加入装Mg条的试管,并观察Mg条表面实验现象。
溶液,按照下表进行系列实验,若有沉淀,先将沉淀过滤后,将滤液加入装Mg条的试管,并观察Mg条表面实验现象。
①根据表中信息,补充数据:a=_______ ,b=_______ 。
②由实验1和实验3对比可知: 有加快
有加快 反应速率的作用。
反应速率的作用。
③由实验_______ 和实验_______ 对比可知: 有加快
有加快 反应速率的作用。
反应速率的作用。
【实验结论】猜想一和猜想二成立。
(2)为了进一步证明 原电池能加快
原电池能加快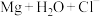 体系中
体系中 的反应速率,研究小组利用数字化实验进行了验证。
的反应速率,研究小组利用数字化实验进行了验证。
【实验设计】选取实验2和实验4两个实验方案,将各实验Mg条、溶液量等比例放大至30cm, ,采集两个实验的
,采集两个实验的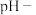 时间、温度-时间变化数据(先采集约10s时溶液的
时间、温度-时间变化数据(先采集约10s时溶液的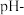 时间、温度-时间数据,再投入Mg条继续采集
时间、温度-时间数据,再投入Mg条继续采集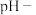 时间、温度-时间数据)。实验数据如图所示:
时间、温度-时间数据)。实验数据如图所示: 数据可知,曲线
数据可知,曲线_______ (填“a”或“b”)表示实验2的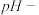 时间变化曲线,请你解释原因
时间变化曲线,请你解释原因_______ 。
⑤在 左右,两实验的
左右,两实验的 变化都明显趋于平缓的原因
变化都明显趋于平缓的原因_______ 。
⑥“温度-时间”曲线分析:两种溶液的初始温度一致,投入镁条后,实验2温度增幅明显大于实验4,说明相同反应时间内,_______ (填“实验2”或“实验4”)放热更多,因此速率更快。
【实验结论2】结合pH-时间、温度-时间曲线可知, 原电池能加快
原电池能加快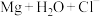 体系中
体系中 的反应速率。
的反应速率。
(1)研究小组向
 溶液中加入
溶液中加入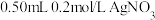 溶液,产生AgCl沉淀,静置,得到AgCl滤液;在AgCl滤液中放入5cm长的镁条后,立即有无色气泡产生,气体可燃,滤液中逐渐出现白色浑浊。
溶液,产生AgCl沉淀,静置,得到AgCl滤液;在AgCl滤液中放入5cm长的镁条后,立即有无色气泡产生,气体可燃,滤液中逐渐出现白色浑浊。【发现问题】对比发现,
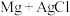 滤液反应比
滤液反应比 反应速率快。研究小组对此实验现象产生的原因进行了探究。
反应速率快。研究小组对此实验现象产生的原因进行了探究。【查阅资料】
 类体积较小的阴离子,能够“钻入”
类体积较小的阴离子,能够“钻入” 膜,达到使其溶解的效果,称作“离子钻入效应”,
膜,达到使其溶解的效果,称作“离子钻入效应”,【提出猜想】
猜想一:
 钻入
钻入 膜形成孔径,增大了
膜形成孔径,增大了 和
和 的接触面积,加快了
的接触面积,加快了 的反应速率;
的反应速率;猜想二:在“离子钻入效应”基础上,
 置换
置换 形成许多微小的
形成许多微小的 原电池,使
原电池,使 反应速率进一步加快。
反应速率进一步加快。【实验设计】用砂纸擦去镁条表面氧化膜,取表面积和质量相同的镁条(5cm),用浓度分别为
 、
、 、
、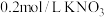 溶液,按照下表进行系列实验,若有沉淀,先将沉淀过滤后,将滤液加入装Mg条的试管,并观察Mg条表面实验现象。
溶液,按照下表进行系列实验,若有沉淀,先将沉淀过滤后,将滤液加入装Mg条的试管,并观察Mg条表面实验现象。| 实验序号 |
| 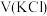  | 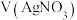  | 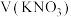  | 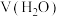  | 实验现象 |
| 1 | / | / | / | 5.00 | 微小气泡附着 | |
| 2 | 4.50 | 0.50 | / | / | 大量气泡放出 | |
| 3 | 4.50 | / | / | 0.50 | 少量气泡放出 | |
| 4 | a | / | b | / | 少量气泡放出 |
②由实验1和实验3对比可知:
 有加快
有加快 反应速率的作用。
反应速率的作用。③由实验
 有加快
有加快 反应速率的作用。
反应速率的作用。【实验结论】猜想一和猜想二成立。
(2)为了进一步证明
 原电池能加快
原电池能加快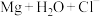 体系中
体系中 的反应速率,研究小组利用数字化实验进行了验证。
的反应速率,研究小组利用数字化实验进行了验证。【实验设计】选取实验2和实验4两个实验方案,将各实验Mg条、溶液量等比例放大至30cm,
 ,采集两个实验的
,采集两个实验的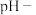 时间、温度-时间变化数据(先采集约10s时溶液的
时间、温度-时间变化数据(先采集约10s时溶液的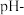 时间、温度-时间数据,再投入Mg条继续采集
时间、温度-时间数据,再投入Mg条继续采集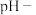 时间、温度-时间数据)。实验数据如图所示:
时间、温度-时间数据)。实验数据如图所示: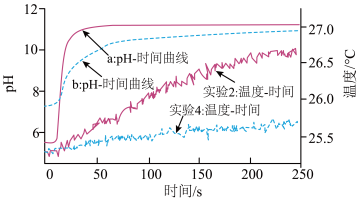
 数据可知,曲线
数据可知,曲线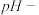 时间变化曲线,请你解释原因
时间变化曲线,请你解释原因⑤在
 左右,两实验的
左右,两实验的 变化都明显趋于平缓的原因
变化都明显趋于平缓的原因⑥“温度-时间”曲线分析:两种溶液的初始温度一致,投入镁条后,实验2温度增幅明显大于实验4,说明相同反应时间内,
【实验结论2】结合pH-时间、温度-时间曲线可知,
 原电池能加快
原电池能加快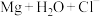 体系中
体系中 的反应速率。
的反应速率。
【知识点】 原电池原理对化学反应速率的影响解读
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
18. 铈(Ce)是一种应用广泛的稀土元素,从氟碳铈矿(主要含CeFCO3、Fe2O3、SiO2)和天青石(主要含SrSO4、并含有少量Ba、Ca等杂质)伴生矿中回收铈,同时生产高纯碳酸锶(SrCO3)的一种生产工艺流程如图:
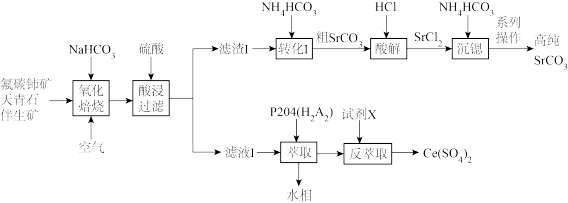
已知:①铈的常见价态是+3和+4价;
②碳酸氢铵受热易分解
(1)① 中Ce的化合价为
中Ce的化合价为_______ ;
②“氧化焙烧”时,Ce元素转化为CeO2,F元素转化为NaF,该过程中氧化剂与还原剂的物质的量之比为_______ 。
(2)焙烧温度是影响浸出率的关键因素之一,下图为不同焙烧温度对Ce和Sr浸出率的影响。
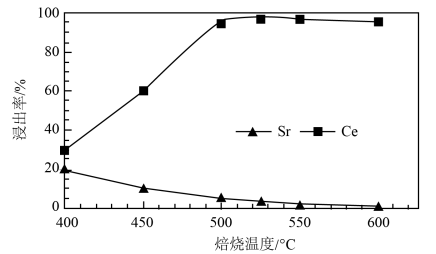
结合实际生产可知,“氧化焙烧”步骤应控制焙烧温度为_______ ,原因为_______ 。
(3)“沉锶”步骤中发生的离子反应方程式:_______ 。
(4)“萃取”步骤的原理为: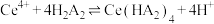 ,则试剂X为
,则试剂X为_______ 。

已知:①铈的常见价态是+3和+4价;
②碳酸氢铵受热易分解
(1)①
 中Ce的化合价为
中Ce的化合价为②“氧化焙烧”时,Ce元素转化为CeO2,F元素转化为NaF,该过程中氧化剂与还原剂的物质的量之比为
(2)焙烧温度是影响浸出率的关键因素之一,下图为不同焙烧温度对Ce和Sr浸出率的影响。

结合实际生产可知,“氧化焙烧”步骤应控制焙烧温度为
(3)“沉锶”步骤中发生的离子反应方程式:
(4)“萃取”步骤的原理为:
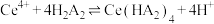 ,则试剂X为
,则试剂X为
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
19. 甲醇(CH3OH)是一种基础有机化工原料,将成为21世纪具有竞争力的清洁燃料之一,下面是利用工业废气CO2为碳源合成甲醇的反应原理。
①
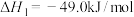
②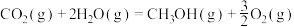
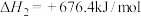
③
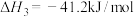
④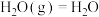 (1)
(1) 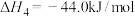
(1)写出表示 燃烧热的热化学反应方程式
燃烧热的热化学反应方程式_______ 。
(2)某实验室控制 和
和 初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
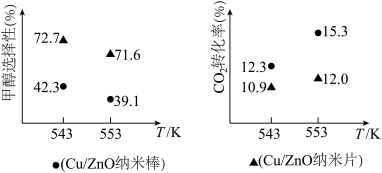
根据上述材料,请你选择合成甲醇的最佳条件_______ 。温度553K,选择催化剂II时,CO2的转化率12.0%是不是该状态下平衡转化率?_______ (填“是”或“不是”),原因是_______ 。
(3)针对反应①,下列说法正确的是_______。
(4)控制温度553K,向一定体积的刚性容器中投入 和
和 发生反应①、②、③,达到平衡时,容器内的气体压强为
发生反应①、②、③,达到平衡时,容器内的气体压强为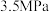 ,平衡时
,平衡时 的转化率为80%,
的转化率为80%, 的选择性为50%,生成
的选择性为50%,生成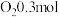 ,则反应①的分压平衡常数
,则反应①的分压平衡常数
_______ 。(已知:分压=组分物质的量分数×总压,甲醇的选择性 )
)
①

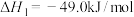
②
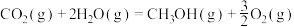
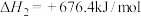
③

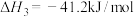
④
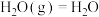 (1)
(1) 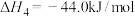
(1)写出表示
 燃烧热的热化学反应方程式
燃烧热的热化学反应方程式(2)某实验室控制
 和
和 初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
根据上述材料,请你选择合成甲醇的最佳条件
(3)针对反应①,下列说法正确的是_______。
| A.压缩容器体积,正反应速率和逆反应速率都增大 |
B.升高温度, 的转化率一定增大 的转化率一定增大 |
C.选用合适的催化剂可提高 的生产效率 的生产效率 |
D.增大 和 和 的初始投料比可提高 的初始投料比可提高 的转化率 的转化率 |
 和
和 发生反应①、②、③,达到平衡时,容器内的气体压强为
发生反应①、②、③,达到平衡时,容器内的气体压强为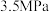 ,平衡时
,平衡时 的转化率为80%,
的转化率为80%, 的选择性为50%,生成
的选择性为50%,生成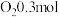 ,则反应①的分压平衡常数
,则反应①的分压平衡常数
 )
)
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
20. 甲醛是甲醇的氧化产物,对人体有较大损害。空气中甲醛的去除一直是研究的热点问题, 、
、 、
、 等对甲醛都有较好的催化氧化作用。回答下列问题:
等对甲醛都有较好的催化氧化作用。回答下列问题:
(1) 中σ键和π键个数比为
中σ键和π键个数比为_______ ,甲醛的VSEPR模型为_______ 。
(2)分子内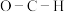 的键角:甲醇
的键角:甲醇_______ 甲醛(填“>”或“<”或“=”)。
(3)基态 和
和 中价电子层的成对电子对之比是
中价电子层的成对电子对之比是_______ 。
(4)甲醛常温下为气态,而甲醇为液态,原因是_______ 。
(5) 的晶胞结构如图所示,与O原子距离最短的Ce原子的数目是
的晶胞结构如图所示,与O原子距离最短的Ce原子的数目是_______ 。若该立方晶胞参数为apm,X与Y的核间距最小为_______ pm。
 、
、 、
、 等对甲醛都有较好的催化氧化作用。回答下列问题:
等对甲醛都有较好的催化氧化作用。回答下列问题:(1)
 中σ键和π键个数比为
中σ键和π键个数比为(2)分子内
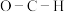 的键角:甲醇
的键角:甲醇(3)基态
 和
和 中价电子层的成对电子对之比是
中价电子层的成对电子对之比是(4)甲醛常温下为气态,而甲醇为液态,原因是
(5)
 的晶胞结构如图所示,与O原子距离最短的Ce原子的数目是
的晶胞结构如图所示,与O原子距离最短的Ce原子的数目是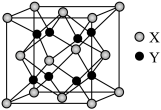
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
21. 毛兰素是天然石斛中最重要的成分之一,具有抗氧化、抑制血管生成和抑制肿瘤生长等多种药理作用。毛兰素F的一种化学合成路线如下(部分反应条件已省略):

已知: +
+

 +H2O
+H2O
回答下列问题:
(1)A的结构简式为_______ ,A→B的目的是_______ 。
(2)B中含氧官能团的名称:_______ 。
(3)D→E的反应类型为_______ 。
(4)同时满足下列条件的B的同分异构体有多种:
a.苯环上有4个取代基的单环化合物,且Cl原子直接连在苯环上
b.能发生银镜反应,不含酯基和醚键
c.滴加FeCl3溶液不显紫色
写出其中核磁共振氢谱有四组峰,峰面积之比为4:2:2:1的结构简式(任写一种):_______ 。
(5)根据上述信息,设计由 、
、 和三甲基硅重氮甲烷为原料,制备
和三甲基硅重氮甲烷为原料,制备 的合成路线(无机试剂任选)。
的合成路线(无机试剂任选)。_______

已知:
 +
+

 +H2O
+H2O回答下列问题:
(1)A的结构简式为
(2)B中含氧官能团的名称:
(3)D→E的反应类型为
(4)同时满足下列条件的B的同分异构体有多种:
a.苯环上有4个取代基的单环化合物,且Cl原子直接连在苯环上
b.能发生银镜反应,不含酯基和醚键
c.滴加FeCl3溶液不显紫色
写出其中核磁共振氢谱有四组峰,峰面积之比为4:2:2:1的结构简式(任写一种):
(5)根据上述信息,设计由
 、
、 和三甲基硅重氮甲烷为原料,制备
和三甲基硅重氮甲烷为原料,制备 的合成路线(无机试剂任选)。
的合成路线(无机试剂任选)。
您最近一年使用:0次
试卷分析
导出
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、认识化学科学、有机化学基础、化学反应原理、化学实验基础、物质结构与性质
试卷题型(共 21题)
题型
数量
单选题
16
解答题
5
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 二氧化硅的用途 硅酸盐工业 化学科学对人类文明发展的意义 | |
| 2 | 0.65 | 氧化还原反应在生活、生产中的应用 生活中常见的几种醇 蛋白质的变性 新型有机高分子材料 | |
| 3 | 0.94 | 硅的物理性质与用途 金属的防护 新型有机高分子材料 金属与合金性能比较 | |
| 4 | 0.85 | 化学用语综合判断 有机物的结构式、结构简式、比例模型、球棍模型、最简式 共价型分子结构式、电子式 有机物结构的表示方法 | |
| 5 | 0.85 | 氨气的实验室制法 测定某些反应的反应速率 淀粉水解及其产物检验相关实验 萃取和分液 | |
| 6 | 0.94 | 有机反应类型 有机官能团的性质及结构 分子的手性 有机分子中原子共面的判断 | |
| 7 | 0.85 | 物质的转化 氯气的实验室制法 | |
| 8 | 0.65 | Fe2+的鉴别及其应用 电镀 油脂在碱性条件下水解 简单配合物的成键 | |
| 9 | 0.65 | 22.4L/mol适用条件 结合物质结构基础知识与NA相关推算 同主族元素性质递变规律理解及应用 | |
| 10 | 0.65 | 离子方程式的正误判断 硝酸的强氧化性 二氧化硫与其他强氧化剂的反应 盐类水解在生活、生产中的应用 | |
| 11 | 0.65 | 元素金属性与非金属性递变规律的理解及应用 元素非金属性强弱的比较方法 微粒半径大小的比较方法 | |
| 12 | 0.65 | 温度对化学平衡移动的影响 盐类水解规律理解及应用 元素非金属性强弱的比较方法 化学实验探究 | |
| 13 | 0.65 | 电离平衡常数及影响因素 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 盐的水解常数 | |
| 14 | 0.65 | 化学平衡图像分析 化学平衡常数的有关计算 转化率的相关计算及判断 化学平衡题中基于图表数据的相关计算 | |
| 15 | 0.65 | 催化剂对化学反应速率的影响 取代反应 化学键与化学反应本质联系 共价键概念及判断 | |
| 16 | 0.65 | 原电池原理理解 原电池电极反应式书写 新型电池 原电池、电解池综合考查 | |
| 二、解答题 | |||
| 17 | 0.65 | 原电池原理对化学反应速率的影响 | 实验探究题 |
| 18 | 0.65 | 氧化还原反应方程式的配平 化学反应条件的控制及其应用 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 19 | 0.65 | 盖斯定律及其有关计算 化学平衡的移动及其影响因素 化学平衡图像分析 化学平衡常数的有关计算 | 原理综合题 |
| 20 | 0.65 | 电子排布式 利用杂化轨道理论判断分子的空间构型 晶胞的有关计算 | 结构与性质 |
| 21 | 0.4 | 酯的水解反应机理 逆合成分析法 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |