解题方法
1 . 化学与生活紧密相关,下列与化学知识有关的描述正确的是
| A.小苏打可用作食品膨松剂,利用其水溶液呈碱性 |
B. 可用于饮用水消毒,利用了其强氧化性 可用于饮用水消毒,利用了其强氧化性 |
C. 用于制作光导纤维,利用了其半导体的特性 用于制作光导纤维,利用了其半导体的特性 |
| D.镁铝合金用于制作航天器外壳,利用了其强还原性 |
您最近一年使用:0次
名校
解题方法
2 . 高铁酸钾 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是| A.氢氧化铁胶体具有碱性,可用于净水 |
B. 具有氧化性,可作为特定环境中的抗氧化剂 具有氧化性,可作为特定环境中的抗氧化剂 |
| C.高铁酸钾能溶于水,水溶液呈紫色,可作氧化剂 |
| D.氧化铁呈红棕色且遮盖效果好,可用作红色颜料 |
您最近一年使用:0次
2023-12-31更新
|
253次组卷
|
2卷引用:江苏省南通市名校联盟2024届高三上学期12月学业质量联合监测化学试卷
3 . 生物质铁炭纳米材料可以活化过一硫酸盐,降解废水中有机污染物.
(1)生物质铁炭纳米材料活化过—硫酸钾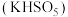 降解有机污染物的反应历程如图-1所示.图中
降解有机污染物的反应历程如图-1所示.图中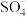 和
和 分别表示硫酸根自由基和羟基自由基.
分别表示硫酸根自由基和羟基自由基. (S的化合价为
(S的化合价为 )在水中的电离过程为:
)在水中的电离过程为: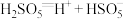 、
、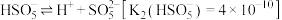 .写出
.写出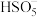 的结构式:
的结构式:_______ 。
②生物质铁炭纳米材料降解有机污染物的机理可描述为______ 。
③若有机污染物为苯酚,写出酸性条件下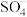 与苯酚反应的化学方程式:
与苯酚反应的化学方程式:______ 。
(2)与直接使用纳米铁颗粒相比,使用生物质铁炭纳米材料降解的优点是:______ 。
(3)铁炭纳米材料在不同 对有机污染物去除率(
对有机污染物去除率( 溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示,
溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示, 越小有机污染物去除率越高的原因是:
越小有机污染物去除率越高的原因是:______ 。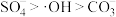 。水中存在一定量
。水中存在一定量 和无
和无 存在时对铁炭纳米材料降解有机污染物的影响如图-3所示.
存在时对铁炭纳米材料降解有机污染物的影响如图-3所示. 的存在对有机污染物的降解有影响,原因是:
的存在对有机污染物的降解有影响,原因是:______ 。
(1)生物质铁炭纳米材料活化过—硫酸钾
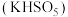 降解有机污染物的反应历程如图-1所示.图中
降解有机污染物的反应历程如图-1所示.图中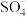 和
和 分别表示硫酸根自由基和羟基自由基.
分别表示硫酸根自由基和羟基自由基.
 (S的化合价为
(S的化合价为 )在水中的电离过程为:
)在水中的电离过程为: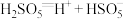 、
、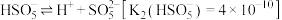 .写出
.写出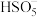 的结构式:
的结构式:②生物质铁炭纳米材料降解有机污染物的机理可描述为
③若有机污染物为苯酚,写出酸性条件下
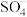 与苯酚反应的化学方程式:
与苯酚反应的化学方程式:(2)与直接使用纳米铁颗粒相比,使用生物质铁炭纳米材料降解的优点是:
(3)铁炭纳米材料在不同
 对有机污染物去除率(
对有机污染物去除率( 溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示,
溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示, 越小有机污染物去除率越高的原因是:
越小有机污染物去除率越高的原因是: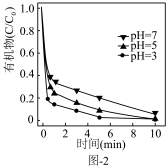
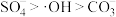 。水中存在一定量
。水中存在一定量 和无
和无 存在时对铁炭纳米材料降解有机污染物的影响如图-3所示.
存在时对铁炭纳米材料降解有机污染物的影响如图-3所示. 的存在对有机污染物的降解有影响,原因是:
的存在对有机污染物的降解有影响,原因是: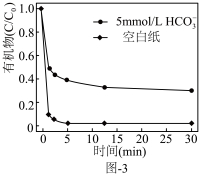
您最近一年使用:0次
名校
4 . 研究有机物的结构和性质对生产生活意义深远。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。___________ ,B物质的分子式为:___________ 。
(2)按官能团分类,D所属的类别是___________ 。
(3)1molE与足量的金属钠反应产生___________ L氢气(标况下)。
(4)实验室制取C的化学方程式___________ 。
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。___________ (填名称)。
(6)脱氢维生素C中,键角①___________ 键角②(填“>”、“=”或“<”)。
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是___________ 。
(8)标出维生素C中所有的手性碳原子(用*标注)___________ 。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。A. 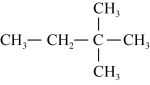 B.
B. 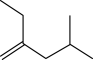 C.
C. D.
D. 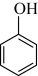 E.
E.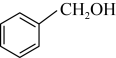
(2)按官能团分类,D所属的类别是
(3)1molE与足量的金属钠反应产生
(4)实验室制取C的化学方程式
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。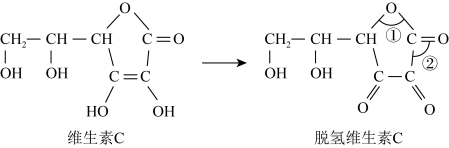
(6)脱氢维生素C中,键角①
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是
(8)标出维生素C中所有的手性碳原子(用*标注)
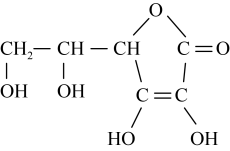
您最近一年使用:0次
解题方法
5 . 化学与科技、生活密切相关,下列说法正确的是
| A.75%的乙醇与84消毒液都具有强氧化性,可以杀菌消毒 |
| B.食品中常放一个包装袋,装有的硅胶、生石灰、还原铁粉等物质均为抗氧化剂 |
| C.我国空间站上使用大量高性能氮化硼陶瓷,氮化硼为分子晶体 |
D.将水果放在浸泡过 的硅藻土中运输,可以防止水果过熟变质 的硅藻土中运输,可以防止水果过熟变质 |
您最近一年使用:0次
6 .  的治理是当前生态环境保护中的重要课题之一,回答下列问题:
的治理是当前生态环境保护中的重要课题之一,回答下列问题:
(1)氮元素的常见单质有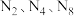 。
。 中原子之间只形成
中原子之间只形成 键,且均达到最外层8电子稳定结构,
键,且均达到最外层8电子稳定结构, 的结构式为
的结构式为______________ *.
(2) 催化还原
催化还原 ,保持其它初始条件不变,使用甲、乙催化剂时,
,保持其它初始条件不变,使用甲、乙催化剂时, 转化率随温度的变化如图1所示。
转化率随温度的变化如图1所示。 点对应的速率
点对应的速率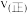
______________ 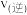 (填“>”“<”或“=”).
(填“>”“<”或“=”).

(3)将含 和
和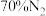 的混合气体以一定流速通过装有催化剂的反应器,发生反应:
的混合气体以一定流速通过装有催化剂的反应器,发生反应: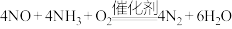 。
。 去除率随反应温度变化如图2所示.在
去除率随反应温度变化如图2所示.在 范围内,
范围内, 去除率随温度的升高而迅速上升的主要原因是
去除率随温度的升高而迅速上升的主要原因是______________ 。
(4)电解氧化吸收法可将废气中的 转变为硝态氮。向
转变为硝态氮。向 溶液(起始
溶液(起始 调至9)中通入
调至9)中通入 ,电解产生的
,电解产生的 将
将 氧化为
氧化为 ,从而实现
,从而实现 的去除.电解过程中测得溶液中相关成分的浓度变化与电流强度的关系如图3所示。
的去除.电解过程中测得溶液中相关成分的浓度变化与电流强度的关系如图3所示。
已知氧化性: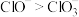 ;
;
①电解液中 氧化
氧化 的离子方程式为
的离子方程式为______________ 。
②电流强度大于 后,随电流强度的增加,
后,随电流强度的增加, 去除率
去除率______________ (填“上升”“下降”或“不变”),原因是______________ 。

 的治理是当前生态环境保护中的重要课题之一,回答下列问题:
的治理是当前生态环境保护中的重要课题之一,回答下列问题:(1)氮元素的常见单质有
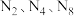 。
。 中原子之间只形成
中原子之间只形成 键,且均达到最外层8电子稳定结构,
键,且均达到最外层8电子稳定结构, 的结构式为
的结构式为(2)
 催化还原
催化还原 ,保持其它初始条件不变,使用甲、乙催化剂时,
,保持其它初始条件不变,使用甲、乙催化剂时, 转化率随温度的变化如图1所示。
转化率随温度的变化如图1所示。 点对应的速率
点对应的速率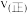
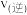 (填“>”“<”或“=”).
(填“>”“<”或“=”).
(3)将含
 和
和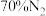 的混合气体以一定流速通过装有催化剂的反应器,发生反应:
的混合气体以一定流速通过装有催化剂的反应器,发生反应: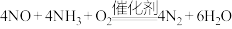 。
。 去除率随反应温度变化如图2所示.在
去除率随反应温度变化如图2所示.在 范围内,
范围内, 去除率随温度的升高而迅速上升的主要原因是
去除率随温度的升高而迅速上升的主要原因是(4)电解氧化吸收法可将废气中的
 转变为硝态氮。向
转变为硝态氮。向 溶液(起始
溶液(起始 调至9)中通入
调至9)中通入 ,电解产生的
,电解产生的 将
将 氧化为
氧化为 ,从而实现
,从而实现 的去除.电解过程中测得溶液中相关成分的浓度变化与电流强度的关系如图3所示。
的去除.电解过程中测得溶液中相关成分的浓度变化与电流强度的关系如图3所示。已知氧化性:
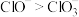 ;
;①电解液中
 氧化
氧化 的离子方程式为
的离子方程式为②电流强度大于
 后,随电流强度的增加,
后,随电流强度的增加, 去除率
去除率
您最近一年使用:0次
7 . 化学与生活、科技、社会、环境密切相关。下列说法正确的是
| A.激光打印机的墨粉中含有四氧化三铁,该氧化物的颜色为红色 |
| B.浓硝酸与铁在常温下不能反应,所以可用铁质容器储运浓硝酸 |
| C.汽车尾气是把氮的氧化物催化还原为氮气 |
| D.水果罐头中常加入维生素C作抗氧化剂是由于其具有氧化性 |
您最近一年使用:0次
名校
8 . 碘量法测定维生素C的含量
利用I2的氧化性,以I2溶液为滴定剂进行分析的方法,称为直接碘量法。某研究小组用碘量法测定维生素C样品中维生素C 的含量并撰写如下实验报告。
碘量法测定维生素C的含量
实验目的:利用碘量法测定维生素C样品中维生素C的含量
实验原理:C6H8O6(维生素C)+I2=C6H6O6+2HI, 。
。
已知:维生素C样品中其余成分不与I2反应。
实验步骤:
①初配浓度约为0.0500mol·L-1的I2溶液
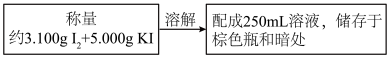
②准确配制0.1000mol·L-1的Na2S2O3溶液
③准确标定I2标准液的准确浓度
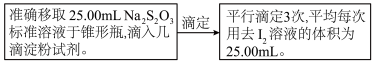
④测定维生素C的含量
每次测定时称维生素C样品2.000g于洁净锥形瓶中,加入室温除氧蒸馏水100.00mL、2.000mol·L-1的CH3COOH溶液10.00mL以调节pH,摇动溶解完全,加淀粉指示剂,摇匀,立即用I2标准溶液滴定到滴定终点,平行滴定3份,平均每份用去标准I2液90.00 mL。
⑤计算维生素C的质量分数
回答问题。
(1)本实验中无需用到的定量仪器是_______ 。
(2)已知I2+I-
 ,I2微溶于水,则配制I2溶液时,结合平衡移动原理解释加入KI的目的是
,I2微溶于水,则配制I2溶液时,结合平衡移动原理解释加入KI的目的是___________ 。
(3)标准I2溶液的准确浓度是________ (保留3位小数)。
(4)溶解维生素C样品时,要用新煮沸并冷却到室温的蒸馏水的原因是_______ ,直接用常温下未煮沸的蒸馏水溶解样品,则会使得测定结果________ (选填“偏大”、“偏小”或“无影响”)。溶解维生素C样品时,加入CH3COOH 的作用是_________ 。
(5)标准I2溶液滴定维生素C样品,确定滴定终点的现象是_________ 。维生素C样品中维生素C的质量分数为________ 。
(6)碘离子易与氧气发生反应:4I-+O2+4H+=2I2+2H2O。若用保存较久的标准I2溶液来滴定,则会使得最终测定的维生素C的质量分数_______ (选填“偏大”、“偏小”或“无影响”)。
利用I2的氧化性,以I2溶液为滴定剂进行分析的方法,称为直接碘量法。某研究小组用碘量法测定维生素C样品中维生素C 的含量并撰写如下实验报告。
碘量法测定维生素C的含量
实验目的:利用碘量法测定维生素C样品中维生素C的含量
实验原理:C6H8O6(维生素C)+I2=C6H6O6+2HI,
 。
。已知:维生素C样品中其余成分不与I2反应。
实验步骤:
①初配浓度约为0.0500mol·L-1的I2溶液

②准确配制0.1000mol·L-1的Na2S2O3溶液
③准确标定I2标准液的准确浓度

④测定维生素C的含量
每次测定时称维生素C样品2.000g于洁净锥形瓶中,加入室温除氧蒸馏水100.00mL、2.000mol·L-1的CH3COOH溶液10.00mL以调节pH,摇动溶解完全,加淀粉指示剂,摇匀,立即用I2标准溶液滴定到滴定终点,平行滴定3份,平均每份用去标准I2液90.00 mL。
⑤计算维生素C的质量分数
回答问题。
(1)本实验中无需用到的定量仪器是
 |  |  |  |
| A.电子天平 | B.滴定管 | C.250mL容量瓶 | D.温度计 |
(2)已知I2+I-

 ,I2微溶于水,则配制I2溶液时,结合平衡移动原理解释加入KI的目的是
,I2微溶于水,则配制I2溶液时,结合平衡移动原理解释加入KI的目的是(3)标准I2溶液的准确浓度是
(4)溶解维生素C样品时,要用新煮沸并冷却到室温的蒸馏水的原因是
(5)标准I2溶液滴定维生素C样品,确定滴定终点的现象是
(6)碘离子易与氧气发生反应:4I-+O2+4H+=2I2+2H2O。若用保存较久的标准I2溶液来滴定,则会使得最终测定的维生素C的质量分数
您最近一年使用:0次
名校
9 . 下列关于物质的性质对应用途的说法错误的是
A.高铁酸钾 具有强氧化性,能杀菌消毒,所以可以用作消毒剂 具有强氧化性,能杀菌消毒,所以可以用作消毒剂 |
B. 具有很强的毒性,所以不能用于自来水的杀菌消毒 具有很强的毒性,所以不能用于自来水的杀菌消毒 |
C. 溶液显血红色,所以可以在影视剧中用作替代血液的道具 溶液显血红色,所以可以在影视剧中用作替代血液的道具 |
| D.钛合金因为其生物相容性好,所以可以用作人造骨骼 |
您最近一年使用:0次
2024-02-20更新
|
137次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一上学期1月期末化学试题
10 . 重铬酸钾(K2Cr2O7)和铬酸钾(K2CrO4)应用广泛,下列说法不正确的是
| A.Cr位于元素周期表d区,最外层电子数为1 |
| B.K2CrO4属于强电解质 |
| C.酸性K2Cr2O7溶液可将乙醇氧化为乙酸 |
| D.K2CrO4在碱性溶液中可转化为K2Cr2O7 |
您最近一年使用:0次



