解题方法
1 . 如图所示,某小组同学拟用如图仪器,在实验室中制备干燥、纯净的氯气。请完成下列空白。
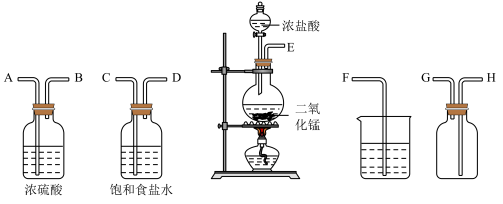
(1)上述仪器正确连接后应进行的操作是___________ 。
(2)实验室制备氯气反应的化学方程式是___________ ,检验反应结束后的溶液中是否有Cl-的方法是:___________ 。
(3)饱和食盐水的作用是___________ ,浓硫酸的作用是___________ ,为防止污染空气,实验时如图烧杯所盛溶液化学式为___________ 。
(4)下列说法正确的是___________(填字母)。

(1)上述仪器正确连接后应进行的操作是
(2)实验室制备氯气反应的化学方程式是
(3)饱和食盐水的作用是
(4)下列说法正确的是___________(填字母)。
| A.铁丝在少量的Cl2中燃烧可生成FeCl2 |
| B.液氯是氯气的水溶液,它能使干燥的有色布条褪色 |
| C.氯水中含有次氯酸,氯水具有杀菌、漂白作用 |
| D.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰 |
您最近一年使用:0次
2 . NaCl是一种化工原料,可以制备多种物质,如下图所示。其中,常温常压下A为黄绿色的气态单质。根据图示的转化关系填空:

(1)请写出结构图中A、B、C、D对应的化学物质:
A:___________ ,B:___________ ,C:___________ 。
(2)纯净的H2在A中反应的化学方程式为___________ 。
(3)实验室中,为了防止金属 变质,常将其保存在
变质,常将其保存在___________ 中,若将金属 久置于空气中最终会转变为
久置于空气中最终会转变为___________ (填化学式)。
(4)下列表述中,金属Na在MgSO4溶液中可能出现的反应现象的是___________。

(1)请写出结构图中A、B、C、D对应的化学物质:
A:
(2)纯净的H2在A中反应的化学方程式为
(3)实验室中,为了防止金属
 变质,常将其保存在
变质,常将其保存在 久置于空气中最终会转变为
久置于空气中最终会转变为(4)下列表述中,金属Na在MgSO4溶液中可能出现的反应现象的是___________。
| A.有气泡生成,钠熔化成小球 | B.钠在液面上四处游动 |
| C.溶液中有银白色金属生成 | D.溶液变浑浊 |
您最近一年使用:0次
名校
解题方法
3 . 某同学设计如图装置进行卤素的性质实验,玻璃管内装有分别滴了不同溶液的棉球,并向其中通入足量的氯气。下列实验现象预测合理的是


| A.①处棉球最终变成无色 | B.②处棉球最终变成红色 |
| C.③处棉球无明显变化 | D.④处棉球先变蓝后褪色 |
您最近一年使用:0次
4 . 如图是氯元素常见物质的“价―类”二维图,f和g为钠盐,下列推断不合理 的是

| A.一定条件下,a与f,a与g均可生成b | B.f溶液的酸碱性可用pH试纸测定 |
| C.c溶于水能生成e,c是酸性氧化物 | D.可存在a→b→d→f→b→a的转化关系 |
您最近一年使用:0次
2024-03-09更新
|
264次组卷
|
3卷引用:湖南省 长沙市周南实验中学2023-2024学年高一下学期第一次月考化学试题
解题方法
5 . 已知实验室常用MnO2粉末和浓盐酸制取Cl2,其反应的化学方程式为: 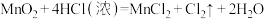 。请回答下列问题:
。请回答下列问题:
(1)如图为Cl2的发生装置,仪器a的名称___________ ,a中盛放的试剂为___________ 。
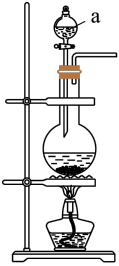
(2)如图为Cl2的收集及尾气处理装置。

①一段时间后,可观察到集气瓶中气体颜色变为___________ 。
A.红棕色 B.黄绿色
②该气体收集方法为___________ 。
A.向上排空气法 B.向下排空气法
③烧杯中NaOH溶液的作用是___________ 。
(3)欲制得标准状况下2.24LCl2,至少需要MnO2的质量为___________ g。
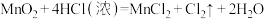 。请回答下列问题:
。请回答下列问题:(1)如图为Cl2的发生装置,仪器a的名称

(2)如图为Cl2的收集及尾气处理装置。

①一段时间后,可观察到集气瓶中气体颜色变为
A.红棕色 B.黄绿色
②该气体收集方法为
A.向上排空气法 B.向下排空气法
③烧杯中NaOH溶液的作用是
(3)欲制得标准状况下2.24LCl2,至少需要MnO2的质量为
您最近一年使用:0次
名校
解题方法
6 . 某小组设计实验探究氯气的性质,装置如图所示:
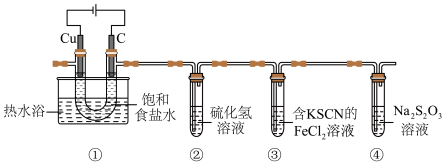
实验中观察到③中溶液先变红色,后褪色。
资料显示:④中反应为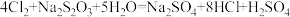
下到叙述错误的是

实验中观察到③中溶液先变红色,后褪色。
资料显示:④中反应为
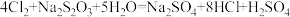
下到叙述错误的是
A.铜极附近逸出气泡,其溶液 升高 升高 |
| B.②中溶液变浑浊,可推知氯的非金属性比硫的强 |
C.取③中溶液,滴加 溶液可判断 溶液可判断 是否被氧化 是否被氧化 |
D.用硝酸酸化的 溶液可验证④中是否生成了 溶液可验证④中是否生成了 |
您最近一年使用:0次
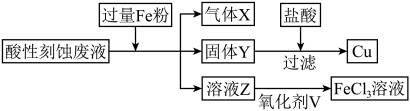
7 . 电子工业中常用 溶液作刻蚀液将覆铜板上不需要的
溶液作刻蚀液将覆铜板上不需要的 腐蚀,某兴趣小组欲回收利用酸性刻蚀废液(含
腐蚀,某兴趣小组欲回收利用酸性刻蚀废液(含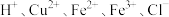 等)中的
等)中的 和
和 ,设计了如下流程。下列说法错误的是
,设计了如下流程。下列说法错误的是
 溶液作刻蚀液将覆铜板上不需要的
溶液作刻蚀液将覆铜板上不需要的 腐蚀,某兴趣小组欲回收利用酸性刻蚀废液(含
腐蚀,某兴趣小组欲回收利用酸性刻蚀废液(含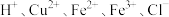 等)中的
等)中的 和
和 ,设计了如下流程。下列说法错误的是
,设计了如下流程。下列说法错误的是
A.氧化剂V可以选择 或盐酸酸化的 或盐酸酸化的 |
| B.固体Y与盐酸反应过滤得到的母液可以合并到溶液Z中以提高利用率 |
C.向溶液Z中加入 溶液,溶液变红 溶液,溶液变红 |
D.气体X与 反应得到的产物与 反应得到的产物与 粉在高温下可以反应生成气体 粉在高温下可以反应生成气体 和 和 |
您最近一年使用:0次
名校
8 . I.铝土矿是工业上制备金属铝的主要原料,其主要成分是 ,同时还含有
,同时还含有 、
、 。工业上可使用碱浸法提取铝土矿中的
。工业上可使用碱浸法提取铝土矿中的 ,其工业流程如图所示。根据图示信息,请回答下列问题:
,其工业流程如图所示。根据图示信息,请回答下列问题:_______ ,滤渣B的主要成分是_______ (填化学式)。
(2)实验室中进行煅烧时最适合用来盛放 固体的实验仪器名称是
固体的实验仪器名称是_______ 。
(3)用 与C、
与C、 在高温条件下反应可制取
在高温条件下反应可制取 ,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是
,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是_______ 。
Ⅱ.高铁酸钾( )具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程:
)具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程: 的部分性质如下:
的部分性质如下:
(4)写出①中发生的离子方程式:_______ 。
(5)②中加入NaOH固体的目的是_______ (填字母序号)
A.加入NaOH固体做氧化剂
B.为后续反应提供碱性环境
C.NaOH固体溶解时会放出较多的热量,有利于后续生成
(6)完成④中反应的离子方程式:_______ 。
(7)⑥中洗涤时,洗涤剂最好选用_______(填字母序号)。
(8)现取洗涤并干燥后 样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为_______ 。(计算结果保留到0.1%)
 ,同时还含有
,同时还含有 、
、 。工业上可使用碱浸法提取铝土矿中的
。工业上可使用碱浸法提取铝土矿中的 ,其工业流程如图所示。根据图示信息,请回答下列问题:
,其工业流程如图所示。根据图示信息,请回答下列问题: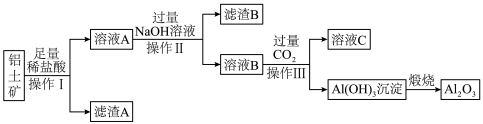
(2)实验室中进行煅烧时最适合用来盛放
 固体的实验仪器名称是
固体的实验仪器名称是(3)用
 与C、
与C、 在高温条件下反应可制取
在高温条件下反应可制取 ,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是
,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是Ⅱ.高铁酸钾(
 )具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程:
)具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程: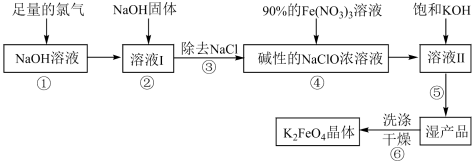
 的部分性质如下:
的部分性质如下:溶解性 | 溶于水,微溶于浓KOH溶液,难溶于有机物 |
稳定性 | 温度为0~5℃或强碱性溶液中能稳定存在;酸性或中性溶液中Fe变为+3价并放出 |
(4)写出①中发生的离子方程式:
(5)②中加入NaOH固体的目的是
A.加入NaOH固体做氧化剂
B.为后续反应提供碱性环境
C.NaOH固体溶解时会放出较多的热量,有利于后续生成

(6)完成④中反应的离子方程式:
(7)⑥中洗涤时,洗涤剂最好选用_______(填字母序号)。
A. | B.KOH溶液 | C.异丙醇 | D. 溶液 溶液 |
(8)现取洗涤并干燥后
 样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
您最近一年使用:0次
2024-02-20更新
|
231次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高一下学期选科适应性检测化学试卷
名校
9 . 利用如图所示装置进行下列实验,打开或关闭弹簧夹a,Z 中实验现象完全相同的是
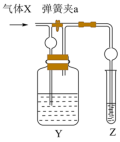
| 选项 | 气体X | Y中试剂 | Z中试剂 | |
| A | HCl | Na2CO3溶液 | NaAlO2溶液 | |
| B | NH3 | H2O | AgNO3溶液 | |
| C | Cl2 | 饱和食盐水 | 淀粉-KI溶液 | |
| D | SO2 | 酸性KMnO4溶液 | Ba(NO3)2溶液 |

| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-15更新
|
171次组卷
|
2卷引用:湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题
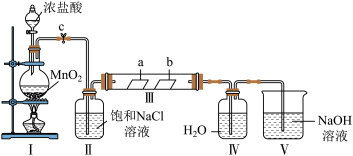
10 . 某化学兴趣小组为探究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)加入药品前,必须先___________ 。盛装浓盐酸的仪器名称为___________ 。
(2)装置I中发生反应的离子方程式为___________ 。
(3)装置V中NaOH溶液的作用是___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应如何改进?___________ 。
(1)加入药品前,必须先
(2)装置I中发生反应的离子方程式为
(3)装置V中NaOH溶液的作用是
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应如何改进?
您最近一年使用:0次
2024-02-02更新
|
57次组卷
|
2卷引用:湖南省益阳市2023-2024学年高一上学期期末质量检测化学试题



