1 . 向 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②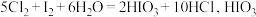 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是

 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:①
的变化曲线如图所示。(已知:① 可将
可将 氧化成
氧化成 ;②
;②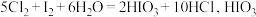 为强酸)下列说法中错误的是
为强酸)下列说法中错误的是
A.还原性: |
B.b点溶液中 |
C.a点时已通入标准状况下氯气的总体积为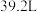 |
D.c点溶液中阴离子的个数为 |
您最近一年使用:0次
2023-12-01更新
|
880次组卷
|
4卷引用:河北省河北正中实验中学2023-2024学年高一上学期月考三化学试题
名校
解题方法
2 . 标准状况下,将SO2和Cl2组成的混合气体a L通入200mL 0.1mol·L-1 Fe2(SO4)3溶液中,充分反应后,气体被完全吸收,溶液的棕黄色变浅(溶液体积近似不变)。向反应后的溶液中加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥后称重,其质量为23.3g。则下列分析错误的是(已知:SO2+2Fe3++2H2O=SO +2Fe2++4H+)
+2Fe2++4H+)
 +2Fe2++4H+)
+2Fe2++4H+)| A.a L混合气体的物质的量可能为0.08mol |
| B.混合气体中SO2的体积为0.896L |
| C.所得沉淀为0.1mol的BaSO4 |
| D.混合气体中Cl2的物质的量可能为0.03mol |
您最近一年使用:0次
2023-02-16更新
|
1784次组卷
|
3卷引用:云南省曲靖市第一中学2022-2023学年高一下学期6月月考化学试题
名校
3 . 用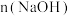 为
为 的
的 浓溶液吸收一定量的氯气,充分反应后溶液中只含有
浓溶液吸收一定量的氯气,充分反应后溶液中只含有 、
、 、
、 三种溶质。下列判断不正确的是
三种溶质。下列判断不正确的是
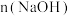 为
为 的
的 浓溶液吸收一定量的氯气,充分反应后溶液中只含有
浓溶液吸收一定量的氯气,充分反应后溶液中只含有 、
、 、
、 三种溶质。下列判断不正确的是
三种溶质。下列判断不正确的是A.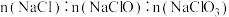 可能为9:4:1 可能为9:4:1 |
B.若反应中转移的电子的物质的量为 ,则 ,则 |
C.被吸收的氯气的物质的量为 |
D. 可能为14:9 可能为14:9 |
您最近一年使用:0次
2022-11-15更新
|
1277次组卷
|
6卷引用:浙江省湖州市吴兴高级中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
4 . 某溶液中有S2-、SO32-、Br-、I-四种阴离子各0.1mol。现通入Cl2,则通入Cl2的体积(标准状况)和溶液中相关离子的物质的量的关系图正确的是
A. | B.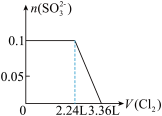 |
C.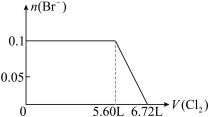 | D.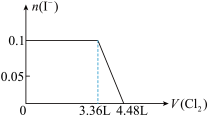 |
您最近一年使用:0次
2020-03-21更新
|
2509次组卷
|
5卷引用:重庆市第二十九中学2021届高三上学期10月月考化学试题
重庆市第二十九中学2021届高三上学期10月月考化学试题河北省昌黎第一中学2023届高三上学期第二次调研考试化学试题上海市普陀区2016届高三下学期质量调研化学试题(已下线)小题必刷05 离子检验与推断——2021年高考化学一轮复习小题必刷(通用版)(已下线)练习6 常见物质的检验-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)
5 . 如图,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请回答下列问题:

(1)A、G的化学式分别为_______________ 、________________ 。
(2)写出A与Fe反应的化学方程式___________________ 。
(3)写出反应②的化学方程式______________________ 。
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊试液中,观察到的现象是________________ ;请写出A与水反应的化学方程
式。
②A与石灰乳反应制得的漂白粉的有效成分是_________ (填化学式);该物质在空气中失效的原因______ (用化学方程式表示)。

(1)A、G的化学式分别为
(2)写出A与Fe反应的化学方程式
(3)写出反应②的化学方程式
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊试液中,观察到的现象是
式。
②A与石灰乳反应制得的漂白粉的有效成分是
您最近一年使用:0次
2016-12-09更新
|
1068次组卷
|
2卷引用:2016-2017学年河南省南阳一中高一上第一次月考化学卷
6 . 中学化学中常见的几种物质存在如图所示的转化关系。其中,A是一种黑色粉末状固体,C是一种黄绿色气体,实验室中常用E溶液吸收多余的C(图中部分产物和反应条件已略去)。

回答下列问题:
(1)写出A与B的浓溶液反应的化学方程式:_________ 。
(2)将ag粉未A加入bmol/L的B的浓溶液cL中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,NA可表示为_____________ 。
(3)将B的浓溶液与H的浓溶液混合,立即产生大最气体C,该反应的离子方程式为_______ 。
(4)某课外小组的同学用E溶液吸收C,利用下图所示装置向吸收液中持续通入SO2气体。
实验过程中观察到如下现象:

①开始时,溶液上方出现白雾,试纸a变红。甲同学认为是HCl使a变红,乙同学不同意甲的观点,乙同学认为使a变红的是_______ (写出一种即可)。
②片刻后,溶液上方出现黄绿色气体,试纸b变蓝。用离子方程式解释b变蓝的原因:_____________
③最终试纸b褪色。同学们认为可能的原因有两种:一是I2有还原性,黄绿色气体等物质将其氧化成IO3-,从而使蓝色消失;二是_______________ 。

回答下列问题:
(1)写出A与B的浓溶液反应的化学方程式:
(2)将ag粉未A加入bmol/L的B的浓溶液cL中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,NA可表示为
(3)将B的浓溶液与H的浓溶液混合,立即产生大最气体C,该反应的离子方程式为
(4)某课外小组的同学用E溶液吸收C,利用下图所示装置向吸收液中持续通入SO2气体。
实验过程中观察到如下现象:

①开始时,溶液上方出现白雾,试纸a变红。甲同学认为是HCl使a变红,乙同学不同意甲的观点,乙同学认为使a变红的是
②片刻后,溶液上方出现黄绿色气体,试纸b变蓝。用离子方程式解释b变蓝的原因:
③最终试纸b褪色。同学们认为可能的原因有两种:一是I2有还原性,黄绿色气体等物质将其氧化成IO3-,从而使蓝色消失;二是
您最近一年使用:0次
解题方法
7 . 有一瓶无色透明溶液,其中可能含有Na+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、I-。取该溶液进行以下实验:
①用PH试纸测得该溶液显酸性;
②取部分溶液,加入数滴新制氯水及少量CCl4,经振荡、静置后,CCl4层呈紫红色;
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐变至碱性,在整个滴加过程中无沉淀生成;
④取部分③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成;
(1)该溶液为无色透明溶液,可确定其中一定不含___________ ;(填离子符号,下同)
(2)由步骤①可知,溶液中一定不存在____________ ;
(3)由步骤②可知,溶液中含有____________ ;
(4)由步骤③可排除_____________ 、____________ 的存在;
(5)由步骤④可知,溶液中含有_________ ,由此可排除_________ 的存在;
(6)试验中不能够确定是否存在的阳离子可用___________ (填操作名称)进行检验。
①用PH试纸测得该溶液显酸性;
②取部分溶液,加入数滴新制氯水及少量CCl4,经振荡、静置后,CCl4层呈紫红色;
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐变至碱性,在整个滴加过程中无沉淀生成;
④取部分③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成;
(1)该溶液为无色透明溶液,可确定其中一定不含
(2)由步骤①可知,溶液中一定不存在
(3)由步骤②可知,溶液中含有
(4)由步骤③可排除
(5)由步骤④可知,溶液中含有
(6)试验中不能够确定是否存在的阳离子可用
您最近一年使用:0次
2016-12-09更新
|
1011次组卷
|
5卷引用:湖北省仙桃市沔城高级中学2021-2022学年高三上学期10月月考化学试题
8 . 某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究。
(1)【查阅资料】SO2Cl2名称是氯化硫酰,常温下是无色液体,极易水解,遇潮湿空气会产生白雾。
【讨论】SO2Cl2中S元素的化合价是________ 。
实验中制取的SO2和Cl2在混合前都必须提纯和干燥。
(2)【实验探究】实验中制得了干燥纯净的SO2和Cl2。
按下图收集满Cl2后,再通入SO2,集气瓶中立即有无色液体产生,充分反应后,将无色液体和剩余气体分离,分别对无色液体和剩余气体进行如下探究。

Ⅰ.探究反应产物。
向所得无色液体中加入水,立即产生白雾,振荡,静置,得无色溶液。经检验:该无色溶液中的阴离子(除OH-外)只有SO42-、Cl-。证明无色液体为SO2Cl2。
SO2Cl2与水反应的化学方程式是_________________ 。
验证无色溶液中含有Cl-的方法是_______________ 。
Ⅱ.探究反应进行的程度。
用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再加入BaCl2溶液,立即产生白色沉淀。
证明SO2与Cl2的反应是可逆反应。
阐述证明SO2与Cl2是可逆反应的理由_____________ 。
(3)【质疑】有同学提出:选修四教材习题中介绍SOCl2(亚硫酰氯)常温下是无色液体,极易水解,遇潮湿空气也会产生白雾。SO2与Cl2反应若还能生成SOCl2则无法证明生成的是SO2Cl2。
SO2Cl2与水反应的化学方程式是_________________ 。
小组讨论后认为不会生成SOCl2,理由是____________ 。
(1)【查阅资料】SO2Cl2名称是氯化硫酰,常温下是无色液体,极易水解,遇潮湿空气会产生白雾。
【讨论】SO2Cl2中S元素的化合价是
实验中制取的SO2和Cl2在混合前都必须提纯和干燥。
(2)【实验探究】实验中制得了干燥纯净的SO2和Cl2。
按下图收集满Cl2后,再通入SO2,集气瓶中立即有无色液体产生,充分反应后,将无色液体和剩余气体分离,分别对无色液体和剩余气体进行如下探究。

Ⅰ.探究反应产物。
向所得无色液体中加入水,立即产生白雾,振荡,静置,得无色溶液。经检验:该无色溶液中的阴离子(除OH-外)只有SO42-、Cl-。证明无色液体为SO2Cl2。
SO2Cl2与水反应的化学方程式是
验证无色溶液中含有Cl-的方法是
Ⅱ.探究反应进行的程度。
用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再加入BaCl2溶液,立即产生白色沉淀。
证明SO2与Cl2的反应是可逆反应。
阐述证明SO2与Cl2是可逆反应的理由
(3)【质疑】有同学提出:选修四教材习题中介绍SOCl2(亚硫酰氯)常温下是无色液体,极易水解,遇潮湿空气也会产生白雾。SO2与Cl2反应若还能生成SOCl2则无法证明生成的是SO2Cl2。
SO2Cl2与水反应的化学方程式是
小组讨论后认为不会生成SOCl2,理由是
您最近一年使用:0次



