1 . 实验室用 和浓盐酸反应制备
和浓盐酸反应制备 并回收
并回收 ,下列装置能达到实验目的的是
,下列装置能达到实验目的的是
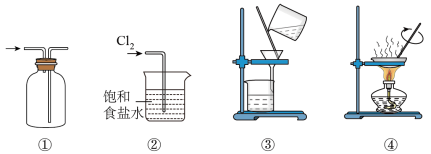
 和浓盐酸反应制备
和浓盐酸反应制备 并回收
并回收 ,下列装置能达到实验目的的是
,下列装置能达到实验目的的是
A.用①收集 | B.用②吸收尾气 |
C.用③分离 和 和 溶液 溶液 | D.用④蒸干 溶液制 溶液制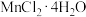 |
您最近一年使用:0次
2023-03-16更新
|
1896次组卷
|
6卷引用:广东省广州市2023届高三一模考试化学试题
广东省广州市2023届高三一模考试化学试题(已下线)专题13 化学实验基础(已下线)广东省广州市天河区2023届高三二模化学试题变式题(选择题6-10)上海市复旦大学附属中学2023-2024学年高一上学期期中考试化学试卷(B卷)广东省广州市2022-2023学年高三普通高中毕业班综合测试(一)化学试题 上海市七宝中学2023-2024学年高一上学期化学12月练习卷
名校
2 . 二氧化氯(ClO2)是一种黄绿色、极易爆炸的强氧化性气体,易溶于水,在水中溶解度约为Cl2的5倍,其水溶液在较高温度与光照下会生成ClO 和ClO
和ClO 。实验室制备ClO2的反应为2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。下列有关实验室制备ClO2的实验原理和装置能达到实验目的的是
。实验室制备ClO2的反应为2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。下列有关实验室制备ClO2的实验原理和装置能达到实验目的的是
 和ClO
和ClO 。实验室制备ClO2的反应为2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。下列有关实验室制备ClO2的实验原理和装置能达到实验目的的是
。实验室制备ClO2的反应为2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。下列有关实验室制备ClO2的实验原理和装置能达到实验目的的是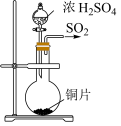 |  | 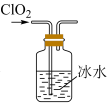 |  |
| A.获取SO2 | B.制备ClO2 | C.吸收ClO2 | D.处理尾气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列用Cl2氧化K2MnO4制备KMnO4的实验原理和装置能达到实验目的的是
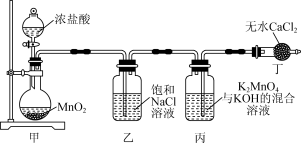

| A.用装置甲制取Cl2 | B.用装置乙除去HCl杂质 |
| C.用装置丙制备KMnO4 | D.用装置丁处理尾气 |
您最近一年使用:0次
2022-11-17更新
|
202次组卷
|
2卷引用:江苏省南通市通州区2022-2023学年高三上学期期中质量监测化学试题
解题方法
4 . 氯的含氧酸盐具有较强的氧化性,能够杀菌消毒,在预防新冠疫情中起到重要作用。某化学兴趣小组用氯气和相应的碱溶液反应制取NaClO和 ,制备装置如图所示(部分加持仪器略去),并研究
,制备装置如图所示(部分加持仪器略去),并研究 的氧化性。已知:氯气与碱反应,温度较高时生成
的氧化性。已知:氯气与碱反应,温度较高时生成 ,温度较低时生成
,温度较低时生成 。
。

(1)盛装浓盐酸的仪器名称是_______ 。
(2)装置A烧瓶中反应的化学方程式为_______ 。
(3)装置C中 与试剂a反应的离子方程式为
与试剂a反应的离子方程式为_______ 。
(4)如果缺少装置B,对制取NaClO和 的影响是
的影响是_______ 。
(5)E中可选用试剂有_______ (填标号)。
A.饱和 溶液 B.浓
溶液 B.浓 C.饱和NaCl溶液 D.NaOH溶液
C.饱和NaCl溶液 D.NaOH溶液
(6)该小组在探究 氧化性时,发现
氧化性时,发现 与
与 的反应速率先增大后减小,反应为
的反应速率先增大后减小,反应为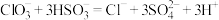 。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究
。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究 对化学反应速率的影响,设计如下实验:
对化学反应速率的影响,设计如下实验:
该实验_______ (填“能”或“不能”)达到实验目的,理由是_______ 。
 ,制备装置如图所示(部分加持仪器略去),并研究
,制备装置如图所示(部分加持仪器略去),并研究 的氧化性。已知:氯气与碱反应,温度较高时生成
的氧化性。已知:氯气与碱反应,温度较高时生成 ,温度较低时生成
,温度较低时生成 。
。
(1)盛装浓盐酸的仪器名称是
(2)装置A烧瓶中反应的化学方程式为
(3)装置C中
 与试剂a反应的离子方程式为
与试剂a反应的离子方程式为(4)如果缺少装置B,对制取NaClO和
 的影响是
的影响是(5)E中可选用试剂有
A.饱和
 溶液 B.浓
溶液 B.浓 C.饱和NaCl溶液 D.NaOH溶液
C.饱和NaCl溶液 D.NaOH溶液(6)该小组在探究
 氧化性时,发现
氧化性时,发现 与
与 的反应速率先增大后减小,反应为
的反应速率先增大后减小,反应为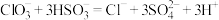 。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究
。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究 对化学反应速率的影响,设计如下实验:
对化学反应速率的影响,设计如下实验:| 实验序号 | 温度 |  | 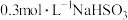 |  盐酸 盐酸 |  |
| ① | 25℃ | 10mL | 10mL | 0mL | 1mL |
| ② | 25℃ | 10mL | 10mL | 1mL | 0mL |
您最近一年使用:0次
2021-06-17更新
|
401次组卷
|
2卷引用:河南省郑州市2020-2021学年高一下学期期末考试化学试题
名校
5 . 氯化氢和氯气在生产生活中具有广泛应用。舍勒发现将软锰矿和浓盐酸混合加热可产生氯气,该方法仍是当今实验室制备氯气的主要方法之一。Deacon曾提在催化剂作用下,通过氧气直接氧化氯化氢制备氯气。该反应为可逆反应,热化学方程式为4HCl(g)+O2(g)=2Cl2(g)+H2O(g) ΔH=-116 kJ-mol-1。实验室制取Cl2时,下列装置能达到相应实验目的的是
| A | B | C | D |
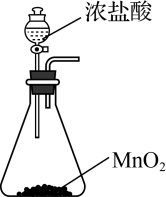 | 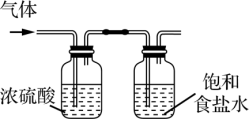 | 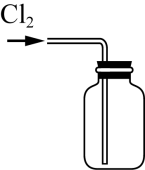 | 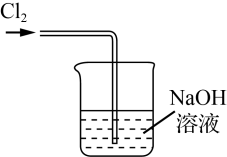 |
| 制备Cl2 | 净化Cl2 | 收集Cl2 | 尾气处理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-05-08更新
|
369次组卷
|
3卷引用:江苏省七市(南通、扬州、泰州、淮安、徐州、宿迁、连云港)2021届高三第三次调研考试化学试题
江苏省七市(南通、扬州、泰州、淮安、徐州、宿迁、连云港)2021届高三第三次调研考试化学试题(已下线)第12讲 富集在海水中的元素——卤素(精练)-2022年高考化学一轮复习讲练测湖南省常德市汉寿县第一中学2022届高三下学期第三次模考化学试题
6 . 如图是实验室用二氧化锰和浓盐酸制备氯气并进行一系列相关实验的装置(夹持装置已略)。

(1)装置A中盛装浓盐酸的仪器名称为________ ,发生反应的离子方程式为________ 。
(2)装置B中盛装的试剂为________ ,在实验过程中可以起到安全瓶的作用,一旦后续装置堵塞,B中会出现________ 现象。
(3)装置C的作用是证明干燥的 无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是________ (填字母,试剂不重复使用)。
a.干燥的石蕊试纸 b.湿润的石蕊试纸
c.碱石灰 d.无水氯化钙
(4)装置E中溶液变蓝色,证明了氯气化学性质中的________ 性;装置F中的试剂为________ 溶液(填化学式)。
(5) 也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用
也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用 和
和 制备等量的氯气,转移电子数之比为
制备等量的氯气,转移电子数之比为________ 。

(1)装置A中盛装浓盐酸的仪器名称为
(2)装置B中盛装的试剂为
(3)装置C的作用是证明干燥的
 无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
无漂白性,但其水溶液具有漂白性,则Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是a.干燥的石蕊试纸 b.湿润的石蕊试纸
c.碱石灰 d.无水氯化钙
(4)装置E中溶液变蓝色,证明了氯气化学性质中的
(5)
 也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用
也可以与浓盐酸反应生成氯气,是实验室快速制氯气的方法之一,分别使用 和
和 制备等量的氯气,转移电子数之比为
制备等量的氯气,转移电子数之比为
您最近一年使用:0次
名校
解题方法
7 . 浓盐酸和高锰酸钾在室温下即可制备氯气,用如图装置制备少量的氯气并探究其性质。下列说法正确的是


A.高锰酸钾和浓盐酸反应的离子方程式为: |
B.根据溴化钠和碘化钠中的现象可证明氧化性: |
| C.紫色石蕊试液先变红后褪色,说明氯气具有酸性和强氧化性 |
| D.可用饱和食盐水代替NaOH溶液吸收多余的氯气 |
您最近一年使用:0次
2023-04-21更新
|
218次组卷
|
2卷引用:江苏省常熟市2022-2023学年高二下学期期中考试化学试题
名校
解题方法
8 . 二氯异氰尿酸钠(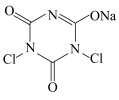 ,简称DCCNa)是一种高效、安全的消毒剂,常温下性质稳定,受热易分解,难溶于冷水。实验室通过以下原理和装置(夹持仪器已略去)可以制取DCCNa。
,简称DCCNa)是一种高效、安全的消毒剂,常温下性质稳定,受热易分解,难溶于冷水。实验室通过以下原理和装置(夹持仪器已略去)可以制取DCCNa。
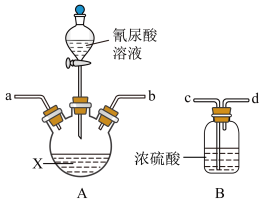
已知:实验室常用高浓度的NaClO溶液和氰尿酸溶液在10℃时反应制备DCCNa,主要发生反应: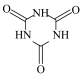 (氰尿酸)
(氰尿酸)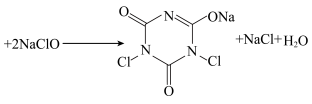
(1) 和
和 中
中 大小:
大小:
___________ -NH2(填“>”“<”或“=”)。
(2)A装置中盛装X试剂的仪器名称是___________ ;D中软导管的作用是___________ 。
(3)请选择合适的装置,按气流从左至右方向组装,则导管连接顺序为___________ (填小写字母)。
(4)X试剂为饱和氢氧化钠溶液。当装置A内出现___________ 现象时,打开装置A的活塞加入 (氰尿酸)溶液,在反应过程中仍不断通入
(氰尿酸)溶液,在反应过程中仍不断通入 的目的是
的目的是___________ 。
(5)实验过程中A的温度必须保持为7℃~12℃,pH值控制在6.5~8.5的范围,则该实验的控温方式是___________ 。若温度过高,pH过低,会生成 和
和 等,写出该反应的化学方程式
等,写出该反应的化学方程式___________ 。
 ,简称DCCNa)是一种高效、安全的消毒剂,常温下性质稳定,受热易分解,难溶于冷水。实验室通过以下原理和装置(夹持仪器已略去)可以制取DCCNa。
,简称DCCNa)是一种高效、安全的消毒剂,常温下性质稳定,受热易分解,难溶于冷水。实验室通过以下原理和装置(夹持仪器已略去)可以制取DCCNa。

已知:实验室常用高浓度的NaClO溶液和氰尿酸溶液在10℃时反应制备DCCNa,主要发生反应:
 (氰尿酸)
(氰尿酸)
(1)
 和
和 中
中 大小:
大小:
(2)A装置中盛装X试剂的仪器名称是
(3)请选择合适的装置,按气流从左至右方向组装,则导管连接顺序为
(4)X试剂为饱和氢氧化钠溶液。当装置A内出现
 (氰尿酸)溶液,在反应过程中仍不断通入
(氰尿酸)溶液,在反应过程中仍不断通入 的目的是
的目的是(5)实验过程中A的温度必须保持为7℃~12℃,pH值控制在6.5~8.5的范围,则该实验的控温方式是
 和
和 等,写出该反应的化学方程式
等,写出该反应的化学方程式
您最近一年使用:0次
名校
9 . 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。
I.制备N2H4
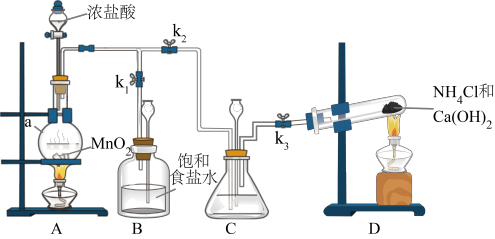
(1)装置C中盛放的试剂是___________ ,其作用是___________ 。(用离子方程式表示)
(2)装置D发生的反应的方程式为___________ 。
(3)制备N2H4的离子方程式为___________ 。
II.探究N2H4的还原性与碱性。将制得的肼分离提纯后,进行如图实验。
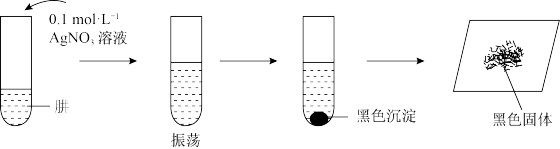
【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如表方案,进行实验。
(4)请完成表中的空白部分
(5)实验表明,黑色固体主要成分是Ag,还有少量氧化银。请解释原因:___________ 。
I.制备N2H4

(1)装置C中盛放的试剂是
(2)装置D发生的反应的方程式为
(3)制备N2H4的离子方程式为
II.探究N2H4的还原性与碱性。将制得的肼分离提纯后,进行如图实验。

【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如表方案,进行实验。
(4)请完成表中的空白部分
| 操作 | 现象 | 实验结论 |
| i. 取少量黑色固体于试管中,加入适量 | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ii. 取少量黑色固体于试管中加入足量稀硝酸,振荡。 | 黑色固体是Ag和Ag2O |
您最近一年使用:0次
10 . 某科学探究小组设计以下装置依次完成氯气的制备、氯酸钠的制备、次氯酸钠的制备并探究氯水的性质。

①为氯气发生装置,烧瓶中盛放MnO2固体;
②的试管里盛有15 mL 30%NaOH溶液。并置于热水浴中;
③的试管里盛有15 ml 8% NaOH溶液,并置于冰水浴中;
④的试管里加有紫色石磊试液:
⑤为尾气吸收装置。
(1)如何检验装置①的气密性_________________ 。
(2)如果实验室没有MnO2,下列物质可以用来代替MnO2制Cl2的是___________。
(3)制备氯酸钠的化学方程式为_____________________ 。
(4)比较制取氯酸钠和次氯酸钠的条件,二者的差异是:__________ 。
(5)④的试管里紫色石蕊试液现象:________________ 。
(6)次氯酸钠溶液可以杀灭析冠病毒,若将其与稀硫酸混合使用可增强消毒能力。现用18 mol/L浓硫酸来配制450 mL 0.2mol/L的稀硫酸。
①需用量筒量取浓硫酸的体积为_____ mL。
②定容时的操作:当液面离容量瓶颈部的刻度线1-2 cm时,_______ ,反复上下顺倒,摇匀。
③若所配制的稀硫酸浓度偏高,则下列可能的原因分析中正多的是________ 。
A.配制前,容量瓶用蒸馏水洗涤后再用硫酸润洗
B.量取浓硫酸时,读数时俯视液体的凹液面
C.浓硫酸稀释后立即转移至容量瓶定容
D.颠倒摇匀后,液面低于刻度线,继续滴加蒸馏水

①为氯气发生装置,烧瓶中盛放MnO2固体;
②的试管里盛有15 mL 30%NaOH溶液。并置于热水浴中;
③的试管里盛有15 ml 8% NaOH溶液,并置于冰水浴中;
④的试管里加有紫色石磊试液:
⑤为尾气吸收装置。
(1)如何检验装置①的气密性
(2)如果实验室没有MnO2,下列物质可以用来代替MnO2制Cl2的是___________。
| A.KMnO4 | B.Fe2O3 | C.浓硫酸 | D.KClO3 |
(4)比较制取氯酸钠和次氯酸钠的条件,二者的差异是:
(5)④的试管里紫色石蕊试液现象:
(6)次氯酸钠溶液可以杀灭析冠病毒,若将其与稀硫酸混合使用可增强消毒能力。现用18 mol/L浓硫酸来配制450 mL 0.2mol/L的稀硫酸。
①需用量筒量取浓硫酸的体积为
②定容时的操作:当液面离容量瓶颈部的刻度线1-2 cm时,
③若所配制的稀硫酸浓度偏高,则下列可能的原因分析中正多的是
A.配制前,容量瓶用蒸馏水洗涤后再用硫酸润洗
B.量取浓硫酸时,读数时俯视液体的凹液面
C.浓硫酸稀释后立即转移至容量瓶定容
D.颠倒摇匀后,液面低于刻度线,继续滴加蒸馏水
您最近一年使用:0次



