名校
1 . 利用 氧化尿素制备
氧化尿素制备 (水合肼)的实验流程如图所示:
(水合肼)的实验流程如图所示: 有强还原性,能与
有强还原性,能与 剧烈反应生成
剧烈反应生成 。
。
下列说法不正确的是
 氧化尿素制备
氧化尿素制备 (水合肼)的实验流程如图所示:
(水合肼)的实验流程如图所示: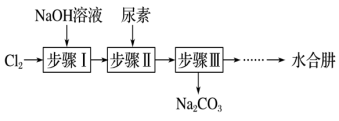
 有强还原性,能与
有强还原性,能与 剧烈反应生成
剧烈反应生成 。
。下列说法不正确的是
| A.步骤Ⅰ中为避免温度过高,可采用冰水浴 |
B.步骤Ⅰ制备 溶液时,测得产物中 溶液时,测得产物中 与 与 的物质的量之比为5∶1,则参与反应的氧化剂与还原剂的物质的量之比为5∶3 的物质的量之比为5∶1,则参与反应的氧化剂与还原剂的物质的量之比为5∶3 |
C.步骤Ⅱ中可将尿素水溶液逐滴滴入 碱性溶液中 碱性溶液中 |
D.生成水合肼反应的离子方程式为ClO﹣+CO(NH2)2+2OH﹣=Cl-+N2H4•H2O+CO |
您最近一年使用:0次
2021-07-24更新
|
1575次组卷
|
10卷引用:辽宁省铁岭市六校2020-2021学年高二下学期期末联考化学试题
辽宁省铁岭市六校2020-2021学年高二下学期期末联考化学试题山西省运城市2021-2022学年高三上学期期中考试化学试题(已下线)第二章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)2021年北京高考化学试题变式题1-10 河南大学附属中学2022-2023学年高一下学期第一次月考化学试题江苏省南菁高级中学2023-2024学年高一上学期9月阶段性检测化学(创优班)试题江苏省南京市第九中学2023-2024学年高一上学期10月阶段学情调研化学试题江苏省苏州市吴县中学2023-2024学年高一上学期12月月考化学试题四川省成都市树德中学2023-2024学年高一下学期3月月考化学试题安徽省马鞍山市第二中学2023-2024学年高一下学期期中测试(实验班)化学试卷
名校
解题方法
2 . 将一定量的氯气通入50mL10mol/L的氢氧化钠浓溶液中,加热少许时间后,溶液中形成NaCl、NaClO、NaClO3共存体系(不考虑氯气和水的反应)。下列说法正确的是
| A.若反应中转移的电子为nmol,则0.25<n<0.5 |
| B.溶液中n(NaCl)∶n(NaClO):n(NaClO3)可能为6∶1∶1 |
| C.与氢氧化钠反应的氯气的物质的量:0.25mol<n(Cl2)<0.75mol |
D.当溶液中n(NaClO):n(NaClO3)=5∶1时,反应的离子方程式为8Cl2+16OH-=10Cl-+5ClO-+ +8H2O +8H2O |
您最近一年使用:0次
2021-07-23更新
|
1285次组卷
|
6卷引用:湖南省岳阳县第一中学2020-2021年高一下学期期末考试化学试题
湖南省岳阳县第一中学2020-2021年高一下学期期末考试化学试题湖北省武汉市蔡甸区汉阳一中2021-2022学年高一上学期9月月考化学试题河北省石家庄市第二中学南校区2021-2022学年高一上学期12月月考化学试题河北省保定市唐县第二中学2022-2023学年高一下学期第一次月考化学试题江西省吉安市第一中学2022-2023学年高一上学期期末考试化学试题(已下线)专题03 氧化还原反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
解题方法
3 . 下列反应的离子方程式书写正确的是
A.用 溶液吸收过量 溶液吸收过量 : :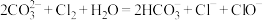 |
B.ICl和 的化学性质相似,将ICl通入NaOH溶液中: 的化学性质相似,将ICl通入NaOH溶液中: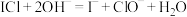 |
C.用稀硝酸清洗试管内壁的银镜: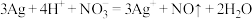 |
D.往溴化银悬浊液中滴加少量KCl稀溶液: |
您最近一年使用:0次
4 . 无水三氯化铁常用于净水剂、印染的媒染剂,印刷制版时的腐蚀剂,在化学工业中还可制造其他铁盐,及处理肥皂提取粗甘油等。它具有易水解、易升华的性质。铁粉与氯气反应制备无水FeCl3的实验装置如图所示:

回答下列问题:
(1)装置A的作用是_______ ,通入氯气后,装置A中观察到有酸雾产生,原因是_______ 。
(2)装置C中P2O5的作用是_______ ,请写出装置D中发生反应的化学方程式:_______ 。
(3)在E、G处收集产物是利用了FeCl3_______ 的性质;实验过程中若F处出现堵塞,则在B处可观察到的现象是_______ 。
(4)装置H的作用是_______ ;装置I中发生反应的离子方程式是_______ 。
(5)某同学用11.2g干燥铁粉制得无水FeCl3样品29.9g,该次实验的产率是_______ 。
(6)实验室中还常用SOCl2与FeCl3·6H2O晶体共热制备无水FeCl3,其化学反应方程式为_______ 。

回答下列问题:
(1)装置A的作用是
(2)装置C中P2O5的作用是
(3)在E、G处收集产物是利用了FeCl3
(4)装置H的作用是
(5)某同学用11.2g干燥铁粉制得无水FeCl3样品29.9g,该次实验的产率是
(6)实验室中还常用SOCl2与FeCl3·6H2O晶体共热制备无水FeCl3,其化学反应方程式为
您最近一年使用:0次
2021·天津·三模
名校
解题方法
5 . ClCH2COOH(氯乙酸,熔点为50℃)是一种化工原料,实验室制备氯乙酸的装置如图:

按下列实验步骤回答问题:
(1)在500mL三颈烧瓶中放置300g冰醋酸和15g催化剂乙酸酐。加热至105℃时,开始徐徐通入干燥纯净的氯气。加热的方法是___ ,仪器X的名称是__ ,乙中盛放的药品是___ 。
(2)氯气通入冰醋酸中呈黄色随即黄色褪去,用化学方程式解释黄色褪去的原因:__ ,氯气通入速率以三颈烧瓶中无黄绿色气体逸出为度,控制通入氯气速率的方法是___ ,戊中漏斗的作用是___ ,NaOH溶液的主要作用是__ 。
(3)反应约需10小时,每隔2小时向三颈烧瓶中加入5g乙酸酐,当取出样品测得其___ 时,停止通入氯气。
(4)将熔融的生成物移至蒸馏瓶中进行蒸馏纯化,收集186~188℃馏分。选择装置a蒸馏,直形冷凝管易炸裂,原因是___ 。
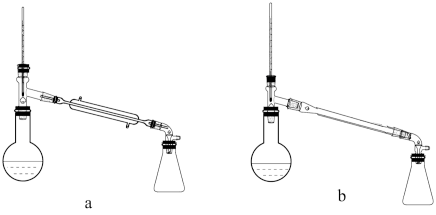
(5)冷凝后生成无色氯乙酸晶体425g,产率约为___ (保留2位有效数字)。

按下列实验步骤回答问题:
(1)在500mL三颈烧瓶中放置300g冰醋酸和15g催化剂乙酸酐。加热至105℃时,开始徐徐通入干燥纯净的氯气。加热的方法是
(2)氯气通入冰醋酸中呈黄色随即黄色褪去,用化学方程式解释黄色褪去的原因:
(3)反应约需10小时,每隔2小时向三颈烧瓶中加入5g乙酸酐,当取出样品测得其
(4)将熔融的生成物移至蒸馏瓶中进行蒸馏纯化,收集186~188℃馏分。选择装置a蒸馏,直形冷凝管易炸裂,原因是

(5)冷凝后生成无色氯乙酸晶体425g,产率约为
您最近一年使用:0次
6 . 某小组以电石渣[主要成分为 和
和 ]为原料制备
]为原料制备 晶体,流程如下:
晶体,流程如下:
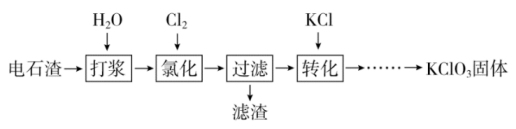
已知:氯化时 与
与 反应生成
反应生成 ,
, 进一步转化生成
进一步转化生成 ,少量
,少量 分解生成
分解生成 和
和 。请回答:
。请回答:
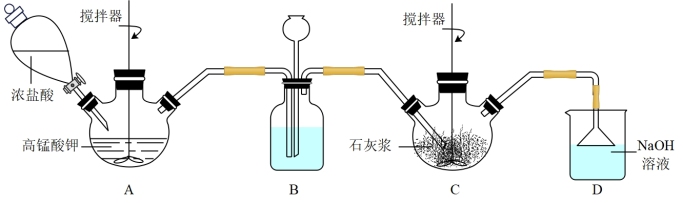
(1)氯化时装置如图所示,B中的试剂是___________ ;若C中导管处堵塞则B中的现象是___________ 。
(2)下列说法不正确 的是___________ 。
A.打浆时加水形成石灰浆的目的是使 与
与 充分反应
充分反应
B.氯化时应快速通入氯气以提高氯气的转化率
C.过滤得到的滤渣中含有 、
、
D.过滤后的滤液中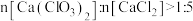
(3)对抽滤后获得的 晶体进行洗涤的方法是
晶体进行洗涤的方法是___________ 。
(4)某小组认为获得的 产品中含有KCl、
产品中含有KCl、 两种物质,为测定
两种物质,为测定 的含量,从下列选项中选出合理的操作(操作可以重复使用)并排序:称取mg样品→用蒸馏水溶解→___________→___________→___________→___________→___________→___________→计算,
的含量,从下列选项中选出合理的操作(操作可以重复使用)并排序:称取mg样品→用蒸馏水溶解→___________→___________→___________→___________→___________→___________→计算,___________
a.往滤液中加入足量的 、
、 溶液b.过滤、洗涤
溶液b.过滤、洗涤
c.干燥、称量d.加入足量的 、
、 溶液
溶液
(5)该小组用上述方法测得 产品中
产品中 的质量分数为72.0%,高于理论值。可能原因是
的质量分数为72.0%,高于理论值。可能原因是___________ 。
 和
和 ]为原料制备
]为原料制备 晶体,流程如下:
晶体,流程如下:
已知:氯化时
 与
与 反应生成
反应生成 ,
, 进一步转化生成
进一步转化生成 ,少量
,少量 分解生成
分解生成 和
和 。请回答:
。请回答:(1)氯化时装置如图所示,B中的试剂是

(2)下列说法
A.打浆时加水形成石灰浆的目的是使
 与
与 充分反应
充分反应B.氯化时应快速通入氯气以提高氯气的转化率
C.过滤得到的滤渣中含有
 、
、
D.过滤后的滤液中
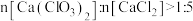
(3)对抽滤后获得的
 晶体进行洗涤的方法是
晶体进行洗涤的方法是(4)某小组认为获得的
 产品中含有KCl、
产品中含有KCl、 两种物质,为测定
两种物质,为测定 的含量,从下列选项中选出合理的操作(操作可以重复使用)并排序:称取mg样品→用蒸馏水溶解→___________→___________→___________→___________→___________→___________→计算,
的含量,从下列选项中选出合理的操作(操作可以重复使用)并排序:称取mg样品→用蒸馏水溶解→___________→___________→___________→___________→___________→___________→计算,a.往滤液中加入足量的
 、
、 溶液b.过滤、洗涤
溶液b.过滤、洗涤c.干燥、称量d.加入足量的
 、
、 溶液
溶液(5)该小组用上述方法测得
 产品中
产品中 的质量分数为72.0%,高于理论值。可能原因是
的质量分数为72.0%,高于理论值。可能原因是
您最近一年使用:0次
名校
解题方法
7 . 一定温度下,将 缓缓通入一定浓度的
缓缓通入一定浓度的 溶液中,至两者恰好完全反应,生成物中有三种含氯的离子,其中
溶液中,至两者恰好完全反应,生成物中有三种含氯的离子,其中 和
和 两种离子的物质的量(n)与时间(t)的关系如图所示。下列说法正确的是
两种离子的物质的量(n)与时间(t)的关系如图所示。下列说法正确的是

 缓缓通入一定浓度的
缓缓通入一定浓度的 溶液中,至两者恰好完全反应,生成物中有三种含氯的离子,其中
溶液中,至两者恰好完全反应,生成物中有三种含氯的离子,其中 和
和 两种离子的物质的量(n)与时间(t)的关系如图所示。下列说法正确的是
两种离子的物质的量(n)与时间(t)的关系如图所示。下列说法正确的是
A.溶液中 |
B.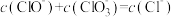 |
C.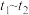 仅发生反应 仅发生反应 |
D.原 溶液中, 溶液中,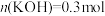 |
您最近一年使用:0次
2021-01-05更新
|
1461次组卷
|
9卷引用:黑龙江省齐齐哈尔市2020-2021学年高一上学期期末考试化学试题
黑龙江省齐齐哈尔市2020-2021学年高一上学期期末考试化学试题山西省晋城市(高平一中、阳城一中、高平实验中学)2020-2021学年高一下学期开学考试化学试题辽宁省实验中学2021-2022学年高一上学期11月期中阶段测试化学试题吉林省长春外国语学校2021-2022学年高一下学期期初考试化学试题黑龙江省牡丹江市第一高级中学2022-2023学年高一上学期11月期中考试化学试题黑龙江省牡丹江市第一高级中学2022-2023学年高一上学期11月期中考试化学试题吉林省四平市第一高级中学2023-2024学年高一上学期第二次月考化学试题江苏省无锡市辅仁高级中学2023-2024学年高一上学期期末复习化学模块综合试卷(一)甘肃省武威市民勤县第一中学2023-2024学年高一下学期开学考试化学试题
名校
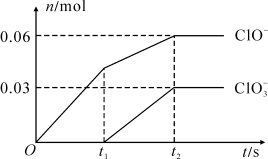
8 . 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
| A.原溶液中KOH的物质的量是0.3 mol |
B. 的生成是由氯气的量的多少引起的 的生成是由氯气的量的多少引起的 |
| C.反应中转移电子的物质的量是0.21 mol |
D.依据图象,总的离子反应方程式为10OH-+5Cl2=2C1O-+ +7Cl-+5H2O +7Cl-+5H2O |
您最近一年使用:0次
2020-10-10更新
|
950次组卷
|
4卷引用:黑龙江省大庆实验中学2021届高三上学期第一次月考化学试题
名校
解题方法
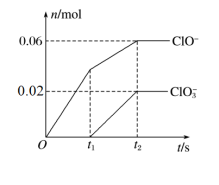
9 . 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有3种含氯元素的离子,其中ClO-和ClO 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法正确的是
| A.苛性钾中KOH的物质的量为0.24mol |
| B.反应中转移电子的物质的量是0.21mol |
| C.有2.688L氯气参与反应 |
D.酸性条件下ClO-和ClO 可生成Cl2 可生成Cl2 |
您最近一年使用:0次
10 . I.橙红色化合物A由五种元素组成,其中一种元素为原子半径最大的短周期元素(稀有气体元素除外),按如图流程进行实验。气体B为纯净物,能使湿润的红色石蕊试纸变蓝,溶液C呈黄色,沉淀D为砖红色沉淀。
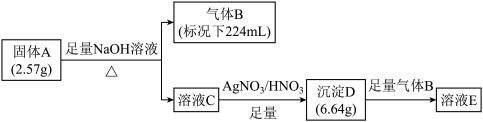
请回答:
(1)组成A的金属元素是___________ (填元素符号),A的化学式是___________ 。
(2)沉淀D与足量B反应的离子反应方程式____________ 。
(3)A中的某种金属元素对应的单质可以通过铝热反应制备,写出化学反应方程式________ 。
II.某兴趣小组为了探究84消毒液(主要成分NaClO)和酒精混合使用是否存在安全隐患,利用如图装置进行实验。
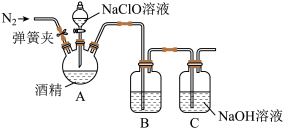
请回答:
(1)三颈烧瓶中出现黄绿色气体,请写出相应的化学方程式__________ 。(乙醇被氧化为乙醛)
(2)有同学用手触碰三颈烧瓶后发现,反应一段时间后装置温度升高,所以提出产生的气体中可能混有O2,请用离子方程式解释__________ ,该同学为了验证O2,打开弹簧夹,用带火星的木条检验,该操作的错误为___________ 。

请回答:
(1)组成A的金属元素是
(2)沉淀D与足量B反应的离子反应方程式
(3)A中的某种金属元素对应的单质可以通过铝热反应制备,写出化学反应方程式
II.某兴趣小组为了探究84消毒液(主要成分NaClO)和酒精混合使用是否存在安全隐患,利用如图装置进行实验。

请回答:
(1)三颈烧瓶中出现黄绿色气体,请写出相应的化学方程式
(2)有同学用手触碰三颈烧瓶后发现,反应一段时间后装置温度升高,所以提出产生的气体中可能混有O2,请用离子方程式解释
您最近一年使用:0次



