1 .  代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.标准状况下,11.2L苯中含有的原子数目为 |
B.0.3 的 的 溶液中含有 溶液中含有 的数目为 的数目为 |
C.用石灰乳完全吸收2mol  时,转移电子的数目是 时,转移电子的数目是 |
D.在常温常压下,44g  与 与 混合物气体中所含的原子数目一定为 混合物气体中所含的原子数目一定为 |
您最近一年使用:0次
名校
解题方法
2 . 微观探析是认识物质的一种途径。设 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是
 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是A.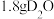 中含有的中子数目为 中含有的中子数目为 |
B.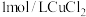 溶液中含有 溶液中含有 的数目小于 的数目小于 |
C. 与 与 的混合物中含有的分子数为 的混合物中含有的分子数为 |
D.25℃,101kPa, 与NaOH溶液完全反应,转移电子数目为 与NaOH溶液完全反应,转移电子数目为 |
您最近一年使用:0次
2024-03-06更新
|
863次组卷
|
4卷引用:2024届广东省汕头市高三下学期一模化学试题
3 . 目前支原体肺炎流行,及时消毒有利于降低感染几率。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂等,其中含氯消毒剂的家族最庞大、应用最广泛。
(1)次氯酸钠( )为“84”消毒液的有效成分,常温下用烧碱溶液吸收
)为“84”消毒液的有效成分,常温下用烧碱溶液吸收 可制备“84”消毒液,反应的化学方程式为
可制备“84”消毒液,反应的化学方程式为___________ 。
(2)但在巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿,一种可能原因是 与
与 反应产生
反应产生 促进藻类快速生长,该反应中氧化剂是
促进藻类快速生长,该反应中氧化剂是___________ ,若生成标况下44.8L的 ,转移电子的数目为
,转移电子的数目为___________ 。
(3)如果在不同温度、浓度的条件下, 与
与 溶液的反应,可以生成
溶液的反应,可以生成 或
或 。现将氯气缓缓通入冷
。现将氯气缓缓通入冷 溶液,当溶液中含有的
溶液,当溶液中含有的 与
与 的物质的量为1:1时,
的物质的量为1:1时,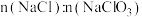 为
为___________ ,整个过程,参加反应所需 与氯气的物质的量之比为
与氯气的物质的量之比为___________ 。
若将 通入含amol
通入含amol 的溶液中,发生上述过程,回答下列问题:
的溶液中,发生上述过程,回答下列问题:
(4) 与
与 的物质的量之和可能为
的物质的量之和可能为 amol,该说法
amol,该说法___________ 。
A.正确 B.错误
(5)反应中转移电子的物质的量可能为___________。
亚氯酸钠( )为便携式消毒除菌卡的主要活性成分,一种制备
)为便携式消毒除菌卡的主要活性成分,一种制备 粗产品的工艺流程如下图,已知,纯
粗产品的工艺流程如下图,已知,纯 易分解爆炸,一般用空气稀释到10%以下。
易分解爆炸,一般用空气稀释到10%以下。 在发生器中发生
在发生器中发生________ (氧化或还原)反应,该反应的还原产物为_________ ,吸收塔中温度不宜过高,否则会导致 产率下降,原因是
产率下降,原因是___________ 。
(7)“有效氯含量”的定义是:每克含氯消毒剂的氧化能力(即得电子数)相当于多少克 的氧化能力(氯元素均被还原至
的氧化能力(氯元素均被还原至 价),则亚氯酸钠
价),则亚氯酸钠 的有效氯含量为
的有效氯含量为___________ 。(保留两位小数)。
(1)次氯酸钠(
 )为“84”消毒液的有效成分,常温下用烧碱溶液吸收
)为“84”消毒液的有效成分,常温下用烧碱溶液吸收 可制备“84”消毒液,反应的化学方程式为
可制备“84”消毒液,反应的化学方程式为(2)但在巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿,一种可能原因是
 与
与 反应产生
反应产生 促进藻类快速生长,该反应中氧化剂是
促进藻类快速生长,该反应中氧化剂是 ,转移电子的数目为
,转移电子的数目为(3)如果在不同温度、浓度的条件下,
 与
与 溶液的反应,可以生成
溶液的反应,可以生成 或
或 。现将氯气缓缓通入冷
。现将氯气缓缓通入冷 溶液,当溶液中含有的
溶液,当溶液中含有的 与
与 的物质的量为1:1时,
的物质的量为1:1时,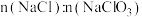 为
为 与氯气的物质的量之比为
与氯气的物质的量之比为若将
 通入含amol
通入含amol 的溶液中,发生上述过程,回答下列问题:
的溶液中,发生上述过程,回答下列问题:(4)
 与
与 的物质的量之和可能为
的物质的量之和可能为 amol,该说法
amol,该说法A.正确 B.错误
(5)反应中转移电子的物质的量可能为___________。
A. amol amol | B. amol amol | C. amol amol | D.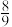 amol amol |
亚氯酸钠(
 )为便携式消毒除菌卡的主要活性成分,一种制备
)为便携式消毒除菌卡的主要活性成分,一种制备 粗产品的工艺流程如下图,已知,纯
粗产品的工艺流程如下图,已知,纯 易分解爆炸,一般用空气稀释到10%以下。
易分解爆炸,一般用空气稀释到10%以下。
 在发生器中发生
在发生器中发生 产率下降,原因是
产率下降,原因是(7)“有效氯含量”的定义是:每克含氯消毒剂的氧化能力(即得电子数)相当于多少克
 的氧化能力(氯元素均被还原至
的氧化能力(氯元素均被还原至 价),则亚氯酸钠
价),则亚氯酸钠 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
2024-02-02更新
|
0次组卷
|
2卷引用:上海交通大学附属中学2023-2024学年高一上学期期末化学试卷
解题方法
4 . 金属钛( )被誉为21世纪的明星金属,工业上利用氢气还原
)被誉为21世纪的明星金属,工业上利用氢气还原 制取金属钛(
制取金属钛( )。某化学实验小组利用反应:TiO2+2C+2Cl2
)。某化学实验小组利用反应:TiO2+2C+2Cl2 TiCl4+2CO,在无水无氧条件下制备
TiCl4+2CO,在无水无氧条件下制备 (熔点:
(熔点: ,沸点
,沸点 ,溶于有机溶剂,遇水生成难溶于水的
,溶于有机溶剂,遇水生成难溶于水的 ),其装置示意图如下(某些夹持仪器略)。回答下列问题:
),其装置示意图如下(某些夹持仪器略)。回答下列问题:
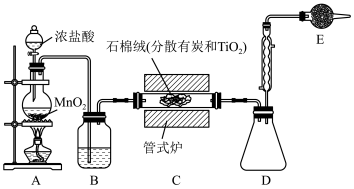
(1)检查装置气密性并加入药品。先点燃酒精灯,当观察到_________ 再加热管式炉,当观察到_________ 时说明反应已结束,停止加热管式炉。
(2)A装置发生反应的化学方程式是___________________________ 。
(3)B中的试剂是_________ ,E装置的作用是__________________ 。
(4)设计一个简单实验证明D装置中生成了
_________________________ 。
(5)该装置存在不足之处,改进的措施是____________________ 。
 )被誉为21世纪的明星金属,工业上利用氢气还原
)被誉为21世纪的明星金属,工业上利用氢气还原 制取金属钛(
制取金属钛( )。某化学实验小组利用反应:TiO2+2C+2Cl2
)。某化学实验小组利用反应:TiO2+2C+2Cl2 TiCl4+2CO,在无水无氧条件下制备
TiCl4+2CO,在无水无氧条件下制备 (熔点:
(熔点: ,沸点
,沸点 ,溶于有机溶剂,遇水生成难溶于水的
,溶于有机溶剂,遇水生成难溶于水的 ),其装置示意图如下(某些夹持仪器略)。回答下列问题:
),其装置示意图如下(某些夹持仪器略)。回答下列问题:
(1)检查装置气密性并加入药品。先点燃酒精灯,当观察到
(2)A装置发生反应的化学方程式是
(3)B中的试剂是
(4)设计一个简单实验证明D装置中生成了

(5)该装置存在不足之处,改进的措施是
您最近一年使用:0次
名校
5 . 元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分。请回答下列问题:
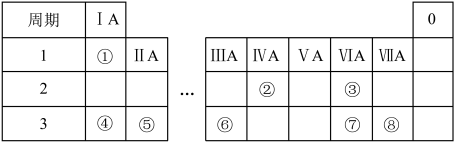
(1)画出④的原子结构示意图_____ 。
(2)①的单质在盛满⑧的单质的集气瓶中燃烧,反应现象为_____ 。
(3)③和④组成的一种物质中含有两种类型的化学键,该物质的化学式为_____ 。
(4)⑥的单质和④的最高价氧化物的水化物反应的化学方程式为_____ 。
(5)已知⑤的单质与②的最高价氧化物A在点燃条件下能反应生成黑色单质,推测④的单质_____ (填“能不能”)与A反应。
(6)为比较⑦和⑧ 非金属性,某小组同学设计实验进行探究。
非金属性,某小组同学设计实验进行探究。
【理论依据】氧化性较强的单质能置换出氧化性较弱的单质
【实验方案】
【实验过程】
按照实验方案操作,观察到的现象与预测的一致,写出该反应的化学方程式_____ 。
【实验结论】非金属性:⑦<⑧

(1)画出④的原子结构示意图
(2)①的单质在盛满⑧的单质的集气瓶中燃烧,反应现象为
(3)③和④组成的一种物质中含有两种类型的化学键,该物质的化学式为
(4)⑥的单质和④的最高价氧化物的水化物反应的化学方程式为
(5)已知⑤的单质与②的最高价氧化物A在点燃条件下能反应生成黑色单质,推测④的单质
(6)为比较⑦和⑧
 非金属性,某小组同学设计实验进行探究。
非金属性,某小组同学设计实验进行探究。【理论依据】氧化性较强的单质能置换出氧化性较弱的单质
【实验方案】
| 实验操作 | 预测现象 |
| 取Na2S溶液于试管中,滴入少量新制氯水 |
按照实验方案操作,观察到的现象与预测的一致,写出该反应的化学方程式
【实验结论】非金属性:⑦<⑧
您最近一年使用:0次
名校
6 . 已知:将一定最的 通入100mL 6
通入100mL 6  NaOH溶液中恰好完全反应,产物中可能有NaCl、NaClO、
NaOH溶液中恰好完全反应,产物中可能有NaCl、NaClO、 ,且
,且 的物质的量浓度与温度高低有关。下列说法正确的是
的物质的量浓度与温度高低有关。下列说法正确的是
 通入100mL 6
通入100mL 6  NaOH溶液中恰好完全反应,产物中可能有NaCl、NaClO、
NaOH溶液中恰好完全反应,产物中可能有NaCl、NaClO、 ,且
,且 的物质的量浓度与温度高低有关。下列说法正确的是
的物质的量浓度与温度高低有关。下列说法正确的是A.反应后溶液中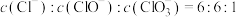 |
B.被氢氧化钠溶液吸收的 的物质的量为1.2mol 的物质的量为1.2mol |
| C.反应中转移的电子的物质的量可能为0.4mol |
D.反应后溶液中 |
您最近一年使用:0次
2023-04-30更新
|
635次组卷
|
4卷引用:山东省青岛市一中2022-2023学年高一下学期期中考试化学试题
名校
7 . 已知:将 通入适量的KOH溶液,反应物恰好完全反应,产物中可能有KCl、KClO、
通入适量的KOH溶液,反应物恰好完全反应,产物中可能有KCl、KClO、 ,且产物的成分与反应温度有关。常温条件下反应为
,且产物的成分与反应温度有关。常温条件下反应为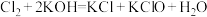 ,加热时反应为
,加热时反应为 ,当
,当 mol时,下列有关说法错误的是
mol时,下列有关说法错误的是
 通入适量的KOH溶液,反应物恰好完全反应,产物中可能有KCl、KClO、
通入适量的KOH溶液,反应物恰好完全反应,产物中可能有KCl、KClO、 ,且产物的成分与反应温度有关。常温条件下反应为
,且产物的成分与反应温度有关。常温条件下反应为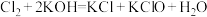 ,加热时反应为
,加热时反应为 ,当
,当 mol时,下列有关说法错误的是
mol时,下列有关说法错误的是| A.参加反应的氯气的物质的量等于0.5a mol |
| B.不管如何改变反应温度,产物中肯定存在KCl |
C.改变反应温度,反应中转移电子的物质的量n的范围是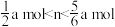 |
D.某温度下反应,若反应后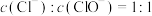 则产物中不可能存在 则产物中不可能存在 |
您最近一年使用:0次
2023-04-21更新
|
449次组卷
|
2卷引用:广西壮族自治区玉林市2022-2023学年高一下学期期中考试化学试题
名校
8 . 氯化亚铜(CuCl)是白色粉末,微溶于水,广泛应用于化工和印染等行业。某研究性学习小组模拟热分解CuCl2•2H2O制备CuCl的过程,并进行相关物质转化的探究。
已知:酸性条件下Cu+不稳定

下列说法不正确的是
已知:酸性条件下Cu+不稳定

下列说法不正确的是
| A.X气体是HCl,可抑制CuCl2•2H2O加热时水解 |
| B.途径1中产生的Cl2可以回收利用,也可以通入饱和NaOH溶液中除去 |
C.途径2中200℃时反应的化学方程式为Cu2(OH)2Cl2 2CuO+2HCl↑ 2CuO+2HCl↑ |
D.CuCl与稀硫酸反应的离子方程式为2Cu++4H++SO =2Cu2++SO2↑+2H2O =2Cu2++SO2↑+2H2O |
您最近一年使用:0次
2023-04-12更新
|
1046次组卷
|
7卷引用:北京市顺义区2023届高三下学期第二次化学统练题
北京市顺义区2023届高三下学期第二次化学统练题(已下线)专题10 物质的反应及转化(已下线)第07练 元素及其化合物基础知识和应用 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题江西省丰城中学2023-2024学年高三上学期开学考试化学试题河南省中原名校联盟2024届高三上学期9月调研考试化学试题陕西省西安市长安区第一中学2023-2024学年高三上学期第三次教学质量检测(期中)化学试题
解题方法
9 . 某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:i. 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ii.浓碱条件下, 可被
可被 还原为
还原为 。
。
iii. 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
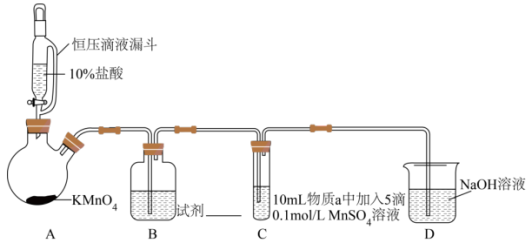
(1)通入 前,II、III中沉淀由白色变为黑色的化学方程式为
前,II、III中沉淀由白色变为黑色的化学方程式为_______ 。
(2)对比实验I、II通入 后的实验现象,对于二价锰化合物还原性的认识是
后的实验现象,对于二价锰化合物还原性的认识是_______ 。
(3)根据资料ⅱ,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入 发生反应
发生反应 ,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①取III中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_______ ,溶液绿色缓慢加深,原因是 被
被_______ (填“化学式”)氧化,可证明III的悬浊液中氧化剂过量;
②取II中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是_______ 。
③从反应速率的角度,分析实验III未得到绿色溶液的可能原因_______ 。
资料:i.
 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。ii.浓碱条件下,
 可被
可被 还原为
还原为 。
。iii.
 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。实验装置如图(夹持装置略)

| 序号 | 物质a | C中实验现象 | |
通入 前 前 | 通入 后 后 | ||
| I | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| II | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| III | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
 前,II、III中沉淀由白色变为黑色的化学方程式为
前,II、III中沉淀由白色变为黑色的化学方程式为(2)对比实验I、II通入
 后的实验现象,对于二价锰化合物还原性的认识是
后的实验现象,对于二价锰化合物还原性的认识是(3)根据资料ⅱ,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入
 发生反应
发生反应 ,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。
,导致溶液的碱性减弱。但通过实验测定溶液的碱性变化很小。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①取III中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
 被
被②取II中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是
③从反应速率的角度,分析实验III未得到绿色溶液的可能原因
您最近一年使用:0次
10 . 用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如下图所示。
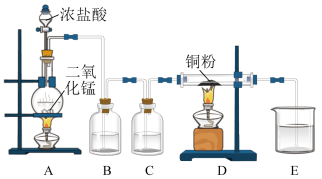
回答下列问题:
(1)写出在A中发生反应的化学方程式为:___________
(2)B中选用的试剂是___________ ,其作用是___________ ;
(3)E中选用的试剂是___________ ,其作用是___________ ;
(4)若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是___________
(5)甲同学依次进行了 与①钠、②铜、③氢气、④水反应的实验。上述反应中属于氧化还原反应的是
与①钠、②铜、③氢气、④水反应的实验。上述反应中属于氧化还原反应的是___________ (填序号)。
(6)甲同学探究氯气能否与水发生反应
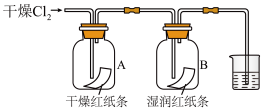
①B中纸条褪色,结合化学方程式解释原因:___________ 。
②装置A的作用是___________ 。
③烧杯中发生反应的化学方程式为___________

回答下列问题:
(1)写出在A中发生反应的化学方程式为:
(2)B中选用的试剂是
(3)E中选用的试剂是
(4)若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是
(5)甲同学依次进行了
 与①钠、②铜、③氢气、④水反应的实验。上述反应中属于氧化还原反应的是
与①钠、②铜、③氢气、④水反应的实验。上述反应中属于氧化还原反应的是(6)甲同学探究氯气能否与水发生反应

①B中纸条褪色,结合化学方程式解释原因:
②装置A的作用是
③烧杯中发生反应的化学方程式为
您最近一年使用:0次



