1 . 钠、铁、镁等元素在生产生活中有广泛的用途,完成下列填空:
Ⅰ钠的重要化合物
(1)在水产养殖上,硫代硫酸钠常用于除去自来水中的氯气,理论上,去除1g的氯气需要0.56g硫代硫酸钠,反应的离子方程式为______ 。
(2)除去Al2O3中混有的Fe2O3,可将混合物溶于过量的盐酸,再加入Na2CO3调节pH使Fe3+沉淀完全而Al3+不沉淀,用化学用语及相应的离子方程式解释加入Na2CO3的目的______ 。
Ⅱ铁的重要化合物
(3)磷酸铁(FePO4•2H2O是难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。实验室可通过下列实验制备磷酸铁。
①称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤,反应加热的目的是______ 。
②向滤液中加入一定量H2O2氧化Fe2+,为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、______ 和______ 。
③将一定量的Na2HPO4溶液(溶液显碱性)加入到含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4•2H2O.若反应得到的FePO4•H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为______ 。
Ⅲ镁的重要化合物
(4)氧化镁和碳粉与氯气在一定条件下反应可制备氯化镁,若尾气可用足量的氢氧化钠溶液完全吸收,则生成的盐为______ 。
Ⅰ钠的重要化合物
(1)在水产养殖上,硫代硫酸钠常用于除去自来水中的氯气,理论上,去除1g的氯气需要0.56g硫代硫酸钠,反应的离子方程式为
(2)除去Al2O3中混有的Fe2O3,可将混合物溶于过量的盐酸,再加入Na2CO3调节pH使Fe3+沉淀完全而Al3+不沉淀,用化学用语及相应的离子方程式解释加入Na2CO3的目的
Ⅱ铁的重要化合物
(3)磷酸铁(FePO4•2H2O是难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。实验室可通过下列实验制备磷酸铁。
①称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤,反应加热的目的是
②向滤液中加入一定量H2O2氧化Fe2+,为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、
③将一定量的Na2HPO4溶液(溶液显碱性)加入到含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4•2H2O.若反应得到的FePO4•H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为
Ⅲ镁的重要化合物
(4)氧化镁和碳粉与氯气在一定条件下反应可制备氯化镁,若尾气可用足量的氢氧化钠溶液完全吸收,则生成的盐为
您最近一年使用:0次
2 . (1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应的化学方程式_____________ 漂白粉的有效成分是__________ (填化学式)。
(2)实验室制取氨气的化学方程式:__________________________________
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是______________ ;
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因___________________ 现象是:_________________________ 。反应的化学方程式:__________________________________
(5)碳酸钠水解反应的离子方程式(第一步):_________________________ 。
(6)铅蓄电池的负极反应式:_________________________ 。
(7)硫酸钡的沉淀溶解平衡:__________________________________ 。
(2)实验室制取氨气的化学方程式:
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因
(5)碳酸钠水解反应的离子方程式(第一步):
(6)铅蓄电池的负极反应式:
(7)硫酸钡的沉淀溶解平衡:
您最近一年使用:0次
名校
3 . 月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________ 。
(2)Na的原子结构示意图为______ 。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为______ 。
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为_________ 、_________ (写化学式)。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为
您最近一年使用:0次
2018-03-13更新
|
634次组卷
|
4卷引用:辽宁省普通高中2017-2018学年高二学业水平考试模拟化学试题
名校
4 . 次氯酸钠(NaClO)是漂白液的主要成分,次氯酸钠溶液可用于消毒、杀菌及水处理。一种生产次氯酸钠的工艺如图所示。
-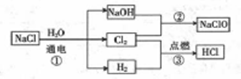
(1)Cl 元素位于元素周期表第______ 周期___ 族。
(2)写出NaOH的电子式:__________ 。
(3)写出反应②的化学方程式:_______________ 。该反应中每生成1mol NaClO时,转移______ mol 电子。
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是_____________________ (用离子方程式表示)。
-

(1)Cl 元素位于元素周期表第
(2)写出NaOH的电子式:
(3)写出反应②的化学方程式:
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是
您最近一年使用:0次
名校
5 . 已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入足量的氯气,二者恰好完全反应。生成Cl-、ClO-、ClO3-三种含氯元素的离子,其中ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
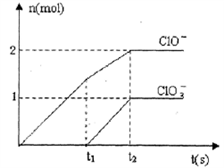
(1)t1时,开始有ClO3-生成的原因是___________________________ 。
(2)t2时,Ca(OH)2与Cl2发生反应的总的化学方程式为___________________________ 。
(3)该石灰乳中含有Ca(OH)2的物质的量是_________ mol。

(1)t1时,开始有ClO3-生成的原因是
(2)t2时,Ca(OH)2与Cl2发生反应的总的化学方程式为
(3)该石灰乳中含有Ca(OH)2的物质的量是
您最近一年使用:0次
名校
6 . 一定条件下,将一定体积的H2和Cl2的混合气体点燃,充分反应后,将混合气体通入含a mol NaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含有Cl-、ClO-、 且三者物质的量之比为8:1:1,则:
且三者物质的量之比为8:1:1,则:
(1)原混合气体中Cl2的物质的量为___________________ (用含a的数学式表示)。
(2)氢气和氯气的物质的量之比为____________________ 。
 且三者物质的量之比为8:1:1,则:
且三者物质的量之比为8:1:1,则:(1)原混合气体中Cl2的物质的量为
(2)氢气和氯气的物质的量之比为
您最近一年使用:0次
2016-12-09更新
|
342次组卷
|
3卷引用:浙江省诸暨市牌头中学2017-2018学年高二下学期期中考试化学试题
11-12高二上·甘肃张掖·期中
7 . 除去下列物质中混有的少量杂质,用有关反应的离子方程式表示:
(1)Fe2O3中混有Al2O3:___________________________________
(2)Na2CO3溶液中混有NaHCO3:__________________________
(3)FeCl2溶液中混有FeCl3:______________________________
(4)“84”消毒液是生活中常用的含氯消毒剂,其制备过程的主要反应是将氯气通入氢氧化钠溶液中,反应的化学方程式为________________________________________
(1)Fe2O3中混有Al2O3:
(2)Na2CO3溶液中混有NaHCO3:
(3)FeCl2溶液中混有FeCl3:
(4)“84”消毒液是生活中常用的含氯消毒剂,其制备过程的主要反应是将氯气通入氢氧化钠溶液中,反应的化学方程式为
您最近一年使用:0次



