1 . 根据题目信息,按要求完成下列填空:
(1)过氧化钠粉末与水反应的化学方程式:_____ 。
(2)实验室制取氨气(两种固体加热)的化学方程式:_____ 。
(3)二氧化硫通入溴水,可使溴水褪色,写出反应的化学方程式:_____ 。
(4)铜与浓硫酸加热条件下反应的化学方程式:_____ 。
(5)实验室制取氯气,多余的氯气可用氢氧化钠溶液吸收,写出反应的离子方程式:_____ 。
(6)三氟化氮(NF3)是一种无色无味的气体,27.0mLNF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:_____ 。
(1)过氧化钠粉末与水反应的化学方程式:
(2)实验室制取氨气(两种固体加热)的化学方程式:
(3)二氧化硫通入溴水,可使溴水褪色,写出反应的化学方程式:
(4)铜与浓硫酸加热条件下反应的化学方程式:
(5)实验室制取氯气,多余的氯气可用氢氧化钠溶液吸收,写出反应的离子方程式:
(6)三氟化氮(NF3)是一种无色无味的气体,27.0mLNF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:
您最近一年使用:0次
名校
解题方法
2 . 各类水处理剂能让水质得到提升达到饮用水的标准。生活中较常见的水处理剂有:氯气、次氯酸钠、漂白粉(主要成分为次氯酸钙)、二氧化氯、明矾、硫酸铁、高铁酸钠等等。
(1)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成 、
、 。请写出在加热时,当
。请写出在加热时,当 与
与 反应生成的
反应生成的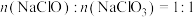 时,
时, 与
与 反应的化学方程式:
反应的化学方程式:_____ 。
(2)下列有关水资源及水质净化的说法,不正确的是_____(填字母)。
(3)高铁酸钠 是一种更为理想的水处理剂,除了能消毒杀菌,还有一个优点是
是一种更为理想的水处理剂,除了能消毒杀菌,还有一个优点是_____ 。
(1)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成
 、
、 。请写出在加热时,当
。请写出在加热时,当 与
与 反应生成的
反应生成的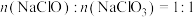 时,
时, 与
与 反应的化学方程式:
反应的化学方程式:(2)下列有关水资源及水质净化的说法,不正确的是_____(填字母)。
A.将自来水煮沸烧开后再饮用更健康、因为能除去残留的 及溶于其中的 及溶于其中的 |
| B.洗涤后得到的含磷污水是很好的肥料,可灌溉庄稼,能直接排放到自然界水体中 |
| C.煤、石油的燃烧和汽车排放的尾气都会引起大气污染,且会出现酸雨等环境问题 |
D.纳米铁粉可以高效地去除被污染水体中的 、 、 等重金属离子,其本质是纳米铁粉对重金属离子有较强的物理吸附 等重金属离子,其本质是纳米铁粉对重金属离子有较强的物理吸附 |
 是一种更为理想的水处理剂,除了能消毒杀菌,还有一个优点是
是一种更为理想的水处理剂,除了能消毒杀菌,还有一个优点是
您最近一年使用:0次
3 . 下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与FeCl3溶液 ⑤Cl2与NaOH溶液 ⑥Fe与HNO3溶液 ⑦Fe与H2SO4溶液 ⑧Na与O2
(1)由于浓度不同而发生不同氧化还原反应的是_______ (填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是_______ 。
(3)氧化还原反应不受浓度、温度影响的是_______ 。
(1)由于浓度不同而发生不同氧化还原反应的是
(2)由于温度不同而发生不同氧化还原反应的是
(3)氧化还原反应不受浓度、温度影响的是
您最近一年使用:0次
解题方法
4 . 写出下列反应的化学方程式,是离子反应的写离子方程式。
(1) 和
和 溶液的反应
溶液的反应_______ ;
(2) 和石灰乳的反应
和石灰乳的反应_______ ;
(3)把 通
通 溶液中
溶液中_______ ;
(4)将 和
和 混合通入
混合通入 中
中_______ ;
(5)将 通入氢硫酸溶液中
通入氢硫酸溶液中_______ ;
(6)将浓盐酸和 混合加热
混合加热_______ ;
(7)电解饱和食盐水_______ ;
(8)将浓盐酸与漂白液混合_______ ;
(9)向 固体滴加浓盐酸
固体滴加浓盐酸_______ ;
(10)向漂白粉溶液中通入少量 气体
气体_______ 。
(1)
 和
和 溶液的反应
溶液的反应(2)
 和石灰乳的反应
和石灰乳的反应(3)把
 通
通 溶液中
溶液中(4)将
 和
和 混合通入
混合通入 中
中(5)将
 通入氢硫酸溶液中
通入氢硫酸溶液中(6)将浓盐酸和
 混合加热
混合加热(7)电解饱和食盐水
(8)将浓盐酸与漂白液混合
(9)向
 固体滴加浓盐酸
固体滴加浓盐酸(10)向漂白粉溶液中通入少量
 气体
气体
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
5 . 分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为_______ ;(CN)2称为“拟卤素”,具有类似Cl2的化学性质,则(CN)2与NaOH水溶液反应的化学方程式为_______ 。
您最近一年使用:0次
解题方法
6 . 工业上是将氯气通入到 的
的 溶液中来制备
溶液中来制备 溶液,若
溶液,若 溶液中
溶液中 的质量分数为
的质量分数为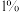 ,则生产
,则生产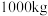 该溶液需消耗氯气的质量为
该溶液需消耗氯气的质量为_______  (保留整数)。
(保留整数)。
 的
的 溶液中来制备
溶液中来制备 溶液,若
溶液,若 溶液中
溶液中 的质量分数为
的质量分数为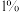 ,则生产
,则生产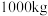 该溶液需消耗氯气的质量为
该溶液需消耗氯气的质量为 (保留整数)。
(保留整数)。
您最近一年使用:0次
7 . FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。常见水处理剂还有高铁酸盐及ClO2,请回答下列问题:
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式________________ ;高铁酸盐是一种绿色净水剂,其有效成分是高铁酸根FeO 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:_______________
(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为___________
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式_________________
(4)描述实验室制备氢氧化铁胶体的方法______________ ;写出对应的化学方程式_______________
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:_____ 。
___________ClO + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式
 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式
(4)描述实验室制备氢氧化铁胶体的方法
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:
___________ClO
 + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
您最近一年使用:0次
8 . 一种生产高铁酸钾的流程如图所示,写出下列反应的离子方程式
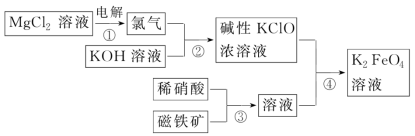
(1)反应①:_______
(2)反应②:_______
(3)反应③:_______
(4)反应④:_______

(1)反应①:
(2)反应②:
(3)反应③:
(4)反应④:
您最近一年使用:0次
名校
9 . 氯气是一种重要的化工原料,在生产生活中具有广泛的应用。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式_______ 。若产生标准状况下4.48 LCl2,则反应过程中被氧化的HCl的物质的量是_______ mol。
②为了防止氯气污染环境,需将剩余氯气通入_______ ,发生的化学反应方程式_______ 。
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下: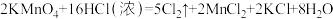 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是_______ (填写字母)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式_______ 。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式
②为了防止氯气污染环境,需将剩余氯气通入
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
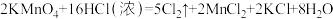 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式
您最近一年使用:0次
2022高三·全国·专题练习
10 . 实验室利用下图装置制备溴苯和硫酸锰。已知反应原理为MnO2 + 2NaBr + 2H2SO4 MnSO4+Na2SO4 +Br2↑+2H2O
MnSO4+Na2SO4 +Br2↑+2H2O
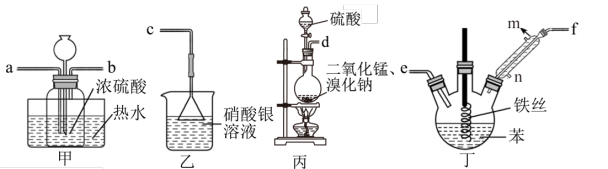
反应结束后,装置丁中液体因溶解了Br2而呈棕褐色,请用离子方程式表示洗去Br2的方法___________ ,干燥之后分离出产物溴苯的方法为___________ 。
 MnSO4+Na2SO4 +Br2↑+2H2O
MnSO4+Na2SO4 +Br2↑+2H2O
反应结束后,装置丁中液体因溶解了Br2而呈棕褐色,请用离子方程式表示洗去Br2的方法
您最近一年使用:0次



