名校
解题方法
1 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
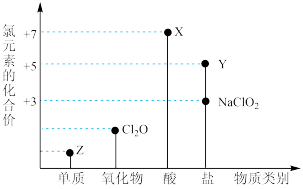
回答下列问题:
(1)X的电离方程式为_________ 。
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为71:48,则m:n=_________ 。
(3) NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式_____________ 。
(4)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的___________ 倍(还原产物都为Cl-,消毒效率以单位物质的量得到的电子数表示)。
(5)Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为_____________ 。
(6)自来水中的 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出在碱性条件下用Al粉还原
的浓度,某研究人员提出在碱性条件下用Al粉还原 ,产物是N2。发生的反应可表示如下,请完成方程式的配平:
,产物是N2。发生的反应可表示如下,请完成方程式的配平:___ Al+ ____  +
+ _____ =___  +
+ _____ N2↑ + _______ H2O

回答下列问题:
(1)X的电离方程式为
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为71:48,则m:n=
(3) NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式
(4)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的
(5)Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为
(6)自来水中的
 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出在碱性条件下用Al粉还原
的浓度,某研究人员提出在碱性条件下用Al粉还原 ,产物是N2。发生的反应可表示如下,请完成方程式的配平:
,产物是N2。发生的反应可表示如下,请完成方程式的配平: +
+  +
+
您最近一年使用:0次
2020-06-15更新
|
101次组卷
|
2卷引用:江西省南昌市八一中学2019-2020学年高一下学期期中考试化学试题
2 . 现有下列物质(括号内为对应物质的主要成分):a.熔融NaOH;b.医用酒精;c.蔗糖晶体;d.加碘盐(NaCl和KIO3);e.“84”消毒液(NaClO);f.小苏打(NaHCO3);g.洁厕灵(HCl),回答下列问题:
(1)上述状态下的物质中,属于电解质且能导电的是_______ (填字母,下同);d和f均为厨房中的常用物质,可用于区分两者的物质是________ 。
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:________ 。
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:___________ ;该反应中被氧化的Ⅰ原子与被还原的Ⅰ原子的个数之比为___________ 。
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:_____ ,__NaClO2+__NaHSO4=___ClO2+___NaCl+__Na2SO4+____H2O;若每片泡腾片中NaClO2的质量分数≥17%为合格品,上述所得ClO2溶液的物质的量浓度为0.002mol/L,则所用泡腾片____ (填“属于”或“不属于”)合格品。
(1)上述状态下的物质中,属于电解质且能导电的是
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:
您最近一年使用:0次
24-25高一上·全国·假期作业
解题方法
3 . 某校高一化学研究性学习小组对氯气在日常生活中的用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等。
(1)氯气可以用于漂白、消毒的原因是氯气能与水反应,生成具有漂白、消毒作用的___________ (填名称),相关反应的离子方程式为___________ 。
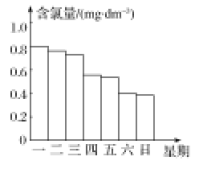
(2)在调查某室外大型游泳池夏季池水消毒情况时,该小组成员了解到,游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池水中的含氯量(有效氯)控制在 时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?
时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?___________ 。
(3)根据下图判断,你认为哪几天的天气炎热、阳光强烈?___________ ,请写出可能的原因:___________ (用化学方程式表示)。
(4)小型游泳池通常使用漂白液(含 的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:
的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:___________ (写出一个即可);用化学方程式说明工业上生产漂白液的原理:___________ 。
(1)氯气可以用于漂白、消毒的原因是氯气能与水反应,生成具有漂白、消毒作用的
(2)在调查某室外大型游泳池夏季池水消毒情况时,该小组成员了解到,游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池水中的含氯量(有效氯)控制在
 时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?
时,效果最好。如图是该小组测定的某周每天19:00时游泳池水中的含氯量,则哪几天使用游泳池相对不太安全?(3)根据下图判断,你认为哪几天的天气炎热、阳光强烈?

(4)小型游泳池通常使用漂白液(含
 的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:
的溶液)而非氯气来消毒,试举出使用漂白液而非氯气消毒的理由:
您最近一年使用:0次
名校
4 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)在新制氯水中加入紫色石蕊试液的现象是_______ 。
(2)现设计实验由大理石、水、氯气来制取漂白粉:
大理石 漂白粉溶液
漂白粉溶液 漂白粉
漂白粉
制取漂白粉溶液的过程中,发生反应的化学方程式为_______ 。漂白粉失效的化学方程式为_______ 。
(3)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。居家消毒时,不能将“84”消毒液与洁厕灵(有效成分为盐酸)混合使用,原因是_______ 。
(4)某同学用排空气法收集一瓶氯气并进行氯气与铁反应的实验:取一根细铁丝,用砂纸将铁丝擦至光亮,用坩埚钳夹住,在酒精灯上烧至红热,铁丝保持红热,然后立即伸入充满氯气的集气瓶中,观察到的现象是_______ 。向反应后的集气瓶中加入适量的蒸馏水,振荡,观察到的现象是_______ 。
(1)在新制氯水中加入紫色石蕊试液的现象是
(2)现设计实验由大理石、水、氯气来制取漂白粉:
大理石
 漂白粉溶液
漂白粉溶液 漂白粉
漂白粉制取漂白粉溶液的过程中,发生反应的化学方程式为
(3)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。居家消毒时,不能将“84”消毒液与洁厕灵(有效成分为盐酸)混合使用,原因是
(4)某同学用排空气法收集一瓶氯气并进行氯气与铁反应的实验:取一根细铁丝,用砂纸将铁丝擦至光亮,用坩埚钳夹住,在酒精灯上烧至红热,铁丝保持红热,然后立即伸入充满氯气的集气瓶中,观察到的现象是
您最近一年使用:0次
名校
解题方法
5 . 含氯消毒剂在生产、生活中有着广泛的用途。
(1)工业上将Cl2溶于一定浓度的NaOH溶液,可制得“84”消毒液,反应的离子方程式为___________ 。
(2)“84”消毒液(主要成分是NaClO)不能和洁厕灵(主要成分是浓盐酸)混用。混用时反应的化学方程式为___________ 。
(3)工业上常用石灰乳和Cl2反应制取漂粉精,其主要设备是氯化塔,将含有3%~6%水分的石灰乳从塔顶喷洒而入,Cl2从塔的最底层通入。这样加料的目的是___________ 。处理从氯化塔中逸出气体的方法是___________ 。
(4)在用ClO2进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+,生成 和MnO2的离子方程式为
和MnO2的离子方程式为___________ 。
(1)工业上将Cl2溶于一定浓度的NaOH溶液,可制得“84”消毒液,反应的离子方程式为
(2)“84”消毒液(主要成分是NaClO)不能和洁厕灵(主要成分是浓盐酸)混用。混用时反应的化学方程式为
(3)工业上常用石灰乳和Cl2反应制取漂粉精,其主要设备是氯化塔,将含有3%~6%水分的石灰乳从塔顶喷洒而入,Cl2从塔的最底层通入。这样加料的目的是
(4)在用ClO2进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+,生成
 和MnO2的离子方程式为
和MnO2的离子方程式为
您最近一年使用:0次
名校
解题方法
6 . 含氯化合物在生产生活中具有广泛的用途。氯及其化合物的“价一类”二维图如图所示,回答下列问题:
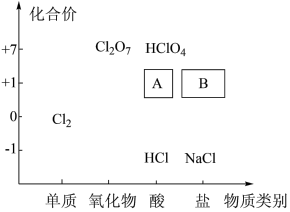
(1)自来水厂常将一定量氯气通入自来水进行消毒杀菌,用化学方程式解释为_____ ;其中具有杀菌作用的物质名称 为_____ ,实验室保存该物质的方法是将其置于_____ 试剂瓶中,_____ 保存。
(2)氯气与烧碱的反应可用于制备84消毒液,反应的化学方程式为_____ 。84消毒液的功能有_____ (填序号),其有效成分 应在“价类二维图“中的位置是_____ (选填A或B)
a.环境消毒b.器物杀菌c.织物漂白d.发酵食物
(3)某同学利用以下试剂研究HClO的性质,并进行了如下预测:
a.NaOHb.NaHCO3c.紫色石蕊试剂
从物质类别角度看,HClO具有酸性,可能与_____ 发生反应;(填标号,下同)
从化合价角度看,HClO具有氧化性,可能与_____ 发生反应;
从稳定性角度看,HClO具有不稳定性,反应的化学方程式为_____ 。
(4)漂白粉也具有和84消毒液类似的作用,漂白粉的有效成分是_____ (填化学式),漂白粉生效的化学方程式为_____ 。

(1)自来水厂常将一定量氯气通入自来水进行消毒杀菌,用化学方程式解释为
(2)氯气与烧碱的反应可用于制备84消毒液,反应的化学方程式为
a.环境消毒b.器物杀菌c.织物漂白d.发酵食物
(3)某同学利用以下试剂研究HClO的性质,并进行了如下预测:
a.NaOHb.NaHCO3c.紫色石蕊试剂
从物质类别角度看,HClO具有酸性,可能与
从化合价角度看,HClO具有氧化性,可能与
从稳定性角度看,HClO具有不稳定性,反应的化学方程式为
(4)漂白粉也具有和84消毒液类似的作用,漂白粉的有效成分是
您最近一年使用:0次
解题方法
7 . 氯元素的单质及其化合物在生产、生活中均有重要用途。请结合相关知识回答下列问题:
(1)84消毒液能有效杀灭新冠病毒,其主要成分为NaClO,在常温下,将氯气通入烧碱中可以得到NaClO,写出该反应的离子方程式___________ ,使用说明中特别提醒84消毒液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生 ,请用离子方程式表示其原因
,请用离子方程式表示其原因___________ 。
(2)世界卫生组织(WHO)和中国卫健委公认二氧化氯( )为新时代绿色消毒剂。工业上可采用
)为新时代绿色消毒剂。工业上可采用 与氯酸钠在硫酸存在的条件下反应制取
与氯酸钠在硫酸存在的条件下反应制取 ,并生成
,并生成 ,写出工业上制取
,写出工业上制取 反应的化学方程式
反应的化学方程式___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(3)现测定二氧化氯漂白液的浓度。步骤如下:量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再加入硫酸和10%碘化钾10mL,此时溶液出现棕色(发生反应: ,然后再逐滴滴入0.12
,然后再逐滴滴入0.12 硫代硫酸钠溶液15mL,恰好完全反应(发生反应:
硫代硫酸钠溶液15mL,恰好完全反应(发生反应: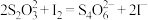 ,计算该漂白液中二氧化氯的物质的量浓度:
,计算该漂白液中二氧化氯的物质的量浓度:___________ 。
(4)实验室要配制1L 0.2 的NaClO溶液。配制过程如下:
的NaClO溶液。配制过程如下:
①将已恢复至室温的溶液沿玻璃棒注入1L容量瓶中。
②盖好容量瓶瓶塞,反复上下颠倒,摇匀。
③用天平准确称取14.9g的NaClO固体并放入烧杯中,加入约30mL的蒸馏水充分搅拌、溶解。
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡。
⑤定容。
⑥将配置好的溶液倒入试剂瓶中,贴好标签。
实验操作顺序依次为___________ (填序号),定容的具体操作是___________ 。
(1)84消毒液能有效杀灭新冠病毒,其主要成分为NaClO,在常温下,将氯气通入烧碱中可以得到NaClO,写出该反应的离子方程式
 ,请用离子方程式表示其原因
,请用离子方程式表示其原因(2)世界卫生组织(WHO)和中国卫健委公认二氧化氯(
 )为新时代绿色消毒剂。工业上可采用
)为新时代绿色消毒剂。工业上可采用 与氯酸钠在硫酸存在的条件下反应制取
与氯酸钠在硫酸存在的条件下反应制取 ,并生成
,并生成 ,写出工业上制取
,写出工业上制取 反应的化学方程式
反应的化学方程式(3)现测定二氧化氯漂白液的浓度。步骤如下:量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再加入硫酸和10%碘化钾10mL,此时溶液出现棕色(发生反应:
 ,然后再逐滴滴入0.12
,然后再逐滴滴入0.12 硫代硫酸钠溶液15mL,恰好完全反应(发生反应:
硫代硫酸钠溶液15mL,恰好完全反应(发生反应: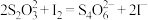 ,计算该漂白液中二氧化氯的物质的量浓度:
,计算该漂白液中二氧化氯的物质的量浓度:(4)实验室要配制1L 0.2
 的NaClO溶液。配制过程如下:
的NaClO溶液。配制过程如下:①将已恢复至室温的溶液沿玻璃棒注入1L容量瓶中。
②盖好容量瓶瓶塞,反复上下颠倒,摇匀。
③用天平准确称取14.9g的NaClO固体并放入烧杯中,加入约30mL的蒸馏水充分搅拌、溶解。
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡。
⑤定容。
⑥将配置好的溶液倒入试剂瓶中,贴好标签。
实验操作顺序依次为
您最近一年使用:0次
8 . 利用分类法可以更系统、全面的认识物质的性质以及化学反应。
Ⅰ、有下列物质:①盐酸② ③
③ ④KOH溶液⑤
④KOH溶液⑤
(1)属于碱性氧化物的是___________ (填序号)。
(2)③属于___________ (填“共价”或“离子”)化合物。
(3)属于电解质的是___________ (填序号)。
(4)①和④反应的离子方程式是___________ 。
Ⅱ、有以下四个反应:①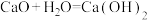 ②
②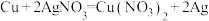
③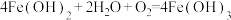 ④
④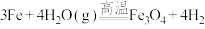
(5)不属于氧化还原反应的是___________ (填序号)。
(6)既是化合反应又是氧化还原反应的是___________ (填序号)。
Ⅲ、单质到盐的转化关系可表示为:A(单质)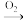 B(氧化物)
B(氧化物)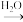 C
C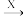 D(盐)。
D(盐)。
(7)若A是碳单质,则C的水溶液呈___________ (填“酸”、“碱”或“中”)性。
(8)若C→D的转化可用于工业制漂白粉,则物质X是___________ 。
(9)若B是一种淡黄色固体,X是 ,则B的用途是
,则B的用途是___________ (举一例),D的化学式可能是___________ 。
Ⅰ、有下列物质:①盐酸②
 ③
③ ④KOH溶液⑤
④KOH溶液⑤
(1)属于碱性氧化物的是
(2)③属于
(3)属于电解质的是
(4)①和④反应的离子方程式是
Ⅱ、有以下四个反应:①
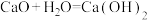 ②
②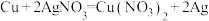
③
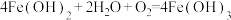 ④
④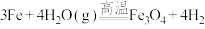
(5)不属于氧化还原反应的是
(6)既是化合反应又是氧化还原反应的是
Ⅲ、单质到盐的转化关系可表示为:A(单质)
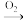 B(氧化物)
B(氧化物)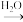 C
C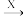 D(盐)。
D(盐)。(7)若A是碳单质,则C的水溶液呈
(8)若C→D的转化可用于工业制漂白粉,则物质X是
(9)若B是一种淡黄色固体,X是
 ,则B的用途是
,则B的用途是
您最近一年使用:0次
9 . 氯是重要的非金属元素,研究它的性质及用途对生产, 生活、科研具有重要意义。
(1)一氯胺(NH2Cl)是一种长效缓释水消毒剂,在中性或酸性环境中会发生反应,生成一种具有强烈杀菌作用的物质,该物质为_______ 。工业上可利用NH3和Cl2反应制备一氯胺; 生成1molNH2Cl时,转移的电子数目为_______ 。
(2)Cl2 与NaOH溶液反应可制取“84消毒液。
用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3), 此时ClO-的浓度为c0mol/L;加热时NaClO能转化为NaClO3,测得t时刻溶液中ClO-的浓度为c1 mol/L (不考虑加热前后溶液体积的变化)。
①用24gNaOH配成250mL溶液时,c(NaOH)=_______ mol/L。
②写出溶液中NaClO分解生成NaClO3的化学方程式:_______ 。
③t时刻溶液中c(Cl-)=_______ mol/L(用含c0、c1的代数式表示)。
(1)一氯胺(NH2Cl)是一种长效缓释水消毒剂,在中性或酸性环境中会发生反应,生成一种具有强烈杀菌作用的物质,该物质为
(2)Cl2 与NaOH溶液反应可制取“84消毒液。
用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3), 此时ClO-的浓度为c0mol/L;加热时NaClO能转化为NaClO3,测得t时刻溶液中ClO-的浓度为c1 mol/L (不考虑加热前后溶液体积的变化)。
①用24gNaOH配成250mL溶液时,c(NaOH)=
②写出溶液中NaClO分解生成NaClO3的化学方程式:
③t时刻溶液中c(Cl-)=
您最近一年使用:0次
解题方法
10 .  溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
(1)某同学设计如下实验研究 的性质:
的性质:
①理论上 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明 具有还原性的是实验
具有还原性的是实验_______ (填序号)。
(2)84消毒液的有效成分为 。
。
①NaClO中Cl元素的化合价是_______ 。
②84消毒液不能用于钢制器具的消毒,原因是 具有
具有_______ 性。
③84消毒液吸收空气中的 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为_______ 。
(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式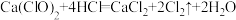 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:_______ 。
②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)_______ (填“能”或“不能”)同时使用,其原因是_______ 。
 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:(1)某同学设计如下实验研究
 的性质:
的性质:| 实验 | 操作 | 现象 |
| i | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是②能证明
 具有还原性的是实验
具有还原性的是实验(2)84消毒液的有效成分为
 。
。①NaClO中Cl元素的化合价是
②84消毒液不能用于钢制器具的消毒,原因是
 具有
具有③84消毒液吸收空气中的
 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式
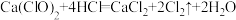 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)
您最近一年使用:0次



