名校
解题方法
1 . 下列装置所示的实验中,能达到实验目的的是
| A | B | C | D |
 | 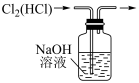 |  |  |
| 分离碘和酒精 | 除去Cl2中HCl | 实验室制氨气 | 排水法收集NO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-02-16更新
|
264次组卷
|
2卷引用:福建省平潭翰英中学2021-2022学年高一下学期第一次月考化学试题
2 . 化学在治理空气污染方面发挥着重要的作用。
I、化石燃料的过度使用是导致酸雨的主要原因。研究表明,NOx、SO2形成酸雨时的转化关系如图所示:
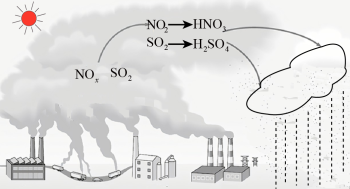
(1)HNO3的电离方程式为_______ 。
(2)SO2会被雨水吸收形成酸雨,这种酸雨在空气中久置酸性增强的原因是_______ (用化学方程式表示)。
Ⅱ、NOx、SO2等均为大气污染物,需处理后才能排放。
(3)用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.
ii.
①反应i中,每消耗0.3molNO2,转移电子数为_______ 。
②反应ii中,氧化剂和还原剂的物质的量之比为_______ 。
(4)用氨水可以吸收SO2制取铵盐。
①实验室用NH4Cl和Ca(OH)2制取NH3的化学方程式为_______ 。
②用足量氨水吸收SO2的化学方程式为_______ 。
(5)利用NaClO吸收液可在脱除烟气中NOx的同时脱除SO2。研究发现在不同的初始pH条件下,吸收液对流动烟气的脱硫效率都接近100%,而对NO的脱除率如下图所示。
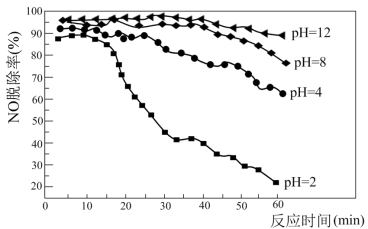
pH=2时,脱除SO2的离子方程式为_______ ;脱硝效率随反应时间的延长而逐渐降低的可能原因是_______ 。
I、化石燃料的过度使用是导致酸雨的主要原因。研究表明,NOx、SO2形成酸雨时的转化关系如图所示:

(1)HNO3的电离方程式为
(2)SO2会被雨水吸收形成酸雨,这种酸雨在空气中久置酸性增强的原因是
Ⅱ、NOx、SO2等均为大气污染物,需处理后才能排放。
(3)用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.

ii.

①反应i中,每消耗0.3molNO2,转移电子数为
②反应ii中,氧化剂和还原剂的物质的量之比为
(4)用氨水可以吸收SO2制取铵盐。
①实验室用NH4Cl和Ca(OH)2制取NH3的化学方程式为
②用足量氨水吸收SO2的化学方程式为
(5)利用NaClO吸收液可在脱除烟气中NOx的同时脱除SO2。研究发现在不同的初始pH条件下,吸收液对流动烟气的脱硫效率都接近100%,而对NO的脱除率如下图所示。

pH=2时,脱除SO2的离子方程式为
您最近一年使用:0次
名校
3 . 某中学化学研究性学习小组利用消石灰和氯化铵制取氨气,装置如下制取并探究氨气的性质。

【实验探究】
(1)写出A中反应的化学方程式___________ ,该反应___________ (填“是”或“不是”)氧化还原反应。
(2)A装置还可用于制取气体___________ (只填一种)
(3)若有10.7g 固体,最多可制取
固体,最多可制取 (标准状况)的体积是
(标准状况)的体积是___________ L
(4)实验室收集氨气的方法是___________
(5)C、D装置中颜色会发生变化的是___________ (填“C”或“D”)
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到的现象是________________ ,原因是___________ (用化学方程式表示)。
(7)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是___________ (填序号)。


【实验探究】
(1)写出A中反应的化学方程式
(2)A装置还可用于制取气体
(3)若有10.7g
 固体,最多可制取
固体,最多可制取 (标准状况)的体积是
(标准状况)的体积是(4)实验室收集氨气的方法是
(5)C、D装置中颜色会发生变化的是
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到的现象是
(7)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是

您最近一年使用:0次
4 . 人类从自然界中获取各种化学物质。
(1)从化石燃料可以获得多种有机物。
①苯的分子式为_______ 。
②甲烷和乙烯是否互为同系物?_______ (填“是”或“否”)
③正丁烷的同分异构体结构简式为_______
(2)从矿石中可以获取多种材料
①常用的金属冶炼方法有①热分解法、②高温还原法和③电解法等
铝的冶炼属于_______ (选填序号)
②铝合金成本低,性能优异.多数合金的熔点_______ (填“高”或“低”)于它的任何一种成分金属
③光导纤维的主要成分为_______ (填化学式)
(3)氮元素的化合价与其形成物质类别的关系如图所示。回答下列问题:
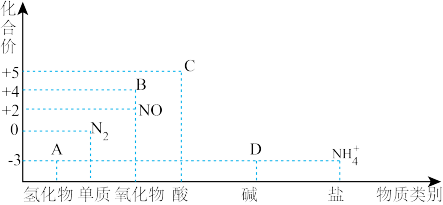
①物质A的水溶液呈_______ (填“酸性”或“碱性”)
②物质C光照易分解,该反应_______ (填“属于”或“不属于”)氧化还原反应
③ 固体和
固体和 固体共热制取氨气的化学方程式为
固体共热制取氨气的化学方程式为_______
(1)从化石燃料可以获得多种有机物。
①苯的分子式为
②甲烷和乙烯是否互为同系物?
③正丁烷的同分异构体结构简式为
(2)从矿石中可以获取多种材料
①常用的金属冶炼方法有①热分解法、②高温还原法和③电解法等
铝的冶炼属于
②铝合金成本低,性能优异.多数合金的熔点
③光导纤维的主要成分为
(3)氮元素的化合价与其形成物质类别的关系如图所示。回答下列问题:

①物质A的水溶液呈
②物质C光照易分解,该反应
③
 固体和
固体和 固体共热制取氨气的化学方程式为
固体共热制取氨气的化学方程式为
您最近一年使用:0次
2022-07-06更新
|
262次组卷
|
2卷引用:福建省泉州市2021-2022学年高一下学期期末教学质量监测化学试题
5 . Ⅰ.某实验小组利用以下装置制取氨气并探究氨气的性质:
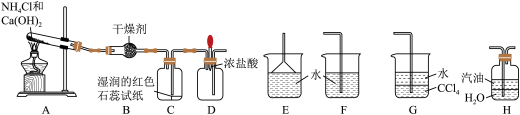
(1)装置A中发生反应的化学方程式为___________ 。
(2)装置B中的干燥剂是___________ (填名称)。
(3)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________
(4)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是___________ (填“E”、“F”、“G”或“H”)。
Ⅱ.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

(5)无水硫酸铜的作用是检验生成的水;有同学认为需要在无水硫酸铜的后面再接一个装有 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是___________ 。
(6)实验中观察到a中CuO粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为___________ 。

(1)装置A中发生反应的化学方程式为
(2)装置B中的干燥剂是
(3)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(4)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是
Ⅱ.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

(5)无水硫酸铜的作用是检验生成的水;有同学认为需要在无水硫酸铜的后面再接一个装有
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(6)实验中观察到a中CuO粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
您最近一年使用:0次
2023-04-16更新
|
296次组卷
|
2卷引用:福建省福州第三中学2022-2023学年高一下学期期中考试化学试题
6 . 各装置图的叙述中,正确的是
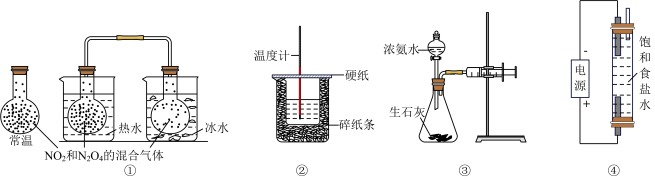

| A.①图证明温度对平衡移动的影响 |
| B.②装置能测定中和热 |
| C.③注射器活塞向右移,说明该反应为放热反应 |
| D.④装置用于制备含NaClO的消毒液 |
您最近一年使用:0次
2023-11-18更新
|
205次组卷
|
2卷引用:福建省漳州市十校2023-2024学年高二上学期期中联考化学试题
解题方法
7 . 氮及硫的化合物在化工生产中扮演着重要角色。下列说法不正确的是
| A.氨气可以使湿润的红色石蕊试纸变蓝 |
| B.实验室制取NH3可以使用NH4Cl和Ca(OH)2 |
| C.检验硫酸根需先加稀盐酸酸化,再加氯化钡溶液 |
| D.向蔗糖中加入浓硫酸时,蔗糖变黑体现了浓硫酸的吸水性 |
您最近一年使用:0次
2022-01-11更新
|
498次组卷
|
3卷引用:福建省德化第二中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
8 . 下列实验能达到实验目的的是
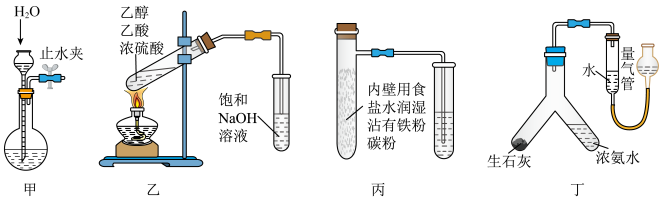
| A.图甲:检查装置的气密性 | B.图乙:实验室制取乙酸乙酯 |
| C.图丙:研究铁的析氢腐蚀 | D.图丁: 测量产生 N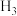 的体积 的体积 |
您最近一年使用:0次
2024-05-02更新
|
239次组卷
|
2卷引用:福建省福州市2023-2024学年高三下学期4月末质量检测(三模)化学试题
解题方法
9 . 硫氰酸钾(KSCN),是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。某化学小组用下图实验装置模拟工业制备硫氰酸钾,并进行相关实验探究。
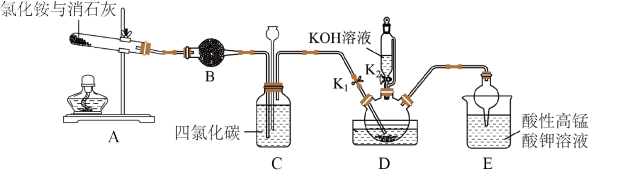
已知:①NH3不溶于CCl4和CS2,CS2不溶于水且密度比水大;
②D中三颈烧瓶内盛放CS2、水和催化剂,发生反应CS2+3NH3 NH4SCN+NH4HS;③NH4SCN在高于170℃时易分解,NH4HS在高于25℃时即分解。
NH4SCN+NH4HS;③NH4SCN在高于170℃时易分解,NH4HS在高于25℃时即分解。
回答下列问题:
(1)装置B的仪器名称是___________ 。
(2)制备KSCN溶液:将D中反应混合液加热至105℃,打开K1通入氨气。
①反应一段时间后,关闭K1,此时装置C中观察到的现象是___________ ,加热方式采用油浴不使用水浴加热的原因是___________ 。
②打开K2,缓缓滴入适量的KOH溶液,继续保持反应混合液温度为105℃。写出装置D中生成KSCN的化学方程式___________ 。
(3)E的作用是吸收尾气中的___________ (填化学式)。
(4)制备硫氰酸钾晶体:先滤去三颈烧瓶中的固体催化剂,再经___________ (填操作名称)、减压蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰酸钾晶体。

已知:①NH3不溶于CCl4和CS2,CS2不溶于水且密度比水大;
②D中三颈烧瓶内盛放CS2、水和催化剂,发生反应CS2+3NH3
 NH4SCN+NH4HS;③NH4SCN在高于170℃时易分解,NH4HS在高于25℃时即分解。
NH4SCN+NH4HS;③NH4SCN在高于170℃时易分解,NH4HS在高于25℃时即分解。回答下列问题:
(1)装置B的仪器名称是
(2)制备KSCN溶液:将D中反应混合液加热至105℃,打开K1通入氨气。
①反应一段时间后,关闭K1,此时装置C中观察到的现象是
②打开K2,缓缓滴入适量的KOH溶液,继续保持反应混合液温度为105℃。写出装置D中生成KSCN的化学方程式
(3)E的作用是吸收尾气中的
(4)制备硫氰酸钾晶体:先滤去三颈烧瓶中的固体催化剂,再经
您最近一年使用:0次
解题方法
10 . 某小组同学在实验室设计实验验证物质的性质及其相互转化。
I.选用如图所示的装置进行实验。

回答下列问题:
(1)实验室用 与
与 反应制取
反应制取 的发生装置为
的发生装置为___________ (填标号),该反应的化学方程式为___________________ , 的尾气处理装置为
的尾气处理装置为___________ (填标号)。
(2)实验室用 与稀硝酸反应制取NO,该气体的收集装置为
与稀硝酸反应制取NO,该气体的收集装置为___________ (填标号)。
II.设计了如图所示的实验装置模拟工业生产制备少量硝酸。
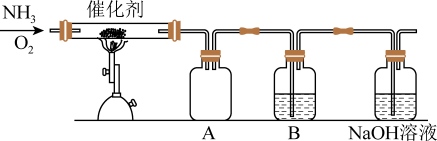
(3)B中试剂为___________ , 溶液的作用是
溶液的作用是___________ 。
(4)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是___________ ,白烟的化学式是___________ 。
②欲检验尾气中是否含有氨气的方法是___________ 。
(5)工业生产中常用氨气检查输送氯气的管道是否有 泄漏。若
泄漏。若 有泄漏,可以观察到有大量的白烟生成(为
有泄漏,可以观察到有大量的白烟生成(为 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:_____ 。
I.选用如图所示的装置进行实验。

回答下列问题:
(1)实验室用
 与
与 反应制取
反应制取 的发生装置为
的发生装置为 的尾气处理装置为
的尾气处理装置为(2)实验室用
 与稀硝酸反应制取NO,该气体的收集装置为
与稀硝酸反应制取NO,该气体的收集装置为II.设计了如图所示的实验装置模拟工业生产制备少量硝酸。

(3)B中试剂为
 溶液的作用是
溶液的作用是(4)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是
②欲检验尾气中是否含有氨气的方法是
(5)工业生产中常用氨气检查输送氯气的管道是否有
 泄漏。若
泄漏。若 有泄漏,可以观察到有大量的白烟生成(为
有泄漏,可以观察到有大量的白烟生成(为 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次



