1 . 如下图所示,某同学利用Na2SO3和浓H2SO4制取SO2并探究其性质。

(1)写出装置B中发生反应的离子方程式:___________ 。
(2)装置C中的实验现象是___________ ,该实验现象说明SO2具有___________ 性。
(3)能验证SO2具有酸性氧化物的通性的实验现象是___________ 。
(4)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:___________ 。
(5)探究H2SO3的酸性强于HClO,该同学用如下图所示装置达成实验目的。
A.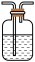 小苏打溶液B.
小苏打溶液B.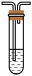 品红溶液C.
品红溶液C. 酸性KMnO4溶液D.
酸性KMnO4溶液D. 漂白粉溶液
漂白粉溶液
装置的连接顺序为纯净SO2→___________ (选填字母); D中反应的离子方程式为___________ 。

(1)写出装置B中发生反应的离子方程式:
(2)装置C中的实验现象是
(3)能验证SO2具有酸性氧化物的通性的实验现象是
(4)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:
(5)探究H2SO3的酸性强于HClO,该同学用如下图所示装置达成实验目的。
A.
 小苏打溶液B.
小苏打溶液B. 品红溶液C.
品红溶液C. 酸性KMnO4溶液D.
酸性KMnO4溶液D. 漂白粉溶液
漂白粉溶液装置的连接顺序为纯净SO2→
您最近一年使用:0次
2023-03-24更新
|
402次组卷
|
2卷引用:河北省石家庄市第二中学西校区2022-2023学年高一下学期3月月考化学试题
解题方法
2 . 用如图装置进行实验,可以达到实验目的的是
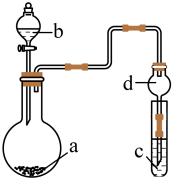

| 选项 | 溶液a | 固体b | 溶液c | 实验目的 |
| A | 70%的硫酸 | Na2SO3 | 石蕊溶液 | SO2具有漂白性 |
| B | 浓盐酸 | KMnO4 | Na2S溶液 | 氧化性:Cl2>S |
| C | 浓HNO3 | CaCO3 | Na2SiO3溶液 | 非金属性N>C>Si |
| D | 浓盐酸 | MnO2 | NaOH溶液 | 制备84消毒液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-16更新
|
110次组卷
|
2卷引用:河北省秦皇岛市青龙满族自治县2023届高三三模联考化学试题
3 . 利用下列装置进行实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 实验 目的 | 收集 气体 气体 | 制备 并检验其漂白性 并检验其漂白性 | 制备并收集 | 证明 易溶于水,且氨水显碱性 易溶于水,且氨水显碱性 |
| 实验 装置 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-02更新
|
158次组卷
|
3卷引用:河北省衡水市枣强中学2023-2024学年高一下学期第二次调研考试化学试题
名校
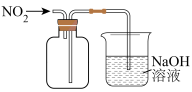
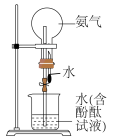
4 . 下列装置或操作能达到相应实验目的的是
| A | B | C | D |
 |  |  |  |
| 除去氯气中的HCl | 用此装置制备气体,测量生成气体的体积时,可以减少误差 | 实验室制取氨气 | 验证SO2漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-05-28更新
|
246次组卷
|
2卷引用:河北省石家庄二中2020-2021学年高一第二学期期中考试化学试题
5 . 用图示装置,不能达到实验目的的是
| A | B | C | D |
 |  | 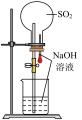 |  |
| 制取氨气 | 制备 | 进行喷泉实验 | 排水法收集 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 下列图示装置不能达到实验目的的是
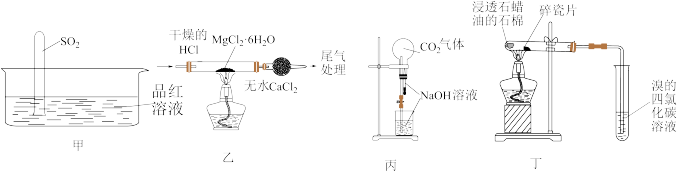

A.用甲装置验证 的溶解性和漂白性 的溶解性和漂白性 | B.用乙装置制备无水 |
| C.用丙装置做喷泉实验 | D.用丁装置证明石蜡油分解生成了乙烯 |
您最近一年使用:0次
名校
7 . 下列实验装置能达到相应实验目的的是

| A.图A是制备氯气 |
| B.图B是制备并检验SO2气体的性质 |
| C.图C是检查装置的气密性 |
| D.图D是收集NO |
您最近一年使用:0次
2022-03-17更新
|
480次组卷
|
5卷引用:河北省名校联盟2021-2022学年高一下学期4月联考化学试题
名校
8 . 用如图所示装置进行实验,仪器a、b、c中分别盛有试剂1、2、3,其中能达到实验目的的是
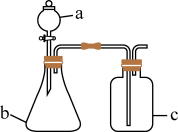

| 选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 |
| A | 浓盐酸 | MnO2 | 饱和食盐水 | 制备氯气 |
| B | 盐酸 | Na2CO3 | Na2SiO3溶液 | 验证碳的非金属性比硅强 |
| C | 盐酸 | Na2SO3 | 品红试液 | 验证SO2具有漂白性 |
| D | 稀硫酸 | 溶液X | 澄清石灰水 | 验证X溶液中是否有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-03-14更新
|
519次组卷
|
5卷引用:河北省衡水市第十四中学2020-2021学年高一下学期一调考试化学试题
9 . 运用化学反应原理研究硫单质及其化合物的反应,对生产、生活、环境保护等领域有着重要的意义。
学习小组在实验室中利用如图所示装置制备SO2并进行相关性质的探究。
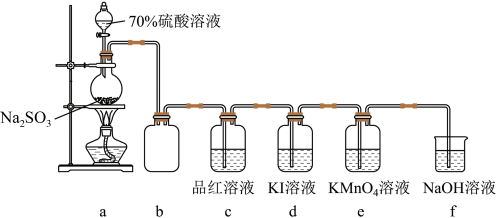
回答下列问题:
(1)实验用70%的硫酸而不用浓硫酸的原因是___________ 。
(2)装置e中出现___________ 填现象可证明SO2具有还原性,反应离子方程式为___________ 。
(3)实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:SO2+4I-+4H+ S↓+2I2+2H2O。
S↓+2I2+2H2O。
探究:SO2在KI溶液体系中的反应产物
有同学提出上述可逆反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO +2I-+4H+。
+2I-+4H+。
为进一步探究体系中的产物,完成下列实验方案。
综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为:___________ 。
(4)晶体碘酸钾(KIO3)是一种常用的食品添加剂,常用硫代硫酸钠滴定测定碘酸钾纯度:准确称取1.000gKIO3产品转移至200mL容量瓶中定容,精确量取20.00mL该溶液置于锥形瓶中,加入足量碘化钾,用5mL盐酸酸化(IO +5I−+6H+=3I2+3H2O),盖紧塞子,置于避光处3min,用0.1004mol/L硫代硫酸钠溶液滴定,当溶液呈淡黄色时,加入少许淀粉溶液,继续滴定至终点(I2+2S2O
+5I−+6H+=3I2+3H2O),盖紧塞子,置于避光处3min,用0.1004mol/L硫代硫酸钠溶液滴定,当溶液呈淡黄色时,加入少许淀粉溶液,继续滴定至终点(I2+2S2O =2I−+S4O
=2I−+S4O )。平行滴定三次,平均消耗0.1004mol/LNa2S2O3溶液的体积为25.00mL。
)。平行滴定三次,平均消耗0.1004mol/LNa2S2O3溶液的体积为25.00mL。
计算产品的纯度___________ 。(请写出计算过程,结果保留三位有效数字)。
学习小组在实验室中利用如图所示装置制备SO2并进行相关性质的探究。

回答下列问题:
(1)实验用70%的硫酸而不用浓硫酸的原因是
(2)装置e中出现
(3)实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:SO2+4I-+4H+
 S↓+2I2+2H2O。
S↓+2I2+2H2O。探究:SO2在KI溶液体系中的反应产物
有同学提出上述可逆反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO
 +2I-+4H+。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
| 方案 | 操作 | 预期现象 | 结论 |
| ⅰ | 取适量装置d中浊液,向其中滴加几滴① | 无明显变化 | 浊液中无I2 |
| ⅱ | 将装置d中浊液进行分离 | 得淡黄色固体和澄清溶液 | |
| 取适量分离后的澄清溶液于试管中,② | ③ | ④ |
(4)晶体碘酸钾(KIO3)是一种常用的食品添加剂,常用硫代硫酸钠滴定测定碘酸钾纯度:准确称取1.000gKIO3产品转移至200mL容量瓶中定容,精确量取20.00mL该溶液置于锥形瓶中,加入足量碘化钾,用5mL盐酸酸化(IO
 +5I−+6H+=3I2+3H2O),盖紧塞子,置于避光处3min,用0.1004mol/L硫代硫酸钠溶液滴定,当溶液呈淡黄色时,加入少许淀粉溶液,继续滴定至终点(I2+2S2O
+5I−+6H+=3I2+3H2O),盖紧塞子,置于避光处3min,用0.1004mol/L硫代硫酸钠溶液滴定,当溶液呈淡黄色时,加入少许淀粉溶液,继续滴定至终点(I2+2S2O =2I−+S4O
=2I−+S4O )。平行滴定三次,平均消耗0.1004mol/LNa2S2O3溶液的体积为25.00mL。
)。平行滴定三次,平均消耗0.1004mol/LNa2S2O3溶液的体积为25.00mL。计算产品的纯度
您最近一年使用:0次
2024-03-01更新
|
464次组卷
|
2卷引用:河北省曲阳县第一高级中学2023-2024学年高一下学期开学考试化学试题
10 . 一体化实验装置能够快速制备物质并检验其性质,具有现象明显、无污染、操作方便等优点。二氧化硫和硫化氢的制备及性质检验一体化实验装置如图所示(夹持装置略去)。
①检查装置气密性。
②打开K2,关闭K1,注射器2将浓硫酸缓慢注入乙试管,观察湿润蓝色石蕊试纸颜色变化。
③关闭K2,打开K1,观察到Y型管A、B两端溶液均褪色。
④注射器3将BaCl2溶液缓慢注入Y型管B端,有白色沉淀生成。
⑤……
⑥用酒精灯微热Y型管A端,观察溶液的颜色变化。
回答下列问题:
(1)步骤②乙试管中发生反应的化学方程式为_______ 。
(2)能说明二氧化硫是酸性氧化物的实验现象为_______ 。
(3)步骤④产生白色沉淀的离子方程式为_______ 。
(4)步骤⑤说明二氧化硫具有氧化性,则该步骤的实验操作为_______ 。
(5)步骤⑥溶液的颜色变化为_______ 。
(6)饱和氢氧化钠溶液的作用是_______ 。
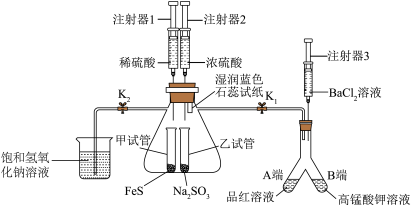
①检查装置气密性。
②打开K2,关闭K1,注射器2将浓硫酸缓慢注入乙试管,观察湿润蓝色石蕊试纸颜色变化。
③关闭K2,打开K1,观察到Y型管A、B两端溶液均褪色。
④注射器3将BaCl2溶液缓慢注入Y型管B端,有白色沉淀生成。
⑤……
⑥用酒精灯微热Y型管A端,观察溶液的颜色变化。
回答下列问题:
(1)步骤②乙试管中发生反应的化学方程式为
(2)能说明二氧化硫是酸性氧化物的实验现象为
(3)步骤④产生白色沉淀的离子方程式为
(4)步骤⑤说明二氧化硫具有氧化性,则该步骤的实验操作为
(5)步骤⑥溶液的颜色变化为
(6)饱和氢氧化钠溶液的作用是
您最近一年使用:0次
2023-01-12更新
|
341次组卷
|
4卷引用:河北省石家庄联邦外国语i学校2023-2024学年高一下学期期中考试化学试题