名校
解题方法
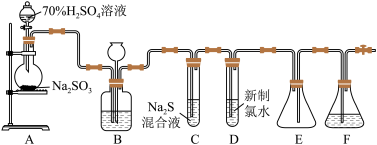
1 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。____ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择______ (填代号)。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案____ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为_____ 。
(5)装置E的作用是______ 。装置F中为_____ 溶液。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案
(5)装置E的作用是
您最近一年使用:0次
2024-04-04更新
|
125次组卷
|
2卷引用:天津市静海区第一中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
2 . 下图中实验装置能达到相应实验目的的是
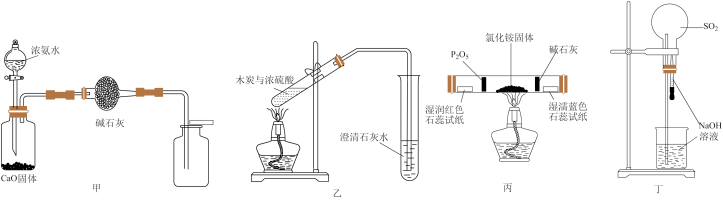
| A.装置甲可用于制备并收集少量干燥氨气 |
B.装置乙可用于验证反应是否有 生成 生成 |
| C.装置丙可用于检验氯化铵受热分解生成的两种气体 |
| D.装置丁可进行喷泉实验 |
您最近一年使用:0次
2023-03-18更新
|
990次组卷
|
8卷引用:天津市滨海新区塘沽第一中学2023-2024学年高一下学期第一次月考化学试卷
名校
3 . 下列有关实验装置进行的相应实验,不能达到实验目的的是
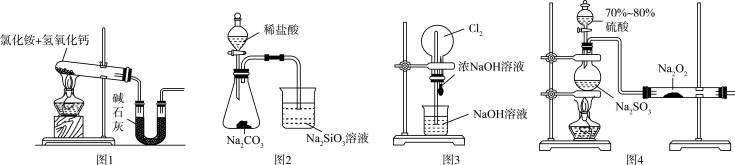
| A.用图1所示装置可制备得到干燥的氨气 |
| B.用图2所示装置证明:非金属性:C>Si |
| C.用图3所示装置可以完成“喷泉”实验 |
| D.用图4所示装置能观察到右边装置中淡黄色固体变白色 |
您最近一年使用:0次
2021-09-29更新
|
1009次组卷
|
15卷引用:天津市第二十一中学2022-2023学年高一下学期期中考试化学试题
天津市第二十一中学2022-2023学年高一下学期期中考试化学试题广东省广州市仲元中学2020-2021学年高一下学期期中考试化学试题广东省广州大学附属中学2021-2022学年高一下学期3月月考化学试题江西省赣州市信丰县第一中学2021-2022学年高一下学期期中考试化学试题江西省抚州市临川第二中学、临汝中学2021-2022学年高一下学期期中考试化学试题广东省广州市第一中学2021-2022学年高一下学期期中考试化学试题河南省郸城第一高级中学2021-2022学年高一下学期第二次月考化学试题广东省揭阳市揭东区2021-2022学年高一下学期期末考试化学试题广东省佛山市第四中学2022-2023学年高一下学期3月月考化学试卷广东省广州市第七中学2022-2023学年高一下学期期中考试化学试题广东省佛山市顺德市李兆基中学2022-2023学年高一下学期3月月考化学试题广东省湛江市坡头区第一中学2022-2023学年高一下学期期中考试化学试题广东省兴宁市沐彬中学2021-2022学年高一下学期期中段考化学试题广东省佛山市顺德区桂洲中学2023-2024学年高一下学期第一次联考模拟化学试题 安徽省淮北市第一中学2023-2024学年高一下学期3月月考化学试题
名校
4 . 某化学小组为了证明二氧化硫和氯气的漂白性,设计了如下图所示的实验装置:

他们制备二氧化硫和氯气所依据的原理分别是:
Na2SO3+H2SO4=Na2SO4+H2O+SO2↑
MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)用来制取氯气的装置是___________ (填字母),反应中浓盐酸所表现出的化学性质是___________ 和___________ 。
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,___________ (填“B”或“D”)试管中无明显现象。
(3)装置C的作用是___________ 。
(4)若装置D中品红溶液换成紫色石蕊溶液,则出现的现象是___________ 。
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1∶1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的离子方程式是___________ 。

他们制备二氧化硫和氯气所依据的原理分别是:
Na2SO3+H2SO4=Na2SO4+H2O+SO2↑
MnO2+4HCl(浓)
 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑(1)用来制取氯气的装置是
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,
(3)装置C的作用是
(4)若装置D中品红溶液换成紫色石蕊溶液,则出现的现象是
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1∶1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的离子方程式是
您最近一年使用:0次
解题方法
5 . 由下列实验现象一定能得出相应结论的是
| 选项 | A | B | C | D |
| 装置 | 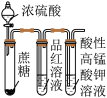 | 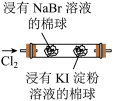 | 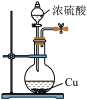 | 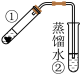 在①中将铁粉、碳粉和NaCl溶液的混合物放置一段时间 |
| 现象 | 蔗糖变黑,有气泡产生,品红溶液和酸性高锰酸钾溶液均褪色 | 左边棉球变黄,右边棉球变蓝 | 产生气泡,溶液冷却后稀释呈蓝色 | ②中倒吸一段水柱 |
| 结论 | 品红溶液褪色和高锰酸钾溶液褪色均体现了 的漂白性 的漂白性 | 氧化性: | 用该装置可以制备 | 说明①中发生了吸氧腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-10更新
|
538次组卷
|
3卷引用:天津市河北区2023-2024学年高三上学期期中考试化学试题
6 . 请用你学到的化学知识填空。
Ⅰ.实验室可用下图装置对铜与浓硫酸的反应进行探究。

(1)加热条件下铜与浓硫酸反应的化学方程式_______ 。反应中氧化剂与还原剂的物质的量之比_______ 。
(2)将产生的气体通入品红溶液中的现象_______ ,通入紫色石蕊溶液中的现象_______ 。
(3)某工厂使用的煤中硫的质量分数为0.64%,该工厂每天燃烧这种煤100 t,如果把产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量为_______ t。
Ⅱ.实验室制氯气可用下图装置,并进行氯气性质实验。
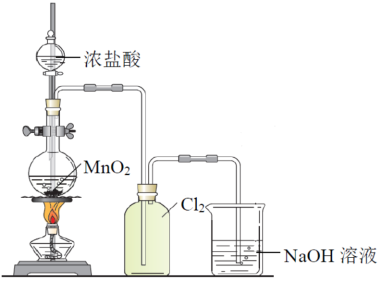
(4)写出实验室制备氯气的化学方程式:_______ 。
(5)将氯气通入冷的石灰乳中可制备用于环境消毒的漂白粉,写出此反应的化学方程式_______ 。
(6)将氯气通入KBr溶液中可发生置换反应,写出反应的离子方程式_______ ;通过单质之间的置换证明氧化性Cl2_______ Br2(填“>”,“<”或“=”)。
Ⅰ.实验室可用下图装置对铜与浓硫酸的反应进行探究。

(1)加热条件下铜与浓硫酸反应的化学方程式
(2)将产生的气体通入品红溶液中的现象
(3)某工厂使用的煤中硫的质量分数为0.64%,该工厂每天燃烧这种煤100 t,如果把产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量为
Ⅱ.实验室制氯气可用下图装置,并进行氯气性质实验。

(4)写出实验室制备氯气的化学方程式:
(5)将氯气通入冷的石灰乳中可制备用于环境消毒的漂白粉,写出此反应的化学方程式
(6)将氯气通入KBr溶液中可发生置换反应,写出反应的离子方程式
您最近一年使用:0次
名校
解题方法
7 . 某校化学兴趣小组探究 与
与 溶液的反应,装置如图所示。
溶液的反应,装置如图所示。
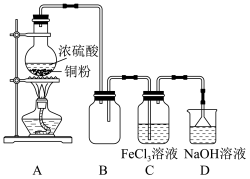
(1)①A装置中制备 的化学方程式为
的化学方程式为_______ ;②装置B的作用_______ 。
(2)该小组同学预测 与
与 溶液反应的现象为溶液由棕黄色变成浅绿色。该小组同学预测的理论依据为:
溶液反应的现象为溶液由棕黄色变成浅绿色。该小组同学预测的理论依据为:_______ (用离子方程式表示)。
(3)该小组探究实验的具体步骤如下:
根据步骤Ⅰ、Ⅱ、Ⅲ的现象,该小组学查阅资料获知:
ⅰ.生成红棕色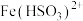 离子的反应为:
离子的反应为:
ⅱ.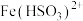 离子可以将
离子可以将 还原为
还原为
③溶液中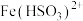 与
与 反应的离子方程式为
反应的离子方程式为_______
④由上述实验可知 与
与 溶液反应生成
溶液反应生成 所需时间较长,缩短该反应所用时间可以采取的措施
所需时间较长,缩短该反应所用时间可以采取的措施_______ (任写两条)
 与
与 溶液的反应,装置如图所示。
溶液的反应,装置如图所示。
(1)①A装置中制备
 的化学方程式为
的化学方程式为(2)该小组同学预测
 与
与 溶液反应的现象为溶液由棕黄色变成浅绿色。该小组同学预测的理论依据为:
溶液反应的现象为溶液由棕黄色变成浅绿色。该小组同学预测的理论依据为:(3)该小组探究实验的具体步骤如下:
| 步骤 | 现象 | 结论 |
Ⅰ。取   溶液于装置C中,并连接好装置,通入 溶液于装置C中,并连接好装置,通入 至饱和。 至饱和。 | 溶液很快由黄色变为红棕色。 | |
| Ⅱ.用激光笔照射步骤Ⅰ中的红棕色溶液。 | 溶液中无明显光路。 | ①红棕色溶液不是 |
| Ⅲ.将步骤Ⅰ中的溶液静置。 | 1小时后,溶液逐渐变为浅绿色。 | ②溶液中有 |
ⅰ.生成红棕色
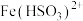 离子的反应为:
离子的反应为:
ⅱ.
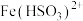 离子可以将
离子可以将 还原为
还原为
③溶液中
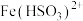 与
与 反应的离子方程式为
反应的离子方程式为④由上述实验可知
 与
与 溶液反应生成
溶液反应生成 所需时间较长,缩短该反应所用时间可以采取的措施
所需时间较长,缩短该反应所用时间可以采取的措施
您最近一年使用:0次
2022-04-04更新
|
584次组卷
|
4卷引用:三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)
(已下线)三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)陕西省咸阳市武功县普集高级中学2021-2022学年高三上学期期末考试化学试题(已下线)秘籍21 性质探究实验-备战2022年高考化学抢分秘籍(全国通用)辽宁省渤海大学附属高级中学2021-2022学年高一下学期第二次阶段性考试化学试题
8 . 下图是实验室制备SO2并验证SO2某些性质的装置图。试回答:

(1)①中的实验现象为_______ ,此实验证明SO2是_______ 气体。
(2)②中的品红溶液_______ ,证明SO2有_______ 性。
(3)③中的实验证明SO2有_______ 性。
(4)④中的实验证明SO2有_______ 性。
(5)⑤的作用是_______ ,反应方程式为_______ 。

(1)①中的实验现象为
(2)②中的品红溶液
(3)③中的实验证明SO2有
(4)④中的实验证明SO2有
(5)⑤的作用是
您最近一年使用:0次
9 . 下列不能 达到“实验目的”的“实验操作及现象”是
| 选项 | 实验目的 | 实验操作及现象 |
| A | 证明浓硫酸有脱水性 | 向蔗糖中滴加浓硫酸,蔗糖变黑 |
| B | 证明SO2具有漂白性 | 向品红溶液中通入SO2,溶液褪色 |
| C | 检验某溶液中含有 | 向某溶液中加入BaCl2溶液,有白色沉淀产生 |
| D | 检验NH4Cl溶液中的 | 向NH4Cl溶液中加入浓NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-19更新
|
544次组卷
|
6卷引用:天津市第五十四中学2023-2024学年高一下学期期中考试化学试卷
解题方法
10 . 下列选用的仪器(部分夹持装置已略去)和药品能达到实验目的的是
|
|
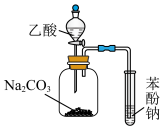
A.检验铜与浓硫酸反应产生的 | B.比较乙酸、碳酸与苯酚的酸性 |
|
|
| C.比较碳酸钠和碳酸氢钠的稳定性 | D.制乙炔并检验乙炔的性质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次