名校
解题方法
1 . 根据要求完成下列各小题实验目的。a、b为弹簧夹,(加热及固定装置已略去)
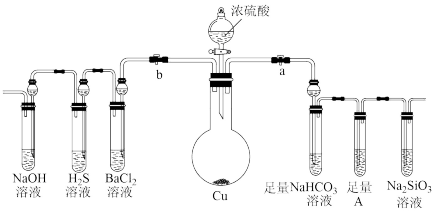
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①连接仪器、_______ 、加药品后,打开a关闭b,打开分液漏斗旋转活塞,然后滴入浓硫酸,发现硫酸滴入几滴,就不再滴下,原因是_______ ,当顺利滴入时加热。
②铜与浓硫酸反应的化学方程式是_______ 。装置A中试剂可以是_______ 。(用a,b,c填空)
a.品红溶液 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
③能说明碳的非金属性比硅强的实验现象是_______ 。
(2)验证 的氧化性、还原性和酸性氧化物的通性。
的氧化性、还原性和酸性氧化物的通性。
①在(1)操作后打开b,关闭a。
②一段时间后, 溶液中的现象是
溶液中的现象是_______ ,化学方程式是_______ 。
(3) 溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①连接仪器、
②铜与浓硫酸反应的化学方程式是
a.品红溶液 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
③能说明碳的非金属性比硅强的实验现象是
(2)验证
 的氧化性、还原性和酸性氧化物的通性。
的氧化性、还原性和酸性氧化物的通性。①在(1)操作后打开b,关闭a。
②一段时间后,
 溶液中的现象是
溶液中的现象是(3)
 溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次
2023-01-21更新
|
372次组卷
|
2卷引用:湖南省益阳市安化县第二中学2022-2023学年高一下学期4月月考化学试题
名校
2 . 下列实验装置或操作正确且能达到实验目的的是
| 选项 | A | B | C | D |
| 装置或操作 | 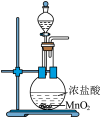 | 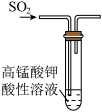 | 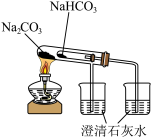 | 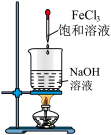 |
| 预期目的 | 实验室制取氯气 | 检验二氧化硫的漂白性 | 比较 、 、 的稳定性 的稳定性 | 制备氢氧化铁胶体目的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-11更新
|
537次组卷
|
3卷引用:湖南省108所学校2022-2023学年高一下学期4月期中联考化学试题
名校
3 . 下列装置合理且能达到实验目的的是
A.制备并收集 | B.验证非金属性:Cl>C>Si |
|
|
| C.进行喷泉实验 | D.除去 中的HCl气体 中的HCl气体 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 用如图所示的装置进行实验(夹持及尾气处理仪器略去),能达到实验目的的是
| 选项 | a中试剂 | b中试剂 | c中试剂 | 实验目的 | 装置 |
| A | 氨水 | CaO | 无 | 制取并收集氨气 |  |
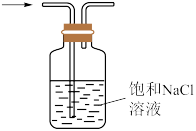
| B | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 制备纯净的Cl2 | |
| C | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 比较酸性强弱: H2CO3>H2SiO3 | |
| D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | 验证SO2具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-06-13更新
|
1811次组卷
|
12卷引用:湖南省常德市芷兰实验中学2020-2021学年高一下学期第一次月考化学试题
湖南省常德市芷兰实验中学2020-2021学年高一下学期第一次月考化学试题北京市朝阳区2020届高三第二次学业水平等级性考试化学试题(已下线)小题必刷17 碳、硅与无机非金属材料——2021年高考化学一轮复习小题必刷(通用版)山东省潍坊第一中学2021届高三上学期开学检测化学试题山东省枣庄滕州一中2021届高三10月月考化学试题山东省德州市2021届高三上学期期中考试化学试题(已下线)专题08 常见无机物及其应用——备战2021年高考化学纠错笔记江西省九校2021-2022学年高三上学期期中联考化学试题北京市海淀区中关村中学2022届高三下学期三模化学试题北京市第十二中学2021-2022学年高一下学期6月月考化学试题北京十二中2021-2022学年高一下学期六月月考(等级考)化学试题(已下线)专题23 化学实验基础性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
5 .  可用于食品工业、农业、染料业等,以下进行其性质的探究。
可用于食品工业、农业、染料业等,以下进行其性质的探究。
(1) 的制备
的制备
实验室可用 固体和75%硫酸制备
固体和75%硫酸制备 ,其化学方程式为:
,其化学方程式为:__________________________ 。
(2) 的收集
的收集
为收集纯净的 可用如图所示装置,则连接顺序为发生装置→
可用如图所示装置,则连接顺序为发生装置→_______ →e。 的性质探究
的性质探究
ⅰ)探究 与水的反应。将注射器中的水注入三颈烧瓶中,测得压强随时间变化如下图所示:
与水的反应。将注射器中的水注入三颈烧瓶中,测得压强随时间变化如下图所示: 的变化速率
的变化速率__________  。
。
②ab段变化及溶液的pH减小,表明 与水发生反应,其方程式为
与水发生反应,其方程式为_____________________ ,该反应的产物不稳定,可通过以下实验证明,请补充操作填在表格横线中。
若____________________ ,证明该反应产物不稳定。
ⅱ)探究 使品红溶液褪色的原因
使品红溶液褪色的原因
操作1:将 通入品红溶液中,品红溶液褪色。
通入品红溶液中,品红溶液褪色。 、
、 、
、____________________ 。
已知:品红是一种棕红色晶体状有机染料,微溶于水,溶于乙醇和酸,溶液呈红色。
④实验设计:小组结合以上信息,设计如下实验证明使品红褪色的微粒不是 请完成表格。
请完成表格。
 可用于食品工业、农业、染料业等,以下进行其性质的探究。
可用于食品工业、农业、染料业等,以下进行其性质的探究。(1)
 的制备
的制备实验室可用
 固体和75%硫酸制备
固体和75%硫酸制备 ,其化学方程式为:
,其化学方程式为:(2)
 的收集
的收集为收集纯净的
 可用如图所示装置,则连接顺序为发生装置→
可用如图所示装置,则连接顺序为发生装置→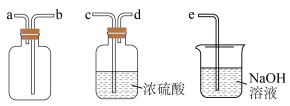
 的性质探究
的性质探究ⅰ)探究
 与水的反应。将注射器中的水注入三颈烧瓶中,测得压强随时间变化如下图所示:
与水的反应。将注射器中的水注入三颈烧瓶中,测得压强随时间变化如下图所示: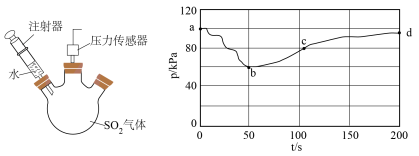
 的变化速率
的变化速率 。
。②ab段变化及溶液的pH减小,表明
 与水发生反应,其方程式为
与水发生反应,其方程式为操作 | 100s内压强变化/kPa |
待烧瓶中压强稳定后,将其置于热水浴中,重新测定压强变化 |
|
|
ⅱ)探究
 使品红溶液褪色的原因
使品红溶液褪色的原因操作1:将
 通入品红溶液中,品红溶液褪色。
通入品红溶液中,品红溶液褪色。
 、
、 、
、已知:品红是一种棕红色晶体状有机染料,微溶于水,溶于乙醇和酸,溶液呈红色。
④实验设计:小组结合以上信息,设计如下实验证明使品红褪色的微粒不是
 请完成表格。
请完成表格。操作2 | 现象 |
不褪色 |
您最近一年使用:0次
2024-04-12更新
|
456次组卷
|
2卷引用:湖南省雅礼中学2024届高三下学期热身训练(三模)化学试题
6 . SO2常用作漂白剂和防腐剂,但它也是造成大气污染的主要有害气体之一、火力发电厂使用的煤炭是常用的含硫燃料,燃煤烟气需净化后再排放。回答下列问题:
(1)某实验小组探究SO2的化学性质,装置如图所示(abc均为浸有相应试液的棉花,夹持与加热装置略)。

制备SO2的反应化学方程式为___________ 。
(2)a处的实验现象为___________ ;b处观察到颜色褪去,SO2体现的化学性质为___________ 。
(3)在工业生产上规定空气中二氧化硫允许排放量不超过0.02mgL1,该小组为测定火力发电厂附近空气中的二氧化硫的含量,进行如下实验:
取标准状况下的空气1L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通入适量I2的淀粉溶液中,则溶液由蓝色变为无色,向所得溶液中加入过量的氯化钡溶液,产生白色沉淀,一系列操作后,称得其质量为0.233g。其中,“一系列操作”为___________ ;空气中SO2是否超过允许排放量:___________ (填“是”或“否”)。
(4)该小组查阅资料知:钙基固硫是燃煤烟气脱硫的常用方法,内容是先用CaCO3浆状物吸收SO2,再鼓入空气,得到硫酸钙用于制备石膏,变废为宝。此过程发生反应的化学方程式依次为___________ ,___________ 。
(1)某实验小组探究SO2的化学性质,装置如图所示(abc均为浸有相应试液的棉花,夹持与加热装置略)。

制备SO2的反应化学方程式为
(2)a处的实验现象为
(3)在工业生产上规定空气中二氧化硫允许排放量不超过0.02mgL1,该小组为测定火力发电厂附近空气中的二氧化硫的含量,进行如下实验:
取标准状况下的空气1L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通入适量I2的淀粉溶液中,则溶液由蓝色变为无色,向所得溶液中加入过量的氯化钡溶液,产生白色沉淀,一系列操作后,称得其质量为0.233g。其中,“一系列操作”为
(4)该小组查阅资料知:钙基固硫是燃煤烟气脱硫的常用方法,内容是先用CaCO3浆状物吸收SO2,再鼓入空气,得到硫酸钙用于制备石膏,变废为宝。此过程发生反应的化学方程式依次为
您最近一年使用:0次
名校
解题方法
7 . 如下图所示,某同学利用 和浓
和浓 制取
制取 并探究其性质。
并探究其性质。____________ 。
(2)装置C中的实验现象是____________ ,该实验现象说明 具有
具有______ 性。
(3)能验证 具有酸性氧化物的通性的实验现象是
具有酸性氧化物的通性的实验现象是____________ 。
(4)装置E的目的是探究 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:____________ 。
(5)甲同学设计下图装置甲来制备 ,但乙同学提出:甲同学制得的
,但乙同学提出:甲同学制得的 中可能含有
中可能含有 ,并用下图的甲、乙、丙、丁装置来检验产物中是否有
,并用下图的甲、乙、丙、丁装置来检验产物中是否有 和
和 。回答下列问题:
。回答下列问题:____________ 。
②乙同学检验产物中有 和
和 ,按气流由左向右流向,连接上述装置的正确顺序是A→
,按气流由左向右流向,连接上述装置的正确顺序是A→______ →B(按顺序填各接口字母,装置可重复使用)。
③可以证明产物中含有 的实验现象是:
的实验现象是:____________ ,乙中澄清石灰水变浑浊。
 和浓
和浓 制取
制取 并探究其性质。
并探究其性质。
(2)装置C中的实验现象是
 具有
具有(3)能验证
 具有酸性氧化物的通性的实验现象是
具有酸性氧化物的通性的实验现象是(4)装置E的目的是探究
 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:(5)甲同学设计下图装置甲来制备
 ,但乙同学提出:甲同学制得的
,但乙同学提出:甲同学制得的 中可能含有
中可能含有 ,并用下图的甲、乙、丙、丁装置来检验产物中是否有
,并用下图的甲、乙、丙、丁装置来检验产物中是否有 和
和 。回答下列问题:
。回答下列问题: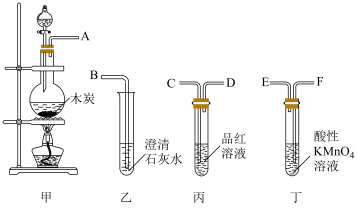
②乙同学检验产物中有
 和
和 ,按气流由左向右流向,连接上述装置的正确顺序是A→
,按气流由左向右流向,连接上述装置的正确顺序是A→③可以证明产物中含有
 的实验现象是:
的实验现象是:
您最近一年使用:0次
解题方法
8 . 某研究性学习小组对二氧化硫的制备、性质以及含量测定进行探究。
Ⅰ.制备二氧化硫
用70%的浓硫酸与 固体反应制备
固体反应制备 气体。
气体。
(1)制备 气体最合适的发生装置是
气体最合适的发生装置是___________ (填写字母),反应的化学方程式为___________ 。
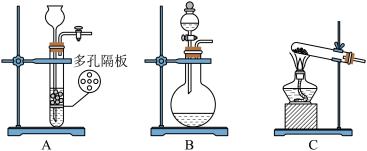
Ⅱ.探究 的性质
的性质
在下图装置中先后三次加入相同浓度、相同体积、不同条件下的钡盐溶液,控制食用油油层厚度一致、打开开关K,通入 流速一致。三次实验现象如下表:
流速一致。三次实验现象如下表:

三次实验分别得到如下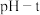 图:
图:
(2)A装置中覆盖食用油的目的是___________ 。
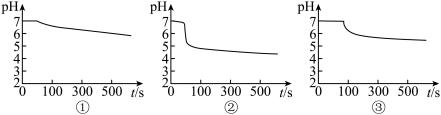
(3)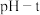 图中,曲线①呈缓慢下降趋势,这是因为
图中,曲线①呈缓慢下降趋势,这是因为___________ ;曲线②出现骤降,这是因为 与
与 溶液中溶解的
溶液中溶解的___________ 发生了氧化还原反应生成了 ;写出实验③中反应的离子方程式为
;写出实验③中反应的离子方程式为___________ 。
Ⅲ.测定空气中二氧化硫含量。
(4)将空气样品经过管道通入密闭容器中的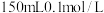 的酸性
的酸性 溶液,若管道中空气流量为
溶液,若管道中空气流量为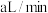 ,经过
,经过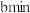 溶液恰好褪色,假设样品中的
溶液恰好褪色,假设样品中的 可被溶液充分吸收。则该空气样品中
可被溶液充分吸收。则该空气样品中 的含量为
的含量为___________  。
。
Ⅰ.制备二氧化硫
用70%的浓硫酸与
 固体反应制备
固体反应制备 气体。
气体。(1)制备
 气体最合适的发生装置是
气体最合适的发生装置是
Ⅱ.探究
 的性质
的性质在下图装置中先后三次加入相同浓度、相同体积、不同条件下的钡盐溶液,控制食用油油层厚度一致、打开开关K,通入
 流速一致。三次实验现象如下表:
流速一致。三次实验现象如下表:| ① | ② | ③ |
已煮沸的 溶液 溶液 | 未煮沸的 溶液 溶液 | 己煮沸的 溶液 溶液 |
| 无白色沉淀生成 | 有白色沉淀生成 | 有白色沉淀生成 |

三次实验分别得到如下
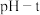 图:
图:
(2)A装置中覆盖食用油的目的是
(3)
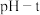 图中,曲线①呈缓慢下降趋势,这是因为
图中,曲线①呈缓慢下降趋势,这是因为 与
与 溶液中溶解的
溶液中溶解的 ;写出实验③中反应的离子方程式为
;写出实验③中反应的离子方程式为Ⅲ.测定空气中二氧化硫含量。
(4)将空气样品经过管道通入密闭容器中的
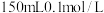 的酸性
的酸性 溶液,若管道中空气流量为
溶液,若管道中空气流量为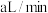 ,经过
,经过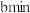 溶液恰好褪色,假设样品中的
溶液恰好褪色,假设样品中的 可被溶液充分吸收。则该空气样品中
可被溶液充分吸收。则该空气样品中 的含量为
的含量为 。
。
您最近一年使用:0次
9 . 某化学学习小组利用铜与浓硫酸在加热条件下制备 ,并对
,并对 的性质进行探究。
的性质进行探究。
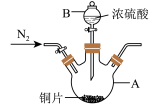
实验Ⅰ:制备
(1)仪器A的名称为___________ 。
(2)制备 的化学方程式为
的化学方程式为___________ 。
(3)A中反应时有白雾(硫酸酸雾)生成,为了避免对后续实验的干扰,可以在A的后面加一个装有___________ 的洗气瓶。
实验Ⅱ:探究 与银盐反应
与银盐反应
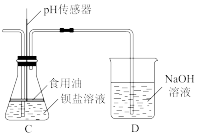
在装置C中先后使用同浓度同体积不同情况的 溶液(①已预先煮沸,②未预先煮沸),控制食用油油层厚度一致、通入
溶液(①已预先煮沸,②未预先煮沸),控制食用油油层厚度一致、通入 流速一致,两次实验分别得到如图
流速一致,两次实验分别得到如图 图:
图:
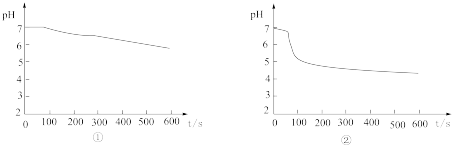
(4)C装置中覆盖食用油的目的是___________ 。
(5)分析 图,写出②中发生反应的离子方程式
图,写出②中发生反应的离子方程式___________ 。
实验Ⅱ:探究 与新制
与新制 悬浊液的反应
悬浊液的反应
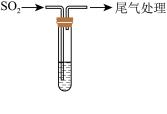
在试管中滴加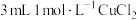 溶液和
溶液和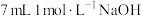 溶液混合,持续通入
溶液混合,持续通入 ,开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈蓝色。
,开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈蓝色。
(6)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸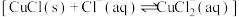 。它与氨水反应生成
。它与氨水反应生成 (无色),在空气中会立即被氧化。
(无色),在空气中会立即被氧化。
①甲同学向洗涤得到的白色沉淀中加入足量的氨水,得到深蓝色溶液,此过程中反应的离子方程式为: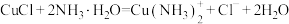 、
、___________ 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,参考如下实验方案填写表格:
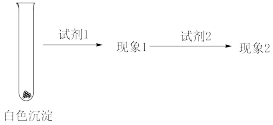
填写下表空格:
 ,并对
,并对 的性质进行探究。
的性质进行探究。
实验Ⅰ:制备

(1)仪器A的名称为
(2)制备
 的化学方程式为
的化学方程式为(3)A中反应时有白雾(硫酸酸雾)生成,为了避免对后续实验的干扰,可以在A的后面加一个装有
实验Ⅱ:探究
 与银盐反应
与银盐反应
在装置C中先后使用同浓度同体积不同情况的
 溶液(①已预先煮沸,②未预先煮沸),控制食用油油层厚度一致、通入
溶液(①已预先煮沸,②未预先煮沸),控制食用油油层厚度一致、通入 流速一致,两次实验分别得到如图
流速一致,两次实验分别得到如图 图:
图:
(4)C装置中覆盖食用油的目的是
(5)分析
 图,写出②中发生反应的离子方程式
图,写出②中发生反应的离子方程式实验Ⅱ:探究
 与新制
与新制 悬浊液的反应
悬浊液的反应
在试管中滴加
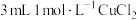 溶液和
溶液和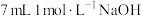 溶液混合,持续通入
溶液混合,持续通入 ,开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈蓝色。
,开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈蓝色。(6)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸
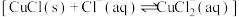 。它与氨水反应生成
。它与氨水反应生成 (无色),在空气中会立即被氧化。
(无色),在空气中会立即被氧化。①甲同学向洗涤得到的白色沉淀中加入足量的氨水,得到深蓝色溶液,此过程中反应的离子方程式为:
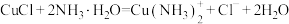 、
、②乙同学用另一种方法证明了该白色沉淀为CuCl,参考如下实验方案填写表格:
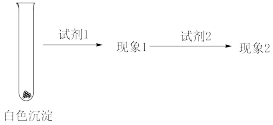
填写下表空格:
| 试剂1 | 试剂2 | 蒸馏水 | |
| 现象1 | 现象2 |
您最近一年使用:0次
名校
解题方法
10 . 硫代硫酸钠是一种重要的化工产品,主要用于照相业作定影剂。其次作鞣革时重铬酸盐的还原剂、含氮尾气的中和剂、媒染剂、麦秆和毛的漂白剂以及纸浆漂白时的脱氯剂等。某兴趣小组制备硫代硫酸钠晶体( ,
,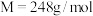 )的实验装置如图所示(省略夹持装置):
)的实验装置如图所示(省略夹持装置):

主要实验步骤为:
①按图连接装置;
② ……,按图示加入试剂;
③先向C中烧瓶加入 和
和 混合溶液,再向A中烧瓶滴加浓
混合溶液,再向A中烧瓶滴加浓 ;
;
④待 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经蒸发浓缩、冷却结晶,过滤、洗涤、干燥后得到产品。
完全消耗后,结束反应。过滤C中混合物,滤液经蒸发浓缩、冷却结晶,过滤、洗涤、干燥后得到产品。
已知:
i. 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成;
溶液混合无沉淀生成;
ii.向 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 ,所得产品常含有少量
,所得产品常含有少量 和
和 ;
;
iii.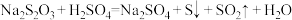 。
。
回答下列问题:
(1)仪器a的名称是_______ ;D装置的作用是_______ ;E中的试剂是_______ ;
(2)补全实验步骤②:_______ ;
(3)为检验产品中是否含有 和
和 ,该小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量
,该小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量 溶液,有白色沉淀生成,向沉淀中滴加足量的
溶液,有白色沉淀生成,向沉淀中滴加足量的_______ ,若_______ (填实验现象),则可以确定产品中含有 和
和 ;
;
(4)称取样品24.8g,配成500mL溶液,取出250mL向其中加入足量稀硫酸,充分反应,静置、过滤、洗涤、干燥、称量得沉淀1.2g,则样品中硫代硫酸钠晶体的百分含量为_______ 。
 ,
,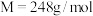 )的实验装置如图所示(省略夹持装置):
)的实验装置如图所示(省略夹持装置):
主要实验步骤为:
①按图连接装置;
② ……,按图示加入试剂;
③先向C中烧瓶加入
 和
和 混合溶液,再向A中烧瓶滴加浓
混合溶液,再向A中烧瓶滴加浓 ;
;④待
 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经蒸发浓缩、冷却结晶,过滤、洗涤、干燥后得到产品。
完全消耗后,结束反应。过滤C中混合物,滤液经蒸发浓缩、冷却结晶,过滤、洗涤、干燥后得到产品。已知:
i.
 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成;
溶液混合无沉淀生成;ii.向
 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 ,所得产品常含有少量
,所得产品常含有少量 和
和 ;
;iii.
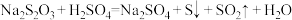 。
。回答下列问题:
(1)仪器a的名称是
(2)补全实验步骤②:
(3)为检验产品中是否含有
 和
和 ,该小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量
,该小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量 溶液,有白色沉淀生成,向沉淀中滴加足量的
溶液,有白色沉淀生成,向沉淀中滴加足量的 和
和 ;
;(4)称取样品24.8g,配成500mL溶液,取出250mL向其中加入足量稀硫酸,充分反应,静置、过滤、洗涤、干燥、称量得沉淀1.2g,则样品中硫代硫酸钠晶体的百分含量为
您最近一年使用:0次