名校
1 . 下列实验装置能达到相应实验目的的是
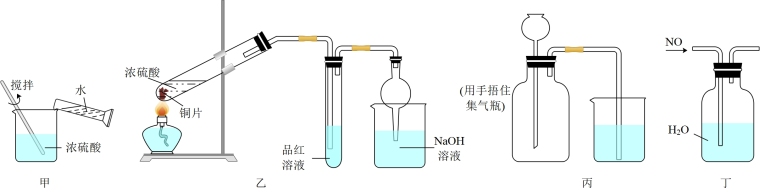
| A.装置甲稀释浓硫酸 |
| B.装置乙制备并检验SO2气体的性质 |
| C.装置丙检查装置的气密性 |
| D.装置丁收集NO |
您最近一年使用:0次
2022-03-23更新
|
539次组卷
|
9卷引用:宁夏石嘴山市平罗中学2021-2022学年高一下学期期中考试化学试题
名校
解题方法
2 . 用下列装置进行相应实验,不能达到实验目的的是
| 选项 | A | B | C | D |
| 装置 |
|
|
|
|
| 目的 | 蒸干 溶液制备无水 溶液制备无水 | 除去 中的 中的 | 分离苯和硝基苯 | 制备 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-09更新
|
560次组卷
|
2卷引用:2024届宁夏银川市唐徕中学高三下学期三模理科综合试题-高中化学
3 . 实验室中用浓硫酸与亚硫酸钠制备SO2并探究其相关性质,所用实验装置如图所示。(CCl4是一种密度比水大的有机溶剂,SO2不溶于CCl4)下列叙述不正确的是


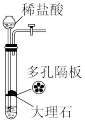
| A.装置①可用于实验室制备CO2 |
| B.装置②中溴水褪色说明SO2具有漂白性 |
| C.装置③中会出现浑浊现象,体现SO2的氧化性 |
| D.装置④中CCl4的作用是防倒吸 |
您最近一年使用:0次
2022-03-14更新
|
397次组卷
|
4卷引用:宁夏石嘴山市平罗中学2021-2022学年高一上学期期末考试化学试题
名校
4 . 下列方案设计、现象和结论均正确的是
选项 | 实验目的 | 方案设计 | 现象和结论 |
A | 探究碳酸钠溶液碱性是CO | 取2.0mL0.lmol/LNa2CO3溶液,滴入3滴酚酸,观察现象,再滴入3滴lmol/LBaCl2溶液 | 滴入酚酞溶液变红,再滴入BaCl2后出现白色沉淀,溶液颜色变浅 |
B | 探究淀粉的水解 | 将淀粉和稀硫酸混合加热一段时间后,再加入新制的Cu(OH)2加热 | 产生红色沉淀,淀粉水解为葡萄糖 |
C | 探究电解质的强弱 | 用pH计测量醋酸溶液、盐酸的pH, | 盐酸的pH小,CH3COOH是弱电解质 |
D | 探究酸性氧化物和盐的反应 | 将SO2通入BaCl2溶液 | 有白色沉淀生成,生成了BaSO3沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
13-14高三上·江西·阶段练习
5 . 二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。探究二氧化硫的制取和性质都有着非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-1价)在高温下和氧气反应制备SO2:4FeS2+11O2 2Fe2O3+8SO2。该反应中被氧化的元素是
2Fe2O3+8SO2。该反应中被氧化的元素是______ (填元素符号)。当该反应转移5.50mol电子时,生成的二氧化硫在标准状况下的体积为______ L。
(2)①实验室可用70%的浓硫酸和亚硫酸钠反应制取二氧化硫,如果能控制反应速度,下图中可选用的发生装置是______ (填写字母)。
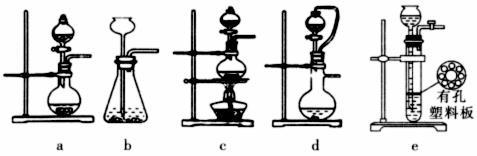
②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有25.2%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠______ g(保留一位小数)。
(3)某化学兴趣小组设计用如图装置验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为______ 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成
上述方案中合理的是______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为______ 。
(1)工业上用黄铁矿(FeS2,其中S元素为-1价)在高温下和氧气反应制备SO2:4FeS2+11O2
 2Fe2O3+8SO2。该反应中被氧化的元素是
2Fe2O3+8SO2。该反应中被氧化的元素是(2)①实验室可用70%的浓硫酸和亚硫酸钠反应制取二氧化硫,如果能控制反应速度,下图中可选用的发生装置是

②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有25.2%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠
(3)某化学兴趣小组设计用如图装置验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成
上述方案中合理的是
您最近一年使用:0次
6 . 下列制取SO2、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是
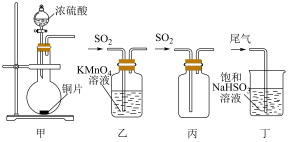
| A.用装置甲制取SO2 | B.用装置乙验证SO2的漂白性 |
| C.用装置丙收集SO2 | D.用装置丁处理实验中的尾气 |
您最近一年使用:0次
2024-03-25更新
|
910次组卷
|
108卷引用:宁夏回族自治区吴忠市青铜峡市高级中学2020届高三上学期第二次月考化学试题
宁夏回族自治区吴忠市青铜峡市高级中学2020届高三上学期第二次月考化学试题宁夏银川一中2020-2021学年高一上学期期末考试(GAC)化学试题宁夏青铜峡市高级中学2021-2022学年高一上学期期末考试化学试题河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题2017年全国普通高等学校招生统一考试化学(江苏卷精编版)安徽省宣城市2016-2017学年高一下学期期末调研测试化学试题江苏省海安高级中学2018届高三1月月考化学试题北京市丰台区2018届高三上学期期末考试化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.15 物质的制备及实验方案设计与评价重庆市第一中学2017-2018学年高一下学期第一次月考化学试题北京市密云区2017-2018学年高三第二学期阶段性练习理综化学试题(已下线)解密16 化学实验基础(教师版)——备战2018年高考化学之高频考点解密【全国百强校】四川省雅安中学2018-2019学年高一上学期开学考试化学试题山东省淄博市淄川中学2019届高三上学期开学考试化学试题【校级联考】湖北省宜昌县域高中协同发展共合体2018-2019学年高一上学期期末考试化学试题【全国百强校】吉林省延边市第二中学2018-2019学年高一下学期开学考试化学试题步步为赢 高二化学暑假作业:作业十二 化学实验基础知识重庆市璧山大路中学校2018-2019学年高一下学期4月月考化学试题重庆市第三十中学2018-2019学年高一下学期期中考试化学试题百所名校联考-非金属及其化合物福建省莆田市莆田第二十五中学2020届高三上学期期中考试化学试题安徽省合肥二中2019-2020学年度高三上学期第一次段考化学试题安徽省芜湖市严桥中学2019-2020学年高三第一学期第三次月考化学试题上海市同济大学第一附属中学2019—2020学年高三上学期期中考试化学试题2019年秋高三化学复习强化练习—— 硫及其化合物上海市普陀区2020届高三上学期一模化学试题江苏省苏州市2018-2019学年高一上学期期末考试化学试题2020届高三化学一轮复习 化学基础实验(选择题和大题训练)(已下线)专题3.4 硫及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》第2章 第3节 化学反应的利用福建省福州市第一中学2020年高一在线自测自评质检化学试题(已下线)广东省深圳中学2020届高三3月份教学质量监测卷理综化学试题四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题福建省泉州第十六中学2019-2020学年高一下学期5月月考化学试题(已下线)专题4.3 硫及其化合物(练)——2020年高考化学一轮复习讲练测(已下线)专题4.3 硫及其化合物(讲)——2020年高考化学一轮复习讲练测北京市丰台区首师大附属云岗中学2019届高三上学期10月月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第二次调研考试化学试题(已下线)考点15 常见非金属元素单质及其重要化合物3——硫-2020年【衔接教材·暑假作业】新高三一轮复习化学(已下线)第6单元 常见的非金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷广东省珠海市2019-2020学年高一下学期期末学业质量监测化学试题苏教版(2020)高一必修第一册专题4 总结检测鲁科版(2019)高一必修第一册第3章 物质的性质与转化 总结检测鲁科版(2019)高一必修第一册第三章C 高考挑战区 过高考 3年真题强化闯关北京师范大学珠海分校附属外国语学校2019-2020学年高一下学期期末考试化学试题高一必修第一册(鲁科2019)第3章 第2节 硫的转化 高考帮高一必修第二册(人教2019版)第五章 素养检测高一必修第一册(苏教2019版)专题4 C 高考挑战区湖南省长沙市雅礼中学2021届高三上学期第二次月考化学试题(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(精练)-2021年高考化学一轮复习讲练测高一必修第一册(苏教2019)专题4 第一单元 含硫化合物的性质3福建省漳州市平和县第一中学2021届高三上学期期中考试化学试题安徽省灵璧县第一中学2020-2021学年高一上学期12月月考试题山东省胶州市实验中学2020-2021学年高一上学期12月月考化学试题(已下线)练习9 硫和二氧化硫-2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)专题4 第一单元综合拔高练-高中化学苏教2019版必修第一册(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物(已下线)5.1.3 不同价态含硫物质的转化(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)江苏省苏州市苏州大学附属中学2020-2021学年高一上学期月考化学试卷2湖南省长沙市第一中学2020-2021学年高一下学期第一次月考化学试题江苏省苏州市园区苏州大学附属中学2020-2021学年高一上学期12月月考化学试题黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高一4月月考化学试题(已下线)【苏州新东方】04 吴县中学黑龙江省哈尔滨市第一六二中学校2020-2021学年高一下学期4月月考化学试题吉林省松原市前郭尔罗斯蒙古族自治县第五中学2021届高三下学期5月月考化学试题甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(理)试题江苏省启东市吕四中学2020-2021学年高一下学期第二次月考化学试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(B)试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(A)试题吉林省白城一中、大安一中、通榆一中、洮南一中、镇赉一中2020-2021学年高一下学期期末考试化学试题(已下线)考向12 硫及其化合物-备战2022年高考化学一轮复习考点微专题江苏省昆山市周市高级中学2020-2021学年高一上学期第二次模块测试化学试题广东省深圳市第七高级中学2022届高三第一次月考化学试卷江苏省盐城市伍佑中学2021-2022学年高二上学期第一次阶段考试化学(必修)试题浙江省温州市瑞安市上海新纪元高级中学2021-2022学年高一9月份月考(5-6班)化学试题陕西省西安市高新第一中学2020届高三教学质量监测理综化学试题江苏省徐州市沛县2021-2022学年高三上学期第一次学情调研化学试题(已下线)考向34 物质的检验、分离和提纯-备战2022年高考化学一轮复习考点微专题江苏省徐州市2021-2022学年高一上学期12月月考化学试题(已下线)上海市华东师范大学第二附属中学2021-2022学年高一上学期12月质量检测化学试题(已下线)第10练 硫及其化合物-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)江苏省盐城市滨海县五汛中学2021-2022学年高二上学期期中考试化学试题甘肃省张掖市第二中学 2021-2022学年高一下学期3月月考化学试题(已下线)卷13 化学基础实验(检验、鉴别、分离、提纯)-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)上海市七宝中学 2021-2022学年高一下学期期中考试化学试题(已下线)【期末复习】必刷题(1)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)广东省广州市育才中学2021-2022学年高一下学期期中考试化学试题天津市第二十一中学2021-2022学年高一下学期期中学情调研化学试题新疆维吾尔自治区阿克苏地区第二中学2021-2022学年高一年级下学期第二次月考化学试题(已下线)【教材实验热点】06 二氧化硫的漂白性(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)江苏省南京市中华中学2021-2022学年高三上学期期中考试化学试题江苏省苏州市常熟中学2022-2023学年高一上学期末测试卷一化学试题江西省上饶市2019-2020学年高一下学期期末教学质量测试化学试题四川省资阳市乐至中学2022-2023学年高一下学期3月月考化学试题四川省自贡市荣县2022-2023学年高一下学期4月期中考试化学试题广东省广州市协和中学2022-2023学年高一下学期期中考试化学试题广东省广州科学城中学2022-2023学年高一下学期期中考试化学试题(已下线)专题突破卷13 化学实验基础(二)-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)考点巩固卷04 非金属及其化合物(4大考点60题)?-2024年高考化学一轮复习考点通关卷(新高考通用)山东省鄄城县第一中学2023-2024学年高三上学期9月月考化学试题(已下线)押题卷01-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)福建省漳州市第一中学2023-2024学年高一上学期化学12月月考(第二单元)江西省丰城市东煌学校2022-2023学年高一下学期6月期末考试化学试题广东实验中学越秀学校2023-2024学年高一3月段考化学试题黑龙江省双鸭山市第一中学2023-2024学年高一下学期4月月考化学试题(已下线)北京市西城区2024届高三下学期第三次模拟测试化学试题广东省东莞市东华高级中学 东华松山湖高级中学 2024届高三下学期第三次模拟考试 化学试题
名校
解题方法
7 . 用如图装置完成下列实验,其中能达到相应实验目的的是
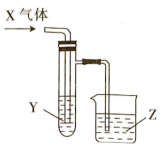

| A.当X气体为SO2,Y为品红溶液时,证明SO2具有强氧化性 |
| B.当X气体为HCl,Y为碳酸钠溶液时,证明氯的非金属性强于碳的 |
| C.当X气体为Cl2,Y为品红溶液时,证明氯气具有漂白性 |
| D.当X气体为乙烯,Y为溴的四氯化碳溶液时,证明乙烯与Br2发生的是加成反应 |
您最近一年使用:0次
2021-06-19更新
|
329次组卷
|
4卷引用:宁夏石嘴山第三中学2021-2022学年高一下学期期末考试化学试题
名校
8 . 下列实验中,操作和现象均正确且能实现相应实验目的的是
| 选项 | 实验目的 | 操作 | 现象 |
| A | 验证BaSO3难溶于水 | 将SO2通入Ba(NO3)2溶液中 | 有白色沉淀生成 |
| B | 验证非金属性:Br > I | 将溴水滴入淀粉KI溶液中 | 溶液变蓝 |
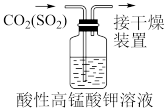
| C | 验证SO2的漂白性 | 将SO2通入酸性KMnO4溶液中 | 溶液褪色 |
| D | 验证某化合物一定是钠盐 | 将该化合物在酒精灯火焰上灼烧 | 焰色为黄色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-03-06更新
|
286次组卷
|
5卷引用:宁夏银川一中2018届高三第六次月考理综化学试题
名校
9 . 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是

| A.洗气瓶中产生的沉淀是硫酸钡 |
| B.在Z导管出来的气体中无二氧化碳 |
| C.洗气瓶中产生的沉淀是碳酸钡 |
| D.在Z导管口无明显现象 |
您最近一年使用:0次
名校
10 . 某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2并完成相关性质探究(不考虑水蒸气)。(已知:C+2H2SO4(浓) CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)
(1)有同学认为制得的SO2中可能混有杂质,其化学式为_________ 。
为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。_________ ;装置C中品红溶液的作用是_________ 。
(3)装置H的作用为_________ 。
兴趣小组设计如图装置验证二氧化硫的化学性质。___________ ;
为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
(5)上述方案中合理的是___________ (填Ⅰ、Ⅱ或Ⅲ);试管b中发生反应的离子方程式为___________ 。
(6)如果用硫酸溶液和 固体反应制取
固体反应制取 装置如图所示。其中
装置如图所示。其中 导管的作用是
导管的作用是________ 。 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。 (标准状况下),最终所得固体质量为
(标准状况下),最终所得固体质量为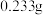 ,通过计算确定该空气中二氧化硫的含量是
,通过计算确定该空气中二氧化硫的含量是________ 。(结果精确到 )
)
 CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)(1)有同学认为制得的SO2中可能混有杂质,其化学式为
为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。
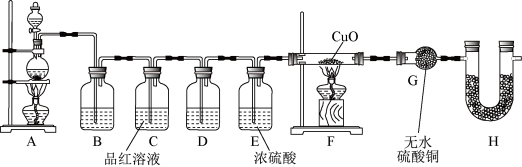
(3)装置H的作用为
兴趣小组设计如图装置验证二氧化硫的化学性质。

为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
(5)上述方案中合理的是
(6)如果用硫酸溶液和
 固体反应制取
固体反应制取 装置如图所示。其中
装置如图所示。其中 导管的作用是
导管的作用是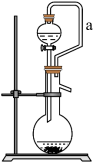
 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
 (标准状况下),最终所得固体质量为
(标准状况下),最终所得固体质量为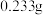 ,通过计算确定该空气中二氧化硫的含量是
,通过计算确定该空气中二氧化硫的含量是 )
)
您最近一年使用:0次
2024-04-29更新
|
172次组卷
|
2卷引用:宁夏石嘴山市平罗中学2023-2024学年高一下学期4月月考化学试题


 水解导致
水解导致

