1 . A、B、C、D是四种短周期元素,E是第四周期的过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(2)用B元素最高价氧化物的水化合物的水溶液进行焰色反应实验,焰色为
(3)C的元素名称为
(4)足量E单质与稀硝酸反应的离子方程式为
您最近一年使用:0次
2 . 下列做法不正确的是
| A.配制一定体积某浓度的稀硫酸,浓硫酸稀释后直接转移至容量瓶,所配溶液浓度偏大 |
| B.做焰色试验所用的铂丝应先蘸稀盐酸,再放在火焰上烧至无色 |
| C.实验剩余的钠单质应该放回到原试剂瓶中 |
D. 和 和 溶液分别与少量氯水反应,根据现象可判断溴与碘的非金属性强弱 溶液分别与少量氯水反应,根据现象可判断溴与碘的非金属性强弱 |
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题:
(1)基态钛原子的价层电子排布式为_______ ,其原子核外电子的空间运动状态有_______ 种,共有_______ 种运动状态不同的电子。
(2)基态Si原子,若其电子排布式表示为[Ne]3s23p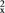 违背了
违背了_______ 。
(3)①基态Cu原子有_______ 种不同能级的电子。铜或铜盐的焰色试验为绿色,该光谱是_______ (填“吸收光谱”或“发射光谱”)。
②N原子中最高能级的电子的电子云轮廓图为_______ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是_______ 。
(1)基态钛原子的价层电子排布式为
(2)基态Si原子,若其电子排布式表示为[Ne]3s23p
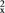 违背了
违背了(3)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
您最近一年使用:0次
4 . 现有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
(2) 元素的原子核外共有
元素的原子核外共有___________ 种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3) 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是___________ 。
(4) 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是___________ 。
(5) 位于元素周期表中
位于元素周期表中___________ 区(按电子排布分区),其基态原子的价层电子排布式为___________ 。
(6)G单质投入水中所得溶液阳离子检验方法___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
 元素是形成化合物种类最多的元素 元素是形成化合物种类最多的元素 |
 元素基态原子的核外 元素基态原子的核外 能级电子数比 能级电子数比 能级电子总数少1个 能级电子总数少1个 |
 元素基态原子的核外 元素基态原子的核外 轨道中有两个未成对电子 轨道中有两个未成对电子 |
 元素的气态基态原子的第一至第四电离能分别是 元素的气态基态原子的第一至第四电离能分别是 , , , , , ,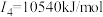 |
 元素的主族序数与周期数的差为4 元素的主族序数与周期数的差为4 |
 元素是前四周期中电负性最小的元素 元素是前四周期中电负性最小的元素 |
 元素位于元素周期表中的第8列 元素位于元素周期表中的第8列 |
 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)(2)
 元素的原子核外共有
元素的原子核外共有(3)
 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是(4)
 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是(5)
 位于元素周期表中
位于元素周期表中(6)G单质投入水中所得溶液阳离子检验方法
您最近一年使用:0次
名校
5 .  是原子序数依次增大的前四周期元素,A元素原子最高能级的不同轨道都有电子且自旋方向相同;B元素原子的价层电子排布式是
是原子序数依次增大的前四周期元素,A元素原子最高能级的不同轨道都有电子且自旋方向相同;B元素原子的价层电子排布式是 ;其中C元素的部分电离能如下表;含D元素的化合物焰色试验火焰呈紫色(透过蓝色钴玻璃)。下列说法
;其中C元素的部分电离能如下表;含D元素的化合物焰色试验火焰呈紫色(透过蓝色钴玻璃)。下列说法不正确 的是
 是原子序数依次增大的前四周期元素,A元素原子最高能级的不同轨道都有电子且自旋方向相同;B元素原子的价层电子排布式是
是原子序数依次增大的前四周期元素,A元素原子最高能级的不同轨道都有电子且自旋方向相同;B元素原子的价层电子排布式是 ;其中C元素的部分电离能如下表;含D元素的化合物焰色试验火焰呈紫色(透过蓝色钴玻璃)。下列说法
;其中C元素的部分电离能如下表;含D元素的化合物焰色试验火焰呈紫色(透过蓝色钴玻璃)。下列说法| 元素 | 电离能 | |||
 |  |  |  | |
| C | 578 | 1817 | 2745 | 11575 |
A.离子半径大小: |
| B.C的最高价氧化物对应水化物可溶于D的最高价氧化物对应水化物的水溶液 |
C.化合物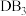 中含离子键和共价键 中含离子键和共价键 |
| D.元素D的核外电子运动具有10种不同的空间运动状态 |
您最近一年使用:0次
2024-04-03更新
|
370次组卷
|
3卷引用:浙江省杭州八县2023-2024学年高二上学期期末考试化学试题
6 . 按要求回答下列问题:
(1)下列B原子的电子排布式的状态中,能量最高的是________(用字母表示)。
(2)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,回答下列问题:
①基态Ge原子的简化的电子排布式为________ ,基态原子核外有________ 种空间运动状态。
②比较下列锗卤化物的熔点和沸点,分析呈现该变化规律的原因是________________________________ 。
③光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________________ 。
(3)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子 的空间构型为
的空间构型为________ ,Na在空气中燃烧则发出黄色火焰,这种黄色焰色用光谱仪摄取的光谱为________ 光谱(填“发射”或“吸收”)。
(4)元素镍与镍钴合金的晶胞结构分别如图a、b所示:
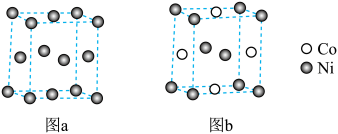
①镍钴合金若写作NixCo1-x,则图b合金中x=________
②已知晶胞(图a)的边长为m pm,设NA为阿伏加德罗常数的值,则镍的密度为________ g/cm3(列出计算式)。
(1)下列B原子的电子排布式的状态中,能量最高的是________(用字母表示)。
A. | B.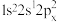 | C. | D.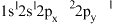 |
(2)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,回答下列问题:
①基态Ge原子的简化的电子排布式为
②比较下列锗卤化物的熔点和沸点,分析呈现该变化规律的原因是
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(3)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子
 的空间构型为
的空间构型为(4)元素镍与镍钴合金的晶胞结构分别如图a、b所示:

①镍钴合金若写作NixCo1-x,则图b合金中x=
②已知晶胞(图a)的边长为m pm,设NA为阿伏加德罗常数的值,则镍的密度为
您最近一年使用:0次
7 . 下列有关光谱的说法中不正确的是
| A.原子中的电子在跃迁时会发生能量变化,这是原子光谱产生的原因 |
| B.焰色反应产生的颜色和五彩霓虹灯都是发射光谱 |
| C.原子光谱可用于鉴定和发现元素 |
| D.原子中的电子在从激发态向基态跃迁时才能产生原子光谱 |
您最近一年使用:0次
2024-03-09更新
|
140次组卷
|
2卷引用:陕西省宝鸡市金台区2023-2024学年高二上学期期末检测化学试题
解题方法
8 . 下列说法错误的是
| A.钠的焰色试验呈黄色是原子核外电子跃迁释放能量的结果 |
| B.根据对角线规则,锂与镁性质相似,锂燃烧生成氧化锂而不是过氧化锂 |
| C.乙酸的酸性弱于三氟乙酸,这是因为两种分子中的碳原子杂化方式不同 |
| D.I2在水中溶解度很小,但在CCl4中溶解度很大,这种现象可用相似相溶原理解释 |
您最近一年使用:0次
9 . 下列关于物质因果关系的叙述中,完全正确的一组是
| 选项 | 现象 | 解释 |
| A | 向淀粉水解液中先加NaOH溶液后,再加入银氨溶液并水浴加热,出现银镜 | 淀粉已完全水解 |
| B | 向久置的 溶液中加入足量稀硝酸,再加入足量 溶液中加入足量稀硝酸,再加入足量 溶液,出现白色沉淀 溶液,出现白色沉淀 | 久置的 溶液已部分被氧化 溶液已部分被氧化 |
| C | 乙醛、乙酸和葡萄糖都能与新制的 反应 反应 | 它们都发生了氧化反应 |
| D | 洁净铂丝蘸取无色盐溶液进行焰色反应,火焰呈黄色 | 该无色盐溶液一定含钠盐 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 我国古代劳动人民对草木灰的使用积累了丰富的经验,草木灰含 等。下列有关说法不正确的是
等。下列有关说法不正确的是
 等。下列有关说法不正确的是
等。下列有关说法不正确的是| A.草木灰可以用作化肥 | B.草木灰浸泡的溶液焰色试验火焰呈黄色 |
| C.草木灰经溶解、过滤、蒸发可制得钾盐 | D.古人可用草木灰浸泡的溶液洗涤衣裳冠带 |
您最近一年使用:0次



