A、B、C、D是四种短周期元素,E是第四周期的过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(2)用B元素最高价氧化物的水化合物的水溶液进行焰色反应实验,焰色为
(3)C的元素名称为
(4)足量E单质与稀硝酸反应的离子方程式为
更新时间:2024-05-03 17:32:03
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某无色试样溶液可能含有以下离子中的一种或几种:K+、Mg2+、Al3+、Cu2+、SO42-、Cl-。现进行如下实验:
① 取少量该试样溶液加入过量的氢氧化钡溶液,充分反应后过滤,得到沉淀1和溶液1。
② 向沉淀1中加入过量盐酸,沉淀部分溶解。
③ 向溶液1中通入适量二氧化碳气体,充分反应后过滤,得到沉淀2和溶液2。
④ 向沉淀2中加入过量盐酸,沉淀溶解并放出气体。
⑤ 另取少量该试样溶液进行焰色反应实验,透过蓝色钴玻璃片观察到紫色火焰。
(1)该试样溶液中肯定存在的离子有______________________ 。
(2)该试样溶液中可能存在的离子有__________________________ 。
(3)该试样溶液中一定不存在的离子有__________________________ 。
① 取少量该试样溶液加入过量的氢氧化钡溶液,充分反应后过滤,得到沉淀1和溶液1。
② 向沉淀1中加入过量盐酸,沉淀部分溶解。
③ 向溶液1中通入适量二氧化碳气体,充分反应后过滤,得到沉淀2和溶液2。
④ 向沉淀2中加入过量盐酸,沉淀溶解并放出气体。
⑤ 另取少量该试样溶液进行焰色反应实验,透过蓝色钴玻璃片观察到紫色火焰。
(1)该试样溶液中肯定存在的离子有
(2)该试样溶液中可能存在的离子有
(3)该试样溶液中一定不存在的离子有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】化合物G是冶炼某常见金属的原料,工业上提取G的流程如下图所示(已知晶体E的焰色反应呈黄色):
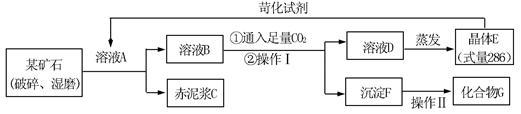
(1)溶液A为_____________ 溶液(用化学式表示,下同),赤泥浆C的主要成分有_____________ ,
(2)操作Ⅰ为_____________ ;操作Ⅱ为_____________ ,
(3)写出由B生产F的离子方程式为__________________
(4)苛化试剂与E溶液反应生成溶液A,则苛化试剂是_____________ ,该工艺的优点是_____________ (答一条,合理即可)。

(1)溶液A为
(2)操作Ⅰ为
(3)写出由B生产F的离子方程式为
(4)苛化试剂与E溶液反应生成溶液A,则苛化试剂是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】如图所示,下列各项变化的未知物焰色试验均呈黄色,E为淡黄色粉末。
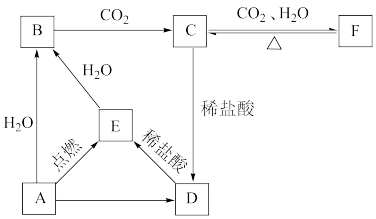
回答下列问题。
(1)写出A→B的化学方程式:___________ 。
(2)写出E→B的离子方程式:___________ 。
(3)B溶液中通入过量CO2可生成F,其反应的离子方程式为:___________ 。
(4)当固体C中含有固体杂质F,如何除杂:___________ ;反应涉及的化学方程式___________ 。
(5)在一密闭容器中有CO、H2、O2共16.5g和足量的E,用电火花引燃,使其完全反应,固体增重7.5g,则原混合气体中O2的质量是___________ g。

回答下列问题。
(1)写出A→B的化学方程式:
(2)写出E→B的离子方程式:
(3)B溶液中通入过量CO2可生成F,其反应的离子方程式为:
(4)当固体C中含有固体杂质F,如何除杂:
(5)在一密闭容器中有CO、H2、O2共16.5g和足量的E,用电火花引燃,使其完全反应,固体增重7.5g,则原混合气体中O2的质量是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W相邻;②X分别与Y、Z、W可组成化学式为YX3,X2Z和X2W三种共价化合物;③Y的最简氢化物可与其最高价含氧酸反应。
(1)X、Y、Z原子最外层电子数之和是_______ 。
(2)X2W的结构式是_______ ;W在元素周期表中的位置是_______ 。
(3)X、Y和Z组成的一种化合物是强酸,写出该酸的稀溶液与铜反应的离子方程式:_______ 。
(4)Y的最简氢化物与其最高价含氧酸反应产物为_________ (填化学式),写出检验其阳离子的办法________ 。
(5)由X、Z元素构成既有极性键又有非极性键的化合物的电子式是______ 。
(1)X、Y、Z原子最外层电子数之和是
(2)X2W的结构式是
(3)X、Y和Z组成的一种化合物是强酸,写出该酸的稀溶液与铜反应的离子方程式:
(4)Y的最简氢化物与其最高价含氧酸反应产物为
(5)由X、Z元素构成既有极性键又有非极性键的化合物的电子式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】元素X、Q、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3︰4,M原子的最外层电子数与次外层电子数之比为3︰4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,Q和Y在周期表中的位置相邻。请回答下列问题。
(1)M在元素周期表中的位置是___ ,写出Z的离子结构示意图:__ ;Q的简单氢化物的结构式为___ 。
(2)写出X、Y、R按原子个数之比1︰1︰1形成的化合物的化学式:___ 。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:___ 。
(4)写出单质R的一种工业用途:___ 。
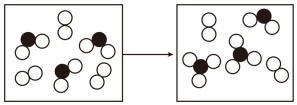
(5)如图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式:___ 。
(6)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式:___ 。
(1)M在元素周期表中的位置是
(2)写出X、Y、R按原子个数之比1︰1︰1形成的化合物的化学式:
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:
(4)写出单质R的一种工业用途:
(5)如图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式:

(6)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】元素X、Y、Z、M、N为短周期主族元素,且原子序数依次增大,已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4且M原子的质子数是Y原子的2倍,N-、Z+、X+的半径逐渐减小,化合物XN在常温下为气体,据此回答下列问题:
(1)写出Z与N形成的化合物的化学式_____ 。
(2)X与Y可分别形成10电子和18电子的分子,写出该18电子电子转化成10电子分子的化学方程式____ (分解反应)。
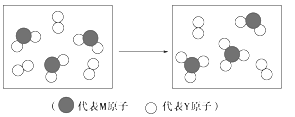
(3)下图表示由上述元素组成的两种气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:________ 。
(4)A、B均为由上述五种元素中的三种元素组成的强电解质,且组成元素的原子个数之比为1:1:1。若在各自的水溶液中,A能抑制水的电离,B能促进水的电离,则A的化学式为____ ,B的化学式为_______ 。
(1)写出Z与N形成的化合物的化学式
(2)X与Y可分别形成10电子和18电子的分子,写出该18电子电子转化成10电子分子的化学方程式
(3)下图表示由上述元素组成的两种气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:

(4)A、B均为由上述五种元素中的三种元素组成的强电解质,且组成元素的原子个数之比为1:1:1。若在各自的水溶液中,A能抑制水的电离,B能促进水的电离,则A的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】Cu(II)可形成多种配合物,呈现出多样化的性质和用途。
(1)向盛有硫酸铜水溶液的试管中加入少量氨水生成蓝色沉淀,继续加入过量氨水,得到深蓝色透明溶液,最后向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
① 产生蓝色沉淀的离子方程式是___________ 。
② [Cu(NH3)4]SO4在水中电离的方程式是___________ 。
(2)如下图所示,Cu(II)配合物A和B可发生配位构型的转变,该转变可带来颜色的变化,因此可用作热致变色材料,在温度传感器、变色涂料等领域应用广泛。

①Cu2+的价层电子排布式为___________ 。
②A中氮原子与其它原子(或离子)之间存在的作用力类型有___________ ,氢原子与其它原子之间存在的作用力类型有___________ 。
③已知:当Cu(II)配合物A和B配位构型由八面体转变为四方平面时,吸收光谱蓝移,配合物颜色紫色变为橙色。
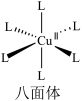

想将配合物的颜色由紫色调整为橙色,需要进行的简单操作为___________ 。
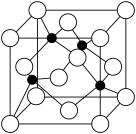
(3)CuCl2和CuCl是铜常见的两种氯化物,下面示意图表示的是___________ 的晶胞。已知晶胞的边长为a pm,阿伏伽德罗常数为NA mol-1,则该晶体的密度为___________ g·cm-3。
(1)向盛有硫酸铜水溶液的试管中加入少量氨水生成蓝色沉淀,继续加入过量氨水,得到深蓝色透明溶液,最后向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
① 产生蓝色沉淀的离子方程式是
② [Cu(NH3)4]SO4在水中电离的方程式是
(2)如下图所示,Cu(II)配合物A和B可发生配位构型的转变,该转变可带来颜色的变化,因此可用作热致变色材料,在温度传感器、变色涂料等领域应用广泛。

①Cu2+的价层电子排布式为
②A中氮原子与其它原子(或离子)之间存在的作用力类型有
③已知:当Cu(II)配合物A和B配位构型由八面体转变为四方平面时,吸收光谱蓝移,配合物颜色紫色变为橙色。


想将配合物的颜色由紫色调整为橙色,需要进行的简单操作为
(3)CuCl2和CuCl是铜常见的两种氯化物,下面示意图表示的是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E 代表前 4 周期的五种元素,原子序数依次增大。请填空:
(1)A 元素基态原子的最外层有 3 个未成对电子,次外层有 2 个电子,其电子轨道表示式为_______ 。其原子核外共有_______ 种不同运动状态的电子;其基态原子中最高能量能级轮廓图形状_______ ,其最高能量能级的电子云在空间有_______ 种伸展方向。
(2)B 元素的负一价离子的电子层结构与氩相同,B 离子的结构示意图为_______ 。
(3)C 元素的正三价离子的 3d 能级为半充满,C 的元素符号为_______ ,该元素在周期表中的位置为_______ 。
(4)D 元素基态原子的M 层全充满,N 层没有成对电子,只有一个未成对电子,D 的元素基态原子的电子排布式为_______ ,在元素周期表中的位置为_______ 。
(5)E 元素基态原子中没有未成对电子,E 的价层电子排布式是_______ 。
(1)A 元素基态原子的最外层有 3 个未成对电子,次外层有 2 个电子,其电子轨道表示式为
(2)B 元素的负一价离子的电子层结构与氩相同,B 离子的结构示意图为
(3)C 元素的正三价离子的 3d 能级为半充满,C 的元素符号为
(4)D 元素基态原子的M 层全充满,N 层没有成对电子,只有一个未成对电子,D 的元素基态原子的电子排布式为
(5)E 元素基态原子中没有未成对电子,E 的价层电子排布式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】物质的组成、结构决定着物质的性质与变化,我们必须在原子、分子层次上深入地研究物质的结构。
Ⅰ.Q、R、X、Y、W、Z六种元素的原子序数依次增大。已知:
①Q、R、X、Y均为短周期主族元素;
②Z的原子序数为29;
③W是前四周期元素中核外电子未成对电子数最多的;
④Y原子外围电子排布msnmpn(m≠n);
⑤R原子核外L层电子数为奇数;
⑥Q、X原子最外层p轨道的电子数分别为2和4。
请回答下列问题:
(1)W原子的原子结构示意图为___________ 。
(2)Z元素位于周期表___________ 区;Z2+的核外电子排布式是___________ 。
(3)Q的最高价氧化物的电子式是___________ 。
(4)Q、Y形成的最简单气态氢化物的稳定性:___________ >___________ 。(填化学式)
(5)Q、R、X三种元素的第一电离能数值由小到大的顺序为___________ (用元素符号填空)。
(6)解释YQ晶体和Y晶体熔点高低的原因:___________ 。
(7)六种元素中,电负性最大与最小的两种非金属元素形成的化合物是___________ 。(填化学式)
Ⅱ.在5-氨基四唑(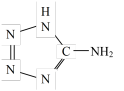 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
(1)基态Ga原子核外电子排布式为___________ ; N原子的外围电子轨道表示式为___________ 。
(2)在1 mol 5-氨基四唑中含有的σ键的数目为___________ 。
(3)以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化钛化合物。其结构是用碳原子取代氮化钛晶胞(结构如下图)顶点的氮原子,这种碳氮化钛化合物的化学式为___________ 。

Ⅰ.Q、R、X、Y、W、Z六种元素的原子序数依次增大。已知:
①Q、R、X、Y均为短周期主族元素;
②Z的原子序数为29;
③W是前四周期元素中核外电子未成对电子数最多的;
④Y原子外围电子排布msnmpn(m≠n);
⑤R原子核外L层电子数为奇数;
⑥Q、X原子最外层p轨道的电子数分别为2和4。
请回答下列问题:
(1)W原子的原子结构示意图为
(2)Z元素位于周期表
(3)Q的最高价氧化物的电子式是
(4)Q、Y形成的最简单气态氢化物的稳定性:
(5)Q、R、X三种元素的第一电离能数值由小到大的顺序为
(6)解释YQ晶体和Y晶体熔点高低的原因:
(7)六种元素中,电负性最大与最小的两种非金属元素形成的化合物是
Ⅱ.在5-氨基四唑(
 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。(1)基态Ga原子核外电子排布式为
(2)在1 mol 5-氨基四唑中含有的σ键的数目为
(3)以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化钛化合物。其结构是用碳原子取代氮化钛晶胞(结构如下图)顶点的氮原子,这种碳氮化钛化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】单晶边缘纳米催化剂技术为工业上有效利用二氧化碳提供了一条经济可行的途径,其中单晶氧化镁负载镍催化剂表现出优异的抗积碳和抗烧结性能。
(1)基态镍原子的价层电子排布图为___________ 。
(2)氧化镁载体及镍催化反应中涉及到CH4、CO2和CH3OH等物质。元素Mg、O和C的第一电离能由小到大排序为___________ ;在上述三种物质的分子中碳原子杂化类型不同于其他两种的是______ ,立体构型为正四面体的分子是___________ ,三 种物质中沸点最高的是CH3OH,其原因是___________ 。
(3)Ni与CO在60~80°C时反应生成Ni(CO)4气体,在Ni(CO)4分子中与Ni形成配位键的原子是___________ ,Ni(CO)4晶体类型是___________ 。
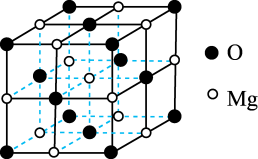
(4)已知MgO具有NaCl型晶体结构,其结构如图所示。已知MgO晶胞棱长为0.42nm,则MgO的密度为___________ g·cm-3(保留小数点后一位,下同);相邻Mg2+之间的最短距离为___________ nm。(已知 =1.414,
=1.414,  =1.732)
=1.732)
(1)基态镍原子的价层电子排布图为
(2)氧化镁载体及镍催化反应中涉及到CH4、CO2和CH3OH等物质。元素Mg、O和C的第一电离能由小到大排序为
(3)Ni与CO在60~80°C时反应生成Ni(CO)4气体,在Ni(CO)4分子中与Ni形成配位键的原子是
(4)已知MgO具有NaCl型晶体结构,其结构如图所示。已知MgO晶胞棱长为0.42nm,则MgO的密度为
 =1.414,
=1.414,  =1.732)
=1.732)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】三明清流“天芳悦潭”温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。
回答下列问题:
(1)基态Ge原子价电子排布图为___ 。
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:Na2GeO3;二锗酸钠:Na2Ge2O5等),也能形成类似于烷烃的锗烷(GenH2n+2)。
①Na2GeO3中锗原子的杂化方式是___ 。
②推测1molGenH2n+2中含有的σ键的数目是__ (用NA表示阿伏加德罗常数值)。
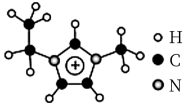
(3)利用离子液体[EMIM][AlCl4]可电沉积还原金属Ge,其熔点只有7℃,其中EMIM+结构如图所示。
①该物质的晶体类型是___ 。
②EMIM+离子中组成元素的电负性由小到大的顺序是___ 。
(4)独立的NH3分子中H—N—H的键角为107.3º,[Zn(NH3)6]2+离子中H—N—H的键角__ 107.3º(填“大于”、“小于”或“等于”)。
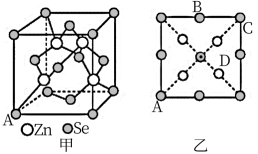
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是___ ;已知晶胞边长为apm,乙图为甲图的俯视图,A点坐标为(0,0,0),B点坐标为( ,a,
,a, ),则D点坐标为
),则D点坐标为___ ;若该晶胞密度为ρg·cm-3,则阿伏加德罗常数NA为___ (只列出计算式)。
回答下列问题:
(1)基态Ge原子价电子排布图为
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:Na2GeO3;二锗酸钠:Na2Ge2O5等),也能形成类似于烷烃的锗烷(GenH2n+2)。
①Na2GeO3中锗原子的杂化方式是
②推测1molGenH2n+2中含有的σ键的数目是
(3)利用离子液体[EMIM][AlCl4]可电沉积还原金属Ge,其熔点只有7℃,其中EMIM+结构如图所示。

①该物质的晶体类型是
②EMIM+离子中组成元素的电负性由小到大的顺序是
(4)独立的NH3分子中H—N—H的键角为107.3º,[Zn(NH3)6]2+离子中H—N—H的键角
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是
 ,a,
,a, ),则D点坐标为
),则D点坐标为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】红土镍矿渣主要成分包含铁、钴、镍、锰、铬、硅的氧化物,为节约和充分利用资源,利用如下流程进行分离回收。已知该温度下 、
、 的溶度积分别是
的溶度积分别是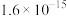 、
、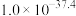 。回答下列问题:
。回答下列问题:
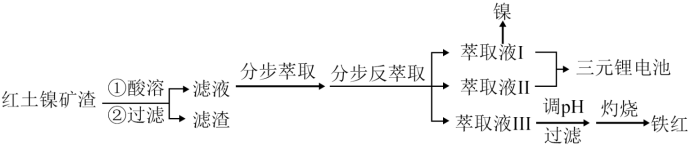
(1)酸溶时,需将红土镍矿渣研成粉末,目的是_______ 。
(2)实验室进行过滤步骤用到的玻璃仪器有_______ 。
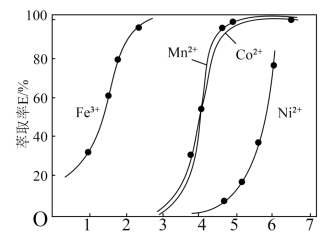
(3)各种离子萃取率与pH关系如图。分步萃取前需通入适量氧气,目的是_______ ,分步萃取浸出金属离子先后顺序为_______ 、_______ 、_______ ,当调 时,溶液中
时,溶液中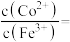
_______ 。
(4)萃取液Ⅰ电解制取镍的阴极电极反应式为_______ 。
(5)写出铬原子的价层电子轨道表示式_______
(6)写出铁红的一种用途:_______ 。
 、
、 的溶度积分别是
的溶度积分别是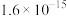 、
、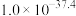 。回答下列问题:
。回答下列问题:
(1)酸溶时,需将红土镍矿渣研成粉末,目的是
(2)实验室进行过滤步骤用到的玻璃仪器有
(3)各种离子萃取率与pH关系如图。分步萃取前需通入适量氧气,目的是
 时,溶液中
时,溶液中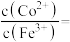

(4)萃取液Ⅰ电解制取镍的阴极电极反应式为
(5)写出铬原子的价层电子轨道表示式
(6)写出铁红的一种用途:
您最近一年使用:0次



