1 . 立德粉ZnS·BaSO4 (也称锌钡白),是一种常用白色颜料。回答下列问题:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧立德粉样品时,钡的焰色为______ (填标号)。
A.黄色 B.砖红色 C.紫色 D.黄绿色
(2)以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:

①在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为______ 。回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO2和一种清洁能源气体,该反应的化学方程式为______ 。
②在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差,其原因是“还原料”表面生成了难溶于水的______ (填化学式)。
③沉淀器中反应的离子方程式为______ 。
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧立德粉样品时,钡的焰色为
A.黄色 B.砖红色 C.紫色 D.黄绿色
(2)以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:

①在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为
②在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差,其原因是“还原料”表面生成了难溶于水的
③沉淀器中反应的离子方程式为
您最近一年使用:0次
2020-03-05更新
|
886次组卷
|
5卷引用:云南省弥勒市第一中学2021-2022学年高二上学期第二次月考化学试题
19-20高二·浙江·期末
2 . 已知化合物M由3种元组成,某学习小组进行了如下实验:
①取适量M,加水完全溶解,无气体产生,溶液呈碱性。取溶液进行焰色反应实验,火焰呈黄色;
②取2.68gM溶于水,加入含 的氢溴酸恰好中和,此时溶液中只含一种溶质;中和后的溶液与硝酸酸化的过量
的氢溴酸恰好中和,此时溶液中只含一种溶质;中和后的溶液与硝酸酸化的过量 溶液反应,得到7.52g的淡黄色沉淀。请回答:
溶液反应,得到7.52g的淡黄色沉淀。请回答:
(1)M中3种元素分别是Na、________ 、________ (用元素符号表示);
(2)M与水反应的化学方程式为________ ;
(3)M中一种元素对应的单质,与等物质的量的 的溶液发生歧化反应,反应产物中含有溴酸钠,同时生成一种无色无味、能使澄清石灰水变浑浊的气体。写出该反应的化学方程式
的溶液发生歧化反应,反应产物中含有溴酸钠,同时生成一种无色无味、能使澄清石灰水变浑浊的气体。写出该反应的化学方程式________ 。
①取适量M,加水完全溶解,无气体产生,溶液呈碱性。取溶液进行焰色反应实验,火焰呈黄色;
②取2.68gM溶于水,加入含
 的氢溴酸恰好中和,此时溶液中只含一种溶质;中和后的溶液与硝酸酸化的过量
的氢溴酸恰好中和,此时溶液中只含一种溶质;中和后的溶液与硝酸酸化的过量 溶液反应,得到7.52g的淡黄色沉淀。请回答:
溶液反应,得到7.52g的淡黄色沉淀。请回答:(1)M中3种元素分别是Na、
(2)M与水反应的化学方程式为
(3)M中一种元素对应的单质,与等物质的量的
 的溶液发生歧化反应,反应产物中含有溴酸钠,同时生成一种无色无味、能使澄清石灰水变浑浊的气体。写出该反应的化学方程式
的溶液发生歧化反应,反应产物中含有溴酸钠,同时生成一种无色无味、能使澄清石灰水变浑浊的气体。写出该反应的化学方程式
您最近一年使用:0次
3 . I.在如图所示的物质转化关系中,C、G、I、M为常见单质,G和M化合可生成最常见液体A,E为黑色粉末,F的焰色反应为黄色,K为一种含有铁元素的白色沉淀,N为红褐色絮状沉淀,I为黄绿色气体,化合物B的摩尔质量为 (部外生成物和反应条件未列出)
(部外生成物和反应条件未列出)
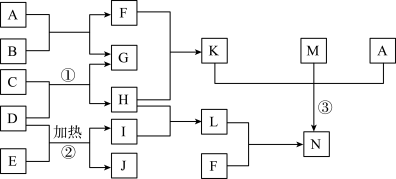
(1)M的化学式为________ 。
(2)B的化学式为________ 。
(3)反应②的化学方程式为________ 。
(4)反应③的化学方程式为________ 。
Ⅱ.今有一混合物的水溶液,只可能含有以下离子中的若干种: 、
、 、
、 、
、 、
、 、
、 、
、 。现取三份各100mL溶液进行如下实验:
。现取三份各100mL溶液进行如下实验:
第一份加入 溶液有沉淀产生;
溶液有沉淀产生;
第二份加入足量 溶液加热后,收集到0.08mol气体;
溶液加热后,收集到0.08mol气体;
第三份加入足量 溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g,根据上述实验;回答以下问题:
溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g,根据上述实验;回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有
________ (填“是”或“否”)。
(2)由第二份进行的实验可知混合物中应含有________ ,其物质的量浓度为________ 。
(3)由第三份进行的实验可知12.54g沉淀的成分为________ (写化学式)。
(4)综合上述实验,你认为以下结论正确的是______
A.该混合物中一定含有 、
、 、
、 、
、 ,可能含有
,可能含有 ,且
,且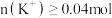
B.该混合物中一定含有 、
、 、
、 ,可能含有
,可能含有 、
、 、
、
C.该混合物中一定含有 、
、 、
、 ,可能含有
,可能含有 、
、
D.该混合物中一定含有 、
、 ,可能含有
,可能含有 、
、 、
、
 (部外生成物和反应条件未列出)
(部外生成物和反应条件未列出)
(1)M的化学式为
(2)B的化学式为
(3)反应②的化学方程式为
(4)反应③的化学方程式为
Ⅱ.今有一混合物的水溶液,只可能含有以下离子中的若干种:
 、
、 、
、 、
、 、
、 、
、 、
、 。现取三份各100mL溶液进行如下实验:
。现取三份各100mL溶液进行如下实验:第一份加入
 溶液有沉淀产生;
溶液有沉淀产生;第二份加入足量
 溶液加热后,收集到0.08mol气体;
溶液加热后,收集到0.08mol气体;第三份加入足量
 溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g,根据上述实验;回答以下问题:
溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g,根据上述实验;回答以下问题:(1)由第一份进行的实验推断该混合物是否一定含有

(2)由第二份进行的实验可知混合物中应含有
(3)由第三份进行的实验可知12.54g沉淀的成分为
(4)综合上述实验,你认为以下结论正确的是
A.该混合物中一定含有
 、
、 、
、 、
、 ,可能含有
,可能含有 ,且
,且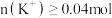
B.该混合物中一定含有
 、
、 、
、 ,可能含有
,可能含有 、
、 、
、
C.该混合物中一定含有
 、
、 、
、 ,可能含有
,可能含有 、
、
D.该混合物中一定含有
 、
、 ,可能含有
,可能含有 、
、 、
、
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
4 . 现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
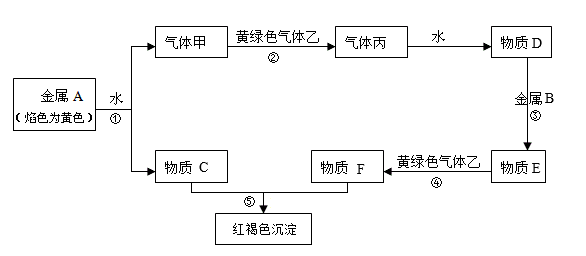
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A________ 、丙________
(2)写出下列反应化学方程式:
反应①________________
反应⑤________________

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
(2)写出下列反应化学方程式:
反应①
反应⑤
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
5 . A、B、C、D、E五种物质所含元素有两种相同,且焰色反应均为黄色,B比A相对更稳定,B是一种淡黄色的固体。C、D是工业上重要的化工原料,也是实验室常用的药品,C、D在一定的条件下可相互转化,F与A、B、C、D在一定的条件下均可发生反应的部分转化关系如图(部分反应物或生成物省略)。
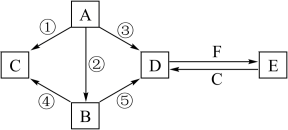
(1)B的化学式___ ,C的俗名为___ 。
(2)在①②③④⑤中,属于氧化还原反应的是___ 。
(3)写出E溶液和C溶液反应的离子方程式:___ 。
(4)写出D转化为C的化学方程式:___ 。

(1)B的化学式
(2)在①②③④⑤中,属于氧化还原反应的是
(3)写出E溶液和C溶液反应的离子方程式:
(4)写出D转化为C的化学方程式:
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
6 . 现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如图反应。(图中有些反应的产物和反应条件没有标出)
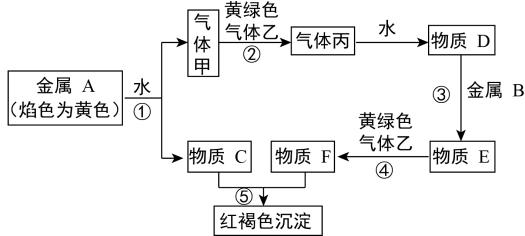
请回答下列问题:
(1)丙的化学式为________
(2)A的一种氧化物为淡黄色固体,该物质的化学式为________
(3)写出气体乙与C溶液反应的化学方程式:________________
(4)写出A与水反应的化学方程式:________________

请回答下列问题:
(1)丙的化学式为
(2)A的一种氧化物为淡黄色固体,该物质的化学式为
(3)写出气体乙与C溶液反应的化学方程式:
(4)写出A与水反应的化学方程式:
您最近一年使用:0次
7 . 如图所涉及的物质均为中学化学中的常见物质(反应①②的一些生成物已经略去,有些反应的条件未列出)。
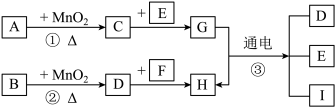
已知:
①C、D、E、F都是单质,其中C、D、E为气体,F为固体。
②化合物A的焰色反应为紫色、化合物H的焰色反应为黄色。
请按要求回答下列问题:
(1)A的化学式为________ 。
(2)指出 在相关反应中的作用:反应①中是
在相关反应中的作用:反应①中是_______ ,反应②中是______ 。
A.还原剂 B.氧化剂 C.催化剂
(3)G、H混合液通电后发生的化学反应方程式为__________ ,标准状况下每生成1mol气体D转移的电子数为________ mol。

已知:
①C、D、E、F都是单质,其中C、D、E为气体,F为固体。
②化合物A的焰色反应为紫色、化合物H的焰色反应为黄色。
请按要求回答下列问题:
(1)A的化学式为
(2)指出
 在相关反应中的作用:反应①中是
在相关反应中的作用:反应①中是A.还原剂 B.氧化剂 C.催化剂
(3)G、H混合液通电后发生的化学反应方程式为
您最近一年使用:0次
19-20高二·浙江·期末
8 . 化合物X由四种常见元素组成,摩尔质量为100g/mol~150g/mol,其焰色反应为黄色,X的水溶液能使紫色石蕊试液变红色。取一定量的X进行下图实验:
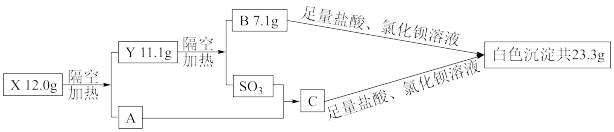
回答下列问题:
(1)X溶于水的电离方程式是____________________________________________________
(2)简述气体A的检验方法______________________________________________________
(3)Y→B+SO3的化学反应方程式___________________________________________________

回答下列问题:
(1)X溶于水的电离方程式是
(2)简述气体A的检验方法
(3)Y→B+SO3的化学反应方程式
您最近一年使用:0次
9 . Ⅰ.某化合物M(仅含三种短周期元素)是一种储氢材料。为探究M的组成和性质,设计并完成如下实验:
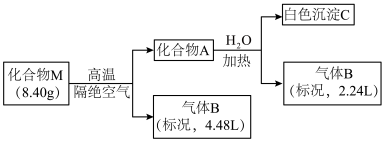
已知:化合物A仅含两种元素;气体B能使湿润的红色石蕊试纸变蓝。
请回答:(1)化合物M的组成元素是______________ (用元素符号表示)。
(2)化合物A与水反应的化学方程式是______________________ 。
(3)镁带在足量气体B中燃烧可生成化合物M和一种单质气体,该反应的化学方程式是______ 。
II.无机盐X仅由三种短周期元素组成,其相对分子质量为238,原子个数比为1︰1︰4。将23.8gX与水共热,生成一种有特殊臭味的气体单质A和某强酸的酸式盐溶液B,B的焰色反应呈黄色,在溶液B中加入足量的BaCl2溶液,产生46.6g白色沉淀。请推测并回答:
(4)单质A有很强的氧化性,可用于净化空气,饮用水消毒等。A中组成元素的简单离子结构示意图为___________________________ 。
(5)X的化学式_____________ 。
(6)实验室可通过低温电解B溶液制备X。该电解反应的化学方程式___________________ 。
(7)X氧化能力强,对环境友好,可用于脱硝、脱硫。在碱性条件下,X氧化NO的离子方程式_____________________ 。
(8)X溶液与铜反应时先慢后快。某同学认为除反应放热这一因素外,还有一种可能是反应生成的Cu2+对后续反应起催化作用,为此他设计了如下实验方案:取少量铜粉置于试管中,先加入少量CuSO4溶液,再加入X溶液,振荡,观察现象。若加入硫酸铜溶液的反应快,说明Cu2+起了催化作用,反之Cu2+不起作用。写出X与铜反应的化学方程式________ ,判断该同学设计的验证方法合理性并说明理由_________ 。

已知:化合物A仅含两种元素;气体B能使湿润的红色石蕊试纸变蓝。
请回答:(1)化合物M的组成元素是
(2)化合物A与水反应的化学方程式是
(3)镁带在足量气体B中燃烧可生成化合物M和一种单质气体,该反应的化学方程式是
II.无机盐X仅由三种短周期元素组成,其相对分子质量为238,原子个数比为1︰1︰4。将23.8gX与水共热,生成一种有特殊臭味的气体单质A和某强酸的酸式盐溶液B,B的焰色反应呈黄色,在溶液B中加入足量的BaCl2溶液,产生46.6g白色沉淀。请推测并回答:
(4)单质A有很强的氧化性,可用于净化空气,饮用水消毒等。A中组成元素的简单离子结构示意图为
(5)X的化学式
(6)实验室可通过低温电解B溶液制备X。该电解反应的化学方程式
(7)X氧化能力强,对环境友好,可用于脱硝、脱硫。在碱性条件下,X氧化NO的离子方程式
(8)X溶液与铜反应时先慢后快。某同学认为除反应放热这一因素外,还有一种可能是反应生成的Cu2+对后续反应起催化作用,为此他设计了如下实验方案:取少量铜粉置于试管中,先加入少量CuSO4溶液,再加入X溶液,振荡,观察现象。若加入硫酸铜溶液的反应快,说明Cu2+起了催化作用,反之Cu2+不起作用。写出X与铜反应的化学方程式
您最近一年使用:0次
10 . 某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制出如下转化关系图(部分反应物或产物略去),并用于研究物质A、B、C、D的性质及其变化。
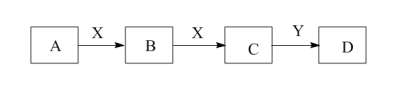
(1)若A是黄绿色气体,X是生活中应用最大量的金属,D是白色固体。
① 组成A的元素在周期表中的位置是______ 。
② 下列说法正确的是______ (填字母)。
a.B的水溶液中加入KSCN溶液,变为红色
b.C只具有还原性
c.若Y是碱,D放置在空气中会迅速变为灰绿色,最终变为红褐色
(2)若A、B、C、D的焰色反应均为黄色,X的固体俗称干冰。
① B转化为C的离子方程式是______ 。
② A用于呼吸面具或潜水艇中氧气的来源,则A和X反应生成1 mol B时,转移电子数为______ 。
③ C与Y反应生成X的离子方程式_________________ 。

(1)若A是黄绿色气体,X是生活中应用最大量的金属,D是白色固体。
① 组成A的元素在周期表中的位置是
② 下列说法正确的是
a.B的水溶液中加入KSCN溶液,变为红色
b.C只具有还原性
c.若Y是碱,D放置在空气中会迅速变为灰绿色,最终变为红褐色
(2)若A、B、C、D的焰色反应均为黄色,X的固体俗称干冰。
① B转化为C的离子方程式是
② A用于呼吸面具或潜水艇中氧气的来源,则A和X反应生成1 mol B时,转移电子数为
③ C与Y反应生成X的离子方程式
您最近一年使用:0次



