名校
解题方法
1 . 某学习小组研究碳酸钠的性质进行以下实验:
(1)欲检验 中存在钠元素,可使用的方法___________。
中存在钠元素,可使用的方法___________。
(2)欲除去 中少量
中少量 ,可使用的方法___________。
,可使用的方法___________。
(1)欲检验
 中存在钠元素,可使用的方法___________。
中存在钠元素,可使用的方法___________。| A.沉淀法 | B.显色法 | C.焰色反应 | D.气体法 |
 中少量
中少量 ,可使用的方法___________。
,可使用的方法___________。| A.加入过量盐酸 | B.直接加热 | C.加入石灰水 | D.通 过量 过量 |
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
(1)基态钛原子的价层电子排布式为_______ ,其原子核外电子的空间运动状态有_______ 种,共有_______ 种运动状态不同的电子。
(2)基态Si原子,若其电子排布式表示为[Ne]3s23p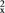 违背了
违背了_______ 。
(3)①基态Cu原子有_______ 种不同能级的电子。铜或铜盐的焰色试验为绿色,该光谱是_______ (填“吸收光谱”或“发射光谱”)。
②N原子中最高能级的电子的电子云轮廓图为_______ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是_______ 。
(1)基态钛原子的价层电子排布式为
(2)基态Si原子,若其电子排布式表示为[Ne]3s23p
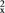 违背了
违背了(3)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
您最近一年使用:0次
3 . 现有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
(2) 元素的原子核外共有
元素的原子核外共有___________ 种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3) 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是___________ 。
(4) 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是___________ 。
(5) 位于元素周期表中
位于元素周期表中___________ 区(按电子排布分区),其基态原子的价层电子排布式为___________ 。
(6)G单质投入水中所得溶液阳离子检验方法___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
 元素是形成化合物种类最多的元素 元素是形成化合物种类最多的元素 |
 元素基态原子的核外 元素基态原子的核外 能级电子数比 能级电子数比 能级电子总数少1个 能级电子总数少1个 |
 元素基态原子的核外 元素基态原子的核外 轨道中有两个未成对电子 轨道中有两个未成对电子 |
 元素的气态基态原子的第一至第四电离能分别是 元素的气态基态原子的第一至第四电离能分别是 , , , , , ,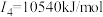 |
 元素的主族序数与周期数的差为4 元素的主族序数与周期数的差为4 |
 元素是前四周期中电负性最小的元素 元素是前四周期中电负性最小的元素 |
 元素位于元素周期表中的第8列 元素位于元素周期表中的第8列 |
 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)(2)
 元素的原子核外共有
元素的原子核外共有(3)
 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是(4)
 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是(5)
 位于元素周期表中
位于元素周期表中(6)G单质投入水中所得溶液阳离子检验方法
您最近一年使用:0次
名校
解题方法
4 . 黑火药的主要成分为木炭(C)、硫黄(S)和火硝 。请回答下列问题。
。请回答下列问题。
(1)基态碳原子的电子排布式为_______ 。
(2)下列轨道表示式能表示基态氮原子的核外电子排布的是_______(填标号)。
(3)C、N、O三种元素的第一电离能由大到小的顺序为_______ 。
(4)Se元素位于第4周期,与O、S同主族。
①基态Se原子中具有_______ 种运动状态不同的电子。其中能量最高的电子占据轨道的形状为_______ 。
②O、S、Se三种元素的电负性依次_______ (填“增大”或“减小”)。
(5)用铂丝蘸取 溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是
溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是_______ 。第4周期元素的基态原子中,与基态K原子具有相同最外层电子数的是_______ (填元素符号)。
 。请回答下列问题。
。请回答下列问题。(1)基态碳原子的电子排布式为
(2)下列轨道表示式能表示基态氮原子的核外电子排布的是_______(填标号)。
A.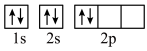 | B.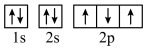 |
C.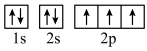 | D.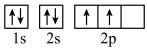 |
(3)C、N、O三种元素的第一电离能由大到小的顺序为
(4)Se元素位于第4周期,与O、S同主族。
①基态Se原子中具有
②O、S、Se三种元素的电负性依次
(5)用铂丝蘸取
 溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是
溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是
您最近一年使用:0次
名校
解题方法
5 . 按要求回答下列问题:
(1)对含有K2CO3的样品进行焰色试验,需要准备的仪器和试剂有:铂丝、酒精灯、___________ 和___________ 。
(2)高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: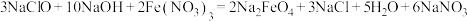 。回答下列问题:
。回答下列问题:
①用氯气制备 的反应原理为
的反应原理为___________ (化学方程式)
②制备高铁酸钠的反应中 体现了
体现了___________ (填“还原性”、“氧化性”或“氧化性和还原性”)
(3)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少了3.1g,所得固体与足量盐酸充分反应(假设CO2完全逸出)。计算:
①混合物中Na2CO3和NaHCO3的物质的量之比为___________ 。
②加入足量盐酸充分反应后产生的CO2在标准状况下的体积为___________ L。
(1)对含有K2CO3的样品进行焰色试验,需要准备的仪器和试剂有:铂丝、酒精灯、
(2)高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: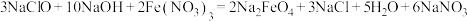 。回答下列问题:
。回答下列问题:①用氯气制备
 的反应原理为
的反应原理为②制备高铁酸钠的反应中
 体现了
体现了(3)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少了3.1g,所得固体与足量盐酸充分反应(假设CO2完全逸出)。计算:
①混合物中Na2CO3和NaHCO3的物质的量之比为
②加入足量盐酸充分反应后产生的CO2在标准状况下的体积为
您最近一年使用:0次
6 . 单质硅是制造太阳能电池板的主要原料,制备电池板时还需添加硼、氮、钛、钴、钙等多种化学物质。
请回答下列问题:
(1)基态硼原子的电子排布式为______ ,下列钴原子的价层电子轨道表示式中,不符合洪特规则的是______ (填选项字母)。
A.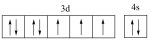 B.
B.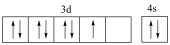
C.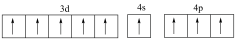 D.
D.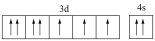
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为______ (用元素符号表示),原因为______ 。
(3)钛元素位于元素周期表______ 区;基态钛原子中,最外层电子的电子云轮廓图为______ 。
(4) 在火焰上灼烧时火焰的颜色为砖红色,从微观角度解释部分金属元素在火焰上灼烧呈现不同颜色的原因:
在火焰上灼烧时火焰的颜色为砖红色,从微观角度解释部分金属元素在火焰上灼烧呈现不同颜色的原因:______ 。
请回答下列问题:
(1)基态硼原子的电子排布式为
A.
 B.
B.
C.
 D.
D.
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为
(3)钛元素位于元素周期表
(4)
 在火焰上灼烧时火焰的颜色为砖红色,从微观角度解释部分金属元素在火焰上灼烧呈现不同颜色的原因:
在火焰上灼烧时火焰的颜色为砖红色,从微观角度解释部分金属元素在火焰上灼烧呈现不同颜色的原因:
您最近一年使用:0次
名校
7 . 生活离不开化学。家庭厨卫中有许多中学化学常见的物质,它们的主要成分如下表。
回答下列问题:
(1)以上主要成分中属于弱电解质的有_______ (填序号)。
(2)当碱面不慎洒落在天然气火焰上,观察到的现象是_______ 。
(3)KAl(SO4)2·12H2O的电离方程式为_______ 。
(4)Na2CO3溶液中混有少量NaHCO3,可加适量的NaOH溶液除杂,离子反应方程式为_______ ;Na2CO3固体中若含有少量NaHCO3,可采取的除杂方法为_______ 。
(5)NaHCO3溶液与白醋反应的离子方程式为_______ 。
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:_______ 。
| 商品 | 食盐 | 碱面 | 84消毒液 | 发酵粉 |
| 主要成分 | ①NaCl | ②Na2CO3 | ③NaClO | ④ NaHCO3⑤KAl(SO4)2·12H2O |
| 商品 | 料酒 | 白醋 | 洁厕灵 | \ |
| 主要成分 | ⑥C2H5OH | ⑦CH3COOH | ⑧HCl |
(1)以上主要成分中属于弱电解质的有
(2)当碱面不慎洒落在天然气火焰上,观察到的现象是
(3)KAl(SO4)2·12H2O的电离方程式为
(4)Na2CO3溶液中混有少量NaHCO3,可加适量的NaOH溶液除杂,离子反应方程式为
(5)NaHCO3溶液与白醋反应的离子方程式为
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
您最近一年使用:0次
2023-02-28更新
|
108次组卷
|
2卷引用:河北省保定市六校联盟2022-2023学年高二下学期7月期末考试化学试题
8 . A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
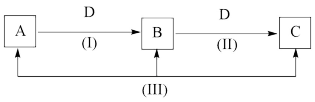
(1)若A、B、C的焰色反应均为黄色,A的水溶液能使酚酞溶液呈红色,C为发酵粉的主要成分之一,D的过度排放会造成温室效应。
①B的化学式为___________ ;D中化学键的类型为___________ (填“离子键”或“共价键”)
②反应Ⅲ的离子方程式是___________ 。
(2)写出Na2O2做防毒面具时涉及到的化学反应的化学方程式:___________ 、___________ 。
(3)写出Al(OH)3受热分解的化学方程式:___________ 。

(1)若A、B、C的焰色反应均为黄色,A的水溶液能使酚酞溶液呈红色,C为发酵粉的主要成分之一,D的过度排放会造成温室效应。
①B的化学式为
②反应Ⅲ的离子方程式是
(2)写出Na2O2做防毒面具时涉及到的化学反应的化学方程式:
(3)写出Al(OH)3受热分解的化学方程式:
您最近一年使用:0次
名校
9 . “鲜花保鲜剂”能延长鲜花的寿命,使人愉悦身心。如表是500mL“鲜花保鲜剂”中含有的成分,阅读后完成以下问题:
(1)“鲜花保鲜剂”的下列成分中,不属于电解质的是_____ 。
(2)计算,500mL“鲜花保鲜剂”中硫酸钾的物质的量是_____ ,其中K+的物质的量浓度是_____ ,溶液中含_____ 个SO 。
。
(3)写出“鲜花保鲜剂”中高锰酸钾的电离方程式_____ 。
(4)鉴定“鲜花保鲜剂”中含有K+的实验方法为_____ 。
(5)某同学在配制500mL“鲜花保鲜剂”溶液时,向容量瓶中转移溶液的操作如图所示,请指出图中的两处错误。
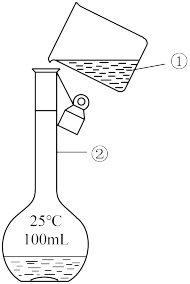
①_____ ;②_____ 。
(6)本实验中,会用到胶头滴管,作用是_____ 。
(7)在溶液配制过程中,下列操作造成所得溶液浓度偏小的是_____ 。
| 成分 | 质量(g) |
| 蔗糖(C12H22O11) | 25.000 |
| 硫酸钾 | 0.870 |
| 阿司匹林 | 0.180 |
| 高锰酸钾 | 0.316 |
| 硝酸银 | 0.075 |
| A.蔗糖 | B.硫酸钾 | C.高锰酸钾 | D.硝酸银 |
 。
。(3)写出“鲜花保鲜剂”中高锰酸钾的电离方程式
(4)鉴定“鲜花保鲜剂”中含有K+的实验方法为
| A.显色法 | B.沉淀法 | C.气体法 | D.焰色反应 |

①
(6)本实验中,会用到胶头滴管,作用是
(7)在溶液配制过程中,下列操作造成所得溶液浓度偏小的是
| A.定容时俯视容量瓶刻度线 |
| B.容量瓶未干燥,里面有少量蒸馏水 |
| C.溶液由烧杯转移到容量瓶时有少量溶液溅到瓶外 |
| D.定容摇匀后发现液面低于容量瓶的刻度线,未做处理 |
您最近一年使用:0次
2023-01-10更新
|
107次组卷
|
2卷引用:上海市七宝中学附属鑫都实验中学2022-2023学年高二下学期阶段测试(3月)化学试题
10 . 向盛有水的烧杯中加入 固体,得到溶液①,再向溶液①中通入
固体,得到溶液①,再向溶液①中通入 气体,得到溶液②。
气体,得到溶液②。
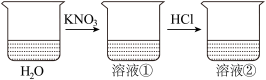
(1)用文字描述溶液②的组成,并在图中标示出来_________ 。
(2)你认为可以通过哪些实验研究溶液②的性质?请标注在上图中______ 。
(3)向溶液②中加入 固体,发现溶液呈黄色,请分析溶液呈黄色的可能原因
固体,发现溶液呈黄色,请分析溶液呈黄色的可能原因________ 。
 固体,得到溶液①,再向溶液①中通入
固体,得到溶液①,再向溶液①中通入 气体,得到溶液②。
气体,得到溶液②。
(1)用文字描述溶液②的组成,并在图中标示出来
(2)你认为可以通过哪些实验研究溶液②的性质?请标注在上图中
(3)向溶液②中加入
 固体,发现溶液呈黄色,请分析溶液呈黄色的可能原因
固体,发现溶液呈黄色,请分析溶液呈黄色的可能原因
您最近一年使用:0次



