名校
解题方法
1 . 下列实验方案、现象、结论的对应关系错误的是
| 选项 | 操作 | 现象 | 解释 |
| A | 用毛皮摩擦过的带电橡胶棒靠近 液流 液流 |  液流方向不变 液流方向不变 |  分子无极性 分子无极性 |
| B | 将含有稀硫酸的蔗糖溶液水浴加热后,加入新制氢氧化铜悬浊液并加热 | 未产生砖红色沉淀 | 蔗糖未水解 |
| C | 向苯酚悬浊液中加入 溶液 溶液 | 溶液变澄清 | 苯环对羟基有影响 |
| D | 向饱和碳酸钠溶液里通入过量的 | 有晶体析出 |  溶解度小 溶解度小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列实验方法不能达到相应实验目的的是
| 选项 | 实验目的 | 实验方法 |
| A | 比较 和 和 的热稳定性 的热稳定性 | 分别加热 和 和 固体,将产生的气体通入澄清石灰水中,观察实验现象 固体,将产生的气体通入澄清石灰水中,观察实验现象 |
| B | 验证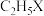 (X代表 (X代表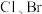 、I)中卤素原子的种类 、I)中卤素原子的种类 | 向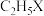 中加入过量的 中加入过量的 溶液,加热一段时间后静置,取少量上层清液于试管中,加入 溶液,加热一段时间后静置,取少量上层清液于试管中,加入 溶液,观察实验现象 溶液,观察实验现象 |
| C | 比较水分子中的氢原子和乙醇羟基中的氢原子的活泼性 | 相同条件下,用金属钠分别与水和乙醇反应,观察实验现象 |
| D | 验证葡萄糖中含有醛基 | 在试管中加入 溶液,滴入5滴 溶液,滴入5滴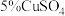 溶液,振荡后加入 溶液,振荡后加入 葡萄糖溶液,加热,观察实验现象 葡萄糖溶液,加热,观察实验现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . Ⅰ.下表是生活生产中常见的物质,表中列出了它们的一种主要成分(其中加碘盐是氯化钠中添加适量的 ,其他成分未列出)
,其他成分未列出)
(1)请你对表中①~⑦的主要成分进行分类,是电解质的是______ ,是非电解质的是______ 。(填序号)
(2)写出④在水中的电离方程式____________ 。
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:______________ 。
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为
(4)反应中氧化剂与还原剂的个数之比为______ ,其中 反应中显出来的性质是
反应中显出来的性质是______ 。
(5)该反应中的氧化产物为______ ,每生成11.2L(标准状况下)的NO,转移的电子个数为______ 。
 ,其他成分未列出)
,其他成分未列出)名称 | 天然气 | 白酒 | 醋酸 | 小苏打 |
主要成分 | ① | ② | ③ | ④ |
名称 | 熟石灰 | 铜线 | 加碘盐 | |
主要成分 | ⑤ | ⑥Cu | ⑦NaCl和 |
(2)写出④在水中的电离方程式
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为

(4)反应中氧化剂与还原剂的个数之比为
 反应中显出来的性质是
反应中显出来的性质是(5)该反应中的氧化产物为
您最近一年使用:0次
解题方法
4 . 有A、B两种常见化合物,其焰色试验均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去)。回答下列问题:______ 。
(2)B加热产生D的化学方程式:____________ 。
(3)请用化学方程式表示A在潜水艇中的一种重要用途:____________ 。
(4)A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物E,其化学式为______ 。
(5)写出一种将E转化为B的化学方程式:____________ 。

(2)B加热产生D的化学方程式:
(3)请用化学方程式表示A在潜水艇中的一种重要用途:
(4)A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物E,其化学式为
(5)写出一种将E转化为B的化学方程式:
您最近一年使用:0次
名校
5 . 按要求回答下列问题:
(1)现有以下物质:①Cl2②CO2③Na2O④NaHSO4⑤漂白粉⑥NaOH溶液⑦Ba(OH)2,其中属于酸性氧化物的有
(2)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量为
(3)下列是部分短周期中第二、第三周期元素的原子半径及主要化合价。
| 元素代号 | A | B | C | D | E | F | G |
原子半径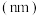 | 0.186 | 0.160 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
①七种元素的最高价氧化物的水化物中,酸性最强的是
②B、E、G的离子半径由大到小的顺序是
③元素G的最简单氢化物的结构式
(4)200mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2充分反应后,得到Na2CO3和NaHCO3的混合溶液,向上述所得溶液中,逐滴加入2mol/L的盐酸,所得气体的体积与所加盐酸的体积关系如图所示(不考虑体积变化):
B点时,反应所得溶液中溶质的物质的量浓度是
(5)向浑浊的水中加入明矾(KAl(SO4)2·12H2O)后,水可得到净化。写出硫酸铝钾在水中的电离方程式:
您最近一年使用:0次
名校
6 . Li2CO3是制备锂离子电极材料LiFePO4的重要原料。以盐湖卤水(主要含有NaCl、MgCl2、LiCl和Na2B4O7等)为原料提取Li2CO3并制备LiFePO4的工艺流程如图所示:

已知:“日晒蒸发喷雾干燥”后固体含NaCl、LiCl、MgCl2•6H2O等。
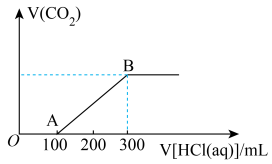
(1)硼酸在水中的溶解度随温度的变化关系如图所示:
已知:H3BO3+H2O⇌[B(OH)4]-+H+。6.2gH3BO3最多与______ mL2.5mol/LNaOH溶液完全反应。“酸化脱硼”中采用______ (填“加热”或“冷却”),其目的是______ 。
(2)“水浸”后的溶液中溶质的主要成分是______ 。
(3)“蒸发分解”生成Li2CO3的化学方程式为______ 。
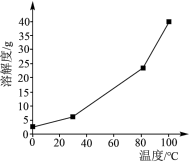
(4)已知不同温度下蒸发分解得到Li2CO3的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是______ ,制得的Li2CO3沉淀需要进行洗涤,具体操作为______ 。
(5)制备LiFePO4时同时生成CO2,其中FePO4与C6H12O6物质的量之比为24:1,该化学反应方程式为______ 。

已知:“日晒蒸发喷雾干燥”后固体含NaCl、LiCl、MgCl2•6H2O等。
(1)硼酸在水中的溶解度随温度的变化关系如图所示:

已知:H3BO3+H2O⇌[B(OH)4]-+H+。6.2gH3BO3最多与
(2)“水浸”后的溶液中溶质的主要成分是
(3)“蒸发分解”生成Li2CO3的化学方程式为
(4)已知不同温度下蒸发分解得到Li2CO3的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是

(5)制备LiFePO4时同时生成CO2,其中FePO4与C6H12O6物质的量之比为24:1,该化学反应方程式为
您最近一年使用:0次
名校
7 . 下列所选仪器或操作符合实验要求的是
| A | B | C | D |
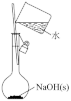 |  | 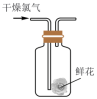 | 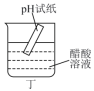 |
配制一定物质的量浓度的 溶液 溶液 | 比较NaHCO3和Na2CO3的热稳定性 | 检验干燥 是否具有漂白性 是否具有漂白性 | 测定醋酸溶液的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下列离子方程式正确的是
A.向硫酸铜溶液中加入适量的氢氧化钡溶液:Ba2++SO =BaSO4↓ =BaSO4↓ |
| B.向氯化亚铁中通入氯气:Fe2++Cl2=Fe3++Cl- |
| C.碳酸钙溶于稀醋酸中CaCO3+2H+=Ca2++H2O+CO2↑ |
D.氢氧化钠溶液中加入过量碳酸氢钙溶液:Ca2++HCO +OH-=CaCO3↓+H2O +OH-=CaCO3↓+H2O |
您最近一年使用:0次
名校
9 . 以下物质之间的每步转化中,不能都通过一步实现的是
A. |
B. |
C.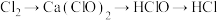 |
D.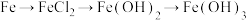 |
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式与所给事实不相符的是
A. 制备84消毒液(主要成分是NaClO): 制备84消毒液(主要成分是NaClO): |
B.食醋去除水垢中的 : :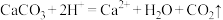 |
C.利用覆铜板制作印刷电路板: |
D.小苏打治疗胃酸过多: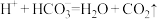 |
您最近一年使用:0次







