名校
1 . 我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要流程如下(部分物质已略去):
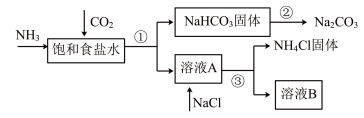
(1)①~③所涉及的操作方法中,包含过滤的是___________ (填序号)。
(2)根据上述流程图,将化学方程式补充完整:________
NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(3)煅烧NaHCO3固体的化学方程式是___________ 。
(4)下列联合制碱法流程说法正确的是___________ (填字母)。
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH 、Cl-
、Cl-
d.①中NaHCO3析出是因为一定条件下NaHCO3的溶解度最小
(5)某纯碱样品中含杂质NaCl,取质量为ag的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到bg固体物质,则此样品中Na2CO3的质量分数为___________ 。(列出表达式即可)

(1)①~③所涉及的操作方法中,包含过滤的是
(2)根据上述流程图,将化学方程式补充完整:
NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(3)煅烧NaHCO3固体的化学方程式是
(4)下列联合制碱法流程说法正确的是
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH
 、Cl-
、Cl-d.①中NaHCO3析出是因为一定条件下NaHCO3的溶解度最小
(5)某纯碱样品中含杂质NaCl,取质量为ag的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到bg固体物质,则此样品中Na2CO3的质量分数为
您最近一年使用:0次
名校
2 . 向 、
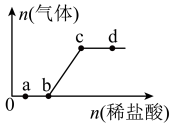
、 的混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸的量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是
的混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸的量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是
 、
、 的混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸的量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是
的混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸的量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是
A.a点对应的溶液中: 、 、 、 、 、 、 |
B.b点对应的溶液中: 、 、 、 、 、 、 |
C.c点对应的溶液中: 、 、 、 、 、 、 |
D.d点对应的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
3 . 某种胃药的有效成分为碳酸氢钠,测定其中碳酸氢钠含量的操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应),该测定实验共进行了四次:
①配制250mL 盐酸和100mL
盐酸和100mL 的NaOH溶液
的NaOH溶液
②向一粒研碎后的药片中加入20.00mL蒸馏水
③用 的NaOH溶液中和过量的盐酸,记录所消耗NaOH溶液的体积
的NaOH溶液中和过量的盐酸,记录所消耗NaOH溶液的体积
④加入 的HCl盐酸
的HCl盐酸
请回答下列问题:
(1)正确的操作顺序是___________ (填序号)。
(2)如图为实验室某浓盐酸试剂瓶上的标签的有关内容

①该浓盐酸中溶质的物质的量浓度为___________  。
。
②用该浓盐酸配制本实验所需的盐酸,需要的仪器有烧杯、玻璃棒、量筒、________ 。
③下列实验操作对所配制的盐酸的物质的量浓度有何影响?(填“偏大一偏小”或“无影响”)
A.容量瓶在使用前未干燥,里面有少量蒸馏水:___________ ;
B.定容时俯视刻度线:___________ 。
(3)某同学4次测定所消耗的NaOH溶液的体积如下:
根据这个同学的实验数据,计算这种药片中碳酸氢钠的质量为___________ 。(小数点后保留2位)
①配制250mL
 盐酸和100mL
盐酸和100mL 的NaOH溶液
的NaOH溶液②向一粒研碎后的药片中加入20.00mL蒸馏水
③用
 的NaOH溶液中和过量的盐酸,记录所消耗NaOH溶液的体积
的NaOH溶液中和过量的盐酸,记录所消耗NaOH溶液的体积④加入
 的HCl盐酸
的HCl盐酸请回答下列问题:
(1)正确的操作顺序是
(2)如图为实验室某浓盐酸试剂瓶上的标签的有关内容

①该浓盐酸中溶质的物质的量浓度为
 。
。②用该浓盐酸配制本实验所需的盐酸,需要的仪器有烧杯、玻璃棒、量筒、
③下列实验操作对所配制的盐酸的物质的量浓度有何影响?(填“偏大一偏小”或“无影响”)
A.容量瓶在使用前未干燥,里面有少量蒸馏水:
B.定容时俯视刻度线:
(3)某同学4次测定所消耗的NaOH溶液的体积如下:
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V[NaOH(aq)]/mL | 19.00 | 19.10 | 18.90 | 17.00 |
您最近一年使用:0次
名校
4 . 某实验小组欲探究 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为___________ 。
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①发现 固体完全溶解,而
固体完全溶解,而 固体有剩余,由此得出结论:
固体有剩余,由此得出结论:___________ 。
②同学们在两烧杯中还观察到以下现象。其中,盛放 的烧杯中出现的现象是
的烧杯中出现的现象是___________ (填字母序号)
a.溶液温度升高 b.溶液温度下降
c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置I和II中分别放入药品,将气球内的固体同时倒入试管中。
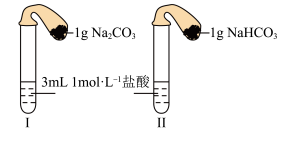
①两试管中均产生气体,___________ 的反应程度更为剧烈。(填“I”或“II”)
②反应结束后,恢复至室温,下列说法正确的是___________ 。
a.装置I的气球体积较大 b.装置II的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:
实施实验后,发现操作1的现象与预测有差异:产生白色沉淀和二氧化碳气体。则该条件下, 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①发现
 固体完全溶解,而
固体完全溶解,而 固体有剩余,由此得出结论:
固体有剩余,由此得出结论:②同学们在两烧杯中还观察到以下现象。其中,盛放
 的烧杯中出现的现象是
的烧杯中出现的现象是a.溶液温度升高 b.溶液温度下降
c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置I和II中分别放入药品,将气球内的固体同时倒入试管中。

①两试管中均产生气体,
②反应结束后,恢复至室温,下列说法正确的是
a.装置I的气球体积较大 b.装置II的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成
 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:| 实验方案 | 预测现象 | 预测依据 |
操作1:向 溶液中滴加 溶液中滴加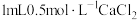 溶液 溶液 | 无白色沉淀 |  溶液中的 溶液中的 浓度很小,不能与 浓度很小,不能与 反应 反应 |
操作2:向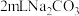 溶液中滴加 溶液中滴加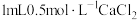 溶液 溶液 | 有白色沉淀 |  溶液中的 溶液中的 浓度较大,能与 浓度较大,能与 发生反应 发生反应 |
 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 某校化学课外小组为了鉴别 和
和 两种白色固体,用不同的方法做了以下实验,如图所示。
两种白色固体,用不同的方法做了以下实验,如图所示。
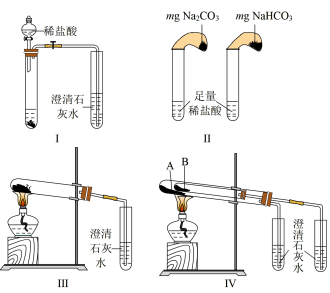
(1)方法Ⅰ是向两种白色粉末中,分别逐滴加入稀盐酸。
方法Ⅰ________ (填“能”或“不能”)鉴别 和
和 。
。
(2)方法Ⅱ能鉴别 和
和 的现象是
的现象是________ .
(3)方法Ⅲ、Ⅳ均能鉴别这两种物质:与方法Ⅲ相比,方法Ⅳ的优点是________(填字母)。
(4)若用方法Ⅳ验证 和
和 的稳定性,则试管B中装入的固体是
的稳定性,则试管B中装入的固体是________ (填化学式)。
(5)除了以上方法,请再写出1种鉴别二者的方法________ 。
 和
和 两种白色固体,用不同的方法做了以下实验,如图所示。
两种白色固体,用不同的方法做了以下实验,如图所示。
(1)方法Ⅰ是向两种白色粉末中,分别逐滴加入稀盐酸。
方法Ⅰ
 和
和 。
。(2)方法Ⅱ能鉴别
 和
和 的现象是
的现象是(3)方法Ⅲ、Ⅳ均能鉴别这两种物质:与方法Ⅲ相比,方法Ⅳ的优点是________(填字母)。
| A.方法Ⅳ比方法Ⅲ复杂 |
| B.方法Ⅳ比方法Ⅲ安全 |
| C.方法Ⅳ比方法Ⅲ操作简便 |
| D.方法Ⅳ可以用一套装置同时进行两个实验,而方法Ⅲ不行 |
(4)若用方法Ⅳ验证
 和
和 的稳定性,则试管B中装入的固体是
的稳定性,则试管B中装入的固体是(5)除了以上方法,请再写出1种鉴别二者的方法
您最近一年使用:0次
6 . 有些挂面在压制过程中会加入少量叫食用碱的碳酸钠。
(一)工业上常采用侯氏制碱法制取碳酸钠,实验装置如图所示(夹持装置省略)。回答:

(1)实验时,先从__________ 管通入__________ 。
(2)有同学建议在b管下端连接多孔球泡装置,理由是__________ 。
(二)碳酸钠样品中往往含有少量的 ,某学习小组设计质量差分析法测定样品中
,某学习小组设计质量差分析法测定样品中 的质量分数。
的质量分数。
(3)将一定质量的样品与足量的稀硫酸反应,采用如下图所示装置,通过称量反应前后盛有碱石灰的干燥管C的质量,利用其质量差计算样品的纯度。

①按照实验顺序排列下列操作步骤__________ gdfch。(某些步骤可以重复)
a.检查装置的气密性 b.打开止水夹 c.缓慢鼓入空气数分钟
d.干燥管C内碱石灰质量为 g e.取
g e.取 g样品装入广口瓶中
g样品装入广口瓶中
f.缓慢加入稀硫酸至不再产生气体为止 g.关闭止水夹
h.称量干燥管C质量为 g(
g( )
)
②在操作h前,要缓慢鼓入空气数分钟,鼓入空气的作用是_________ ,装置A的作用是_________ 。
③若去掉装置D,对实验结果的影响是________ (读“偏大”,“偏小”或“无影响”),样品中 的质量分数
的质量分数_______
(一)工业上常采用侯氏制碱法制取碳酸钠,实验装置如图所示(夹持装置省略)。回答:

(1)实验时,先从
(2)有同学建议在b管下端连接多孔球泡装置,理由是
(二)碳酸钠样品中往往含有少量的
 ,某学习小组设计质量差分析法测定样品中
,某学习小组设计质量差分析法测定样品中 的质量分数。
的质量分数。(3)将一定质量的样品与足量的稀硫酸反应,采用如下图所示装置,通过称量反应前后盛有碱石灰的干燥管C的质量,利用其质量差计算样品的纯度。

①按照实验顺序排列下列操作步骤
a.检查装置的气密性 b.打开止水夹 c.缓慢鼓入空气数分钟
d.干燥管C内碱石灰质量为
 g e.取
g e.取 g样品装入广口瓶中
g样品装入广口瓶中f.缓慢加入稀硫酸至不再产生气体为止 g.关闭止水夹
h.称量干燥管C质量为
 g(
g( )
)②在操作h前,要缓慢鼓入空气数分钟,鼓入空气的作用是
③若去掉装置D,对实验结果的影响是
 的质量分数
的质量分数
您最近一年使用:0次
解题方法
7 . 关注“实验室化学”并加以实践能有效提高同学们的实验素养。用如图所示装置(夹持装置已省略)进行实验,能达到实验目的是


| A.用甲装置收集干燥纯净的氯气 | B.用乙装置制备碳酸氢钠 |
| C.用丙装置观察氢氧化亚铁白色沉淀 | D.用丁装置完成喷泉实验 |
您最近一年使用:0次
名校
8 . 碳酸钠俗称纯碱,用途非常广泛,我国化学家侯德榜发明了“侯氏制碱法”。南宁二中2023级化学兴趣小组在实验室中模拟“侯氏制碱法”制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下所示。
,实验流程如下所示。
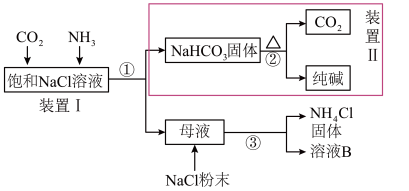
请回答下列问题:
(1)上述流程中,①②③所涉及的操作方法,包含过滤的是___________ (填序号)。过滤时,所需要的玻璃仪器:烧杯、___________ 、___________ 。
(2)向装置Ⅰ的饱和 溶液中通入足量的
溶液中通入足量的 和
和 ,应先通入足量
,应先通入足量___________ (填“ ”或“
”或“ ”)。装置Ⅰ中发生反应的化学方程式为
”)。装置Ⅰ中发生反应的化学方程式为___________ 。
(3)检验装置Ⅱ中制备的纯碱含有 的方法:取少量该纯碱样品溶于水,
的方法:取少量该纯碱样品溶于水,___________ 。
(4)向母液中加入一定量 粉末,存在
粉末,存在 。为使
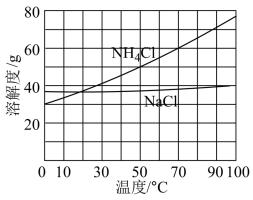
。为使 晶体充分析出并分离,根据下图中
晶体充分析出并分离,根据下图中 和
和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为___________ 、___________ 、过滤、洗涤、干燥。
(5)整个实验流程中,可循环利用的物质的化学式是___________ 。
(6)若装置Ⅱ中得到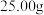 的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了
的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了 ,则原混合物中碳酸钠的质量分数为
,则原混合物中碳酸钠的质量分数为___________ 。
 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下所示。
,实验流程如下所示。
请回答下列问题:
(1)上述流程中,①②③所涉及的操作方法,包含过滤的是
(2)向装置Ⅰ的饱和
 溶液中通入足量的
溶液中通入足量的 和
和 ,应先通入足量
,应先通入足量 ”或“
”或“ ”)。装置Ⅰ中发生反应的化学方程式为
”)。装置Ⅰ中发生反应的化学方程式为(3)检验装置Ⅱ中制备的纯碱含有
 的方法:取少量该纯碱样品溶于水,
的方法:取少量该纯碱样品溶于水,(4)向母液中加入一定量
 粉末,存在
粉末,存在 。为使
。为使 晶体充分析出并分离,根据下图中
晶体充分析出并分离,根据下图中 和
和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为
(5)整个实验流程中,可循环利用的物质的化学式是
(6)若装置Ⅱ中得到
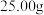 的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了
的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了 ,则原混合物中碳酸钠的质量分数为
,则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
解题方法
9 . 二氧化碳的捕捉与封存是未来实现低碳经济转型的重要途径。
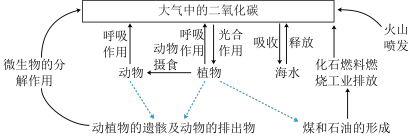
(1)自然界中 主要循环方式如图所示,其中属于“二氧化碳的捕捉与封存”的除了“海水吸收”外,还有
主要循环方式如图所示,其中属于“二氧化碳的捕捉与封存”的除了“海水吸收”外,还有___________ (任写一点)。
(2)科学家设计出烧碱溶液捕捉 法,原理如图所示
法,原理如图所示

①该过程中能实现再生的反应为 和
和___________ 。
②若喷洒完 的
的 溶液后,测得吸收液中的
溶液后,测得吸收液中的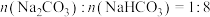 ,则被吸收的
,则被吸收的 在标况下的体积为
在标况下的体积为___________ L。
③下列溶液中,也能用作“捕捉”二氧化碳试剂的是___________ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.稀硫酸
溶液 D.稀硫酸
(3)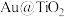 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如下左图所示。制得的甲烷
封存和能量储存双重效果,其原理如下左图所示。制得的甲烷 通过两步法可制取
通过两步法可制取 ,原理如下右图所示。
,原理如下右图所示。


①已知 中
中 为
为 价,则空心球催化剂技术中获得的
价,则空心球催化剂技术中获得的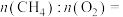
___________ 。
②写出步骤ii的化学方程式并用单线桥表示出电子转移的方向和数目___________ 。
③若不考虑过程中原料损失,则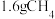 通过两步法最多可制得
通过两步法最多可制得 的物质的量为
的物质的量为___________ 。
(1)自然界中
 主要循环方式如图所示,其中属于“二氧化碳的捕捉与封存”的除了“海水吸收”外,还有
主要循环方式如图所示,其中属于“二氧化碳的捕捉与封存”的除了“海水吸收”外,还有
(2)科学家设计出烧碱溶液捕捉
 法,原理如图所示
法,原理如图所示
①该过程中能实现再生的反应为
 和
和②若喷洒完
 的
的 溶液后,测得吸收液中的
溶液后,测得吸收液中的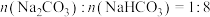 ,则被吸收的
,则被吸收的 在标况下的体积为
在标况下的体积为
③下列溶液中,也能用作“捕捉”二氧化碳试剂的是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.稀硫酸
溶液 D.稀硫酸(3)
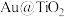 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如下左图所示。制得的甲烷
封存和能量储存双重效果,其原理如下左图所示。制得的甲烷 通过两步法可制取
通过两步法可制取 ,原理如下右图所示。
,原理如下右图所示。

①已知
 中
中 为
为 价,则空心球催化剂技术中获得的
价,则空心球催化剂技术中获得的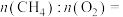
②写出步骤ii的化学方程式并用单线桥表示出电子转移的方向和数目
③若不考虑过程中原料损失,则
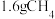 通过两步法最多可制得
通过两步法最多可制得 的物质的量为
的物质的量为
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:

已知NaHCO3在低温下溶解度较小。
(1)反应Ⅰ的化学方程式为_______ 。
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中 Na2CO3的含量。
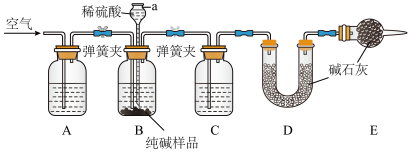
(2)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若_______ ,说明装置不漏气。
(3)装置A中的试剂为_______ ,装置C中的试剂为_______ 。装置E的作用是_______ 。
(4)实验前称取28.80 g样品,实验后测得D装置增重8.80 g,则样品中Na2CO3的质量分数为_______ (保留一位小数);若缺少E装置,会使测定结果_______ (填“偏高”或“偏低”)。

已知NaHCO3在低温下溶解度较小。
(1)反应Ⅰ的化学方程式为
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中 Na2CO3的含量。

(2)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若
(3)装置A中的试剂为
(4)实验前称取28.80 g样品,实验后测得D装置增重8.80 g,则样品中Na2CO3的质量分数为
您最近一年使用:0次
2023-11-26更新
|
221次组卷
|
3卷引用:山西省实验中学2023-2024学年高一上学期期中考试化学试题



