1 . 下图所示实验方案无法达到预期实验目的的是
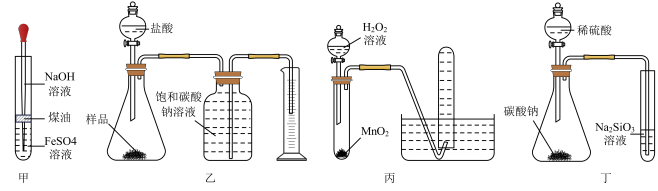

A.用图甲制备 |
| B.用图乙测定纯碱样品中碳酸钠的质量分数(杂质与酸不反应) |
C.用图丙制备并收集 |
| D.用图丁比较S、C、Si的非金属性强弱 |
您最近一年使用:0次
名校
解题方法
2 . 下列关于 和
和 的叙述中,不正确的是
的叙述中,不正确的是
 和
和 的叙述中,不正确的是
的叙述中,不正确的是A. 是白色粉末, 是白色粉末, 是细小的白色晶体 是细小的白色晶体 |
B.分别向 和 和 的固体中加入少量水,均伴随着放热现象 的固体中加入少量水,均伴随着放热现象 |
C.物质的量相等的 和 和 分别与足量盐酸反应,所消耗盐酸的物质的量相同 分别与足量盐酸反应,所消耗盐酸的物质的量相同 |
D.取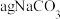 和 和 的固体混合物充分加热,质量减少 的固体混合物充分加热,质量减少 ,可测出 ,可测出 的质量分数 的质量分数 |
您最近一年使用:0次
3 . 为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置如图,下列说法正确的是
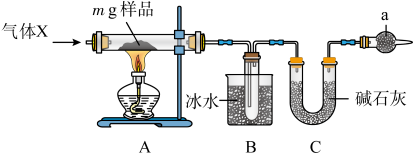

| A.a装置内应装碱石灰,目的是为了尾气处理 |
| B.装置B、C之间缺少CO2的干燥装置 |
| C.没有a装置会导致所测碳酸钠的质量分数偏高 |
| D.X气体可以是空气,反应前和反应后均需通一段时间空气 |
您最近一年使用:0次
名校
解题方法
4 . Ⅰ.Na2CO3和NaHCO3是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
(1)热稳定性差异。乙组设计如图装置进行实验(加热及夹持装置省略)。

将分别装有Na2CO3和NaHCO3的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象为:___________ ,试管b中发生反应的化学方程式为___________ 。
(2)取一定质量的Na2CO3和NaHCO3混合物灼烧至恒重,冷却至室温,共收集到4.4g气体。加热后剩余的固体物质与足量盐酸反应,共收集到8.8g气体。请分别求出原固体混合物中Na2CO3和NaHCO3的质量分别为___________ g、___________ g。
(3)有同学提出:取一定质量的Na2CO3和NaHCO3混合物灼烧至恒重,将产生的气体通入足量Ba(OH)2溶液中,通过生成的沉淀质量计算碳酸钠的含量,发现测量值明显偏大,可能的原因是___________ 。
Ⅱ.我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献,下图为联合制碱法的主要过程(部分物质已略去)。

已知:i.NH3极易溶于水并生成碱,与酸反应生成盐,如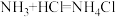 。
。
ii.有关物质的溶解度(20℃)
(4)沉淀池中主要沉淀物___________ (化学式),发生反应的化学方程式为___________ 。
(1)热稳定性差异。乙组设计如图装置进行实验(加热及夹持装置省略)。

将分别装有Na2CO3和NaHCO3的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象为:
(2)取一定质量的Na2CO3和NaHCO3混合物灼烧至恒重,冷却至室温,共收集到4.4g气体。加热后剩余的固体物质与足量盐酸反应,共收集到8.8g气体。请分别求出原固体混合物中Na2CO3和NaHCO3的质量分别为
(3)有同学提出:取一定质量的Na2CO3和NaHCO3混合物灼烧至恒重,将产生的气体通入足量Ba(OH)2溶液中,通过生成的沉淀质量计算碳酸钠的含量,发现测量值明显偏大,可能的原因是
Ⅱ.我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献,下图为联合制碱法的主要过程(部分物质已略去)。

已知:i.NH3极易溶于水并生成碱,与酸反应生成盐,如
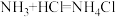 。
。ii.有关物质的溶解度(20℃)
| 物质 | NaCl |  |  |  |
| 溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
(4)沉淀池中主要沉淀物
您最近一年使用:0次
2023-12-26更新
|
52次组卷
|
2卷引用:四川省遂宁中学校2023-2024学年高一上学期期中(半期)考试化学试题
5 . 我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。联合制碱法的工艺流程简化如下:

I.资料1:反应I中的化学方程式为:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓
资料2:20℃时,溶解度小于0.0lg的物质属于难溶物;20℃时BaSO4溶解度为 g。
g。
资料3:表1有关物质的溶解度(20℃)
(1)操作I的名称为_______ ,反应II的化学方程式为_______ 。
(2)相同温度下,用pH试纸测量同等浓度的Na2CO3与NaHCO3溶液pH,_______ 溶液碱性强。
(3)离子反应: ,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是
,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是_______ 。
II.泡腾片是一种医药片剂,适用于儿童、老年人以及吞服药丸困难的患者。泡腾片放入水中,在崩解剂的作用下,即刻产生大量气泡(二氧化碳),使片剂迅速崩解形成水溶液,崩解剂主要由NaHCO3固体与柠檬酸固体组成。
(4)下列说法正确的是_______ (填字母)。
A.NaHCO3固体与柠檬酸固体不反应
B.柠檬酸在水中电离产生H+与NaHCO3反应
C.Na2CO3比NaHCO3稳定,受热不易分解
(5)某NaHCO3样品中含NaCl杂质,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中NaHCO3的质量分数是_______ 。

I.资料1:反应I中的化学方程式为:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓
资料2:20℃时,溶解度小于0.0lg的物质属于难溶物;20℃时BaSO4溶解度为
 g。
g。资料3:表1有关物质的溶解度(20℃)
| 物质 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
(1)操作I的名称为
(2)相同温度下,用pH试纸测量同等浓度的Na2CO3与NaHCO3溶液pH,
(3)离子反应:
 ,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是
,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是II.泡腾片是一种医药片剂,适用于儿童、老年人以及吞服药丸困难的患者。泡腾片放入水中,在崩解剂的作用下,即刻产生大量气泡(二氧化碳),使片剂迅速崩解形成水溶液,崩解剂主要由NaHCO3固体与柠檬酸固体组成。
(4)下列说法正确的是
A.NaHCO3固体与柠檬酸固体不反应
B.柠檬酸在水中电离产生H+与NaHCO3反应
C.Na2CO3比NaHCO3稳定,受热不易分解
(5)某NaHCO3样品中含NaCl杂质,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中NaHCO3的质量分数是
您最近一年使用:0次
解题方法
6 . 下列关于钠及其化合物的说法正确的是
| A.将Na久置于空气中,最终得到的产物为NaOH |
B.将 投入适量紫色石蕊溶液中,溶液褪色 投入适量紫色石蕊溶液中,溶液褪色 |
C. 和 和 组成元素相同,化学性质相似 组成元素相同,化学性质相似 |
D.质量分数相同的 溶液和 溶液和 ,溶液的碱性: ,溶液的碱性: |
您最近一年使用:0次
名校
解题方法
7 . Ⅰ.探究NaHCO3和Na2CO3的热稳定性。

观察到的实验现象如下表所示:
根据上述实验现象,回答下列问题:
(1)加热Na2CO3时,装置C中产生气泡的原因是_______ 。
(2)实验结论是_______ 。
(3)加热NaHCO3发生反应的化学方程式为_______ 。
Ⅱ.为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置示意图如下,请回答:

(4)仪器a的名称是_______ 。
(5)装置B中冰水的作用是_______ 。
(6)该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸钠的质量分数偏高的是_______。

观察到的实验现象如下表所示:
| 物质 | 装置B中现象 | 装置C中现象 |
| Na2CO3 | 无明显变化 | 开始断断续续产生气泡,一会儿后,没有气泡,溶液保持澄清 |
| NaHCO3 | 白色粉末变蓝色 | 开始断断续续产生气泡,一会儿后,产生连续气泡,溶液变浑浊 |
(1)加热Na2CO3时,装置C中产生气泡的原因是
(2)实验结论是
(3)加热NaHCO3发生反应的化学方程式为
Ⅱ.为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置示意图如下,请回答:

(4)仪器a的名称是
(5)装置B中冰水的作用是
(6)该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸钠的质量分数偏高的是_______。
| A.样品分解不完全 |
| B.装置B、C之间缺少CO2的干燥装置 |
| C.产生 CO2气体的速率太快,没有被碱石灰完全吸收 |
| D.反应完全后停止加热,通入过量的空气 |
您最近一年使用:0次
名校
解题方法
8 . Na2CO3和NaHCO3在日常生产生活中有着广泛应用。
(1)探究两者热稳定性的“套管实验”的实验装置如图所示:
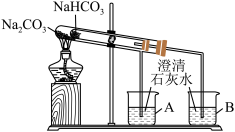
①写出实验过程中试管中发生反应的化学方程式:_______ 。
②证明热稳定性的实验装置中,能否将NaHCO3、Na2CO3的位置互换_______ (填“能”或“不能”)。
(2)能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是_______ 。
A.将Na2CO3和NaHCO3配制成同浓度的溶液,用pH试纸测定pH值并做比较
B.分别在这两种物质的溶液中,滴加同浓度的稀盐酸
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
(3)利用图所示装置来测定纯碱样品中Na2CO3的质量分数(铁架台、铁夹等在图中均已略去)。实验步骤如图:

a.按图连接装置,并检查气密性;
b.准确称得盛有碱石灰的干燥管D的质量为83.4g;
c.准确称得10g纯碱样品放入容器II中;
d.打开分液漏斗I的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
e.打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6g。
①装置A中试剂X应选用_______ ,通入空气的目的是_______ 。
②E装置的作用是_______ 。
③根据实验中测得的有关数据,计算纯碱样品中Na2CO3的质量分数为_______ 。
(1)探究两者热稳定性的“套管实验”的实验装置如图所示:

①写出实验过程中试管中发生反应的化学方程式:
②证明热稳定性的实验装置中,能否将NaHCO3、Na2CO3的位置互换
(2)能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.将Na2CO3和NaHCO3配制成同浓度的溶液,用pH试纸测定pH值并做比较
B.分别在这两种物质的溶液中,滴加同浓度的稀盐酸
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
(3)利用图所示装置来测定纯碱样品中Na2CO3的质量分数(铁架台、铁夹等在图中均已略去)。实验步骤如图:

a.按图连接装置,并检查气密性;
b.准确称得盛有碱石灰的干燥管D的质量为83.4g;
c.准确称得10g纯碱样品放入容器II中;
d.打开分液漏斗I的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
e.打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6g。
①装置A中试剂X应选用
②E装置的作用是
③根据实验中测得的有关数据,计算纯碱样品中Na2CO3的质量分数为
您最近一年使用:0次
名校
9 . 课外兴趣小组的同学探究 和
和 性质。
性质。
【实验一】
(1)室温下, 的溶解度大于
的溶解度大于 的实验证据是
的实验证据是_________ 。
(2)该实验_________ (填能或不能)说明 溶液的碱性强于
溶液的碱性强于 溶液,理由是
溶液,理由是_________ 。
【实验二】资料: 越小,
越小,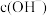 越小,溶液碱性越弱。
越小,溶液碱性越弱。
(3)实验二中,向澄清石灰水滴加 溶液,
溶液, 未参与该反应的实验证据是
未参与该反应的实验证据是_________ 。
(4)实验二中,滴加 溶液的pH变化与滴加
溶液的pH变化与滴加 溶液的有明显差异,结合离子方程式说明原因
溶液的有明显差异,结合离子方程式说明原因_________ 。
(5)为测定 和
和 混合物中
混合物中 的质量分数,同学们取ag混合物充分加热,质量减少bg,则混合物中
的质量分数,同学们取ag混合物充分加热,质量减少bg,则混合物中 的质量分数是
的质量分数是_________ (用含a、b的代数式表示)。
 和
和 性质。
性质。【实验一】
| 序号 | 操作 |  |  |
| ① | 在两支试管中分别加入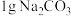 、 、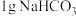 ,再加入 ,再加入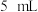 水,充分振荡;将两支温度计分别插入试管中 水,充分振荡;将两支温度计分别插入试管中 | 温度由 变为 变为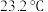 ;放置到室温时,试管内无固体 ;放置到室温时,试管内无固体 | 温度由 变为 变为 ;放置到室温时,试管内有少量固体残留 ;放置到室温时,试管内有少量固体残留 |
| ② | 室温时,分别向①所得溶液中滴入2滴酚酞溶液 | 溶液变红 | 溶液微红 |
 的溶解度大于
的溶解度大于 的实验证据是
的实验证据是(2)该实验
 溶液的碱性强于
溶液的碱性强于 溶液,理由是
溶液,理由是【实验二】资料:
 越小,
越小,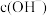 越小,溶液碱性越弱。
越小,溶液碱性越弱。| 实验操作 | 实验数据 |
测量下述实验过程的 变化 变化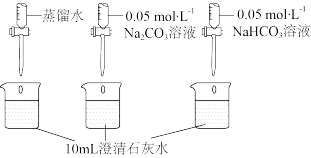 | 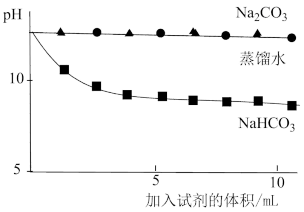 |
 溶液,
溶液, 未参与该反应的实验证据是
未参与该反应的实验证据是(4)实验二中,滴加
 溶液的pH变化与滴加
溶液的pH变化与滴加 溶液的有明显差异,结合离子方程式说明原因
溶液的有明显差异,结合离子方程式说明原因(5)为测定
 和
和 混合物中
混合物中 的质量分数,同学们取ag混合物充分加热,质量减少bg,则混合物中
的质量分数,同学们取ag混合物充分加热,质量减少bg,则混合物中 的质量分数是
的质量分数是
您最近一年使用:0次
解题方法
10 . 下列关于 和
和 的叙述中,不正确的是
的叙述中,不正确的是
 和
和 的叙述中,不正确的是
的叙述中,不正确的是A. 是白色粉末, 是白色粉末, 是细小的白色晶体 是细小的白色晶体 |
B.等质量的 和 和 与足量盐酸反应,相同条件下 与足量盐酸反应,相同条件下 产生的气体体积比较大 产生的气体体积比较大 |
C.分别向 和 和 的固体中加入少量水, 的固体中加入少量水, 伴有放热现象 伴有放热现象 |
D.取ag 和 和 的固体混合物充分加热,质量减少bg,可测定出 的固体混合物充分加热,质量减少bg,可测定出 的质量分数 的质量分数 |
您最近一年使用:0次



