名校
1 . 生活中处处有化学。下列生活中 及其化合物相关反应的离子方程式书写不正确的是
及其化合物相关反应的离子方程式书写不正确的是
 及其化合物相关反应的离子方程式书写不正确的是
及其化合物相关反应的离子方程式书写不正确的是A.胃舒平[主要成分为 ]治疗胃酸过多: ]治疗胃酸过多: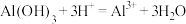 |
B.泡沫灭火器灭火原理: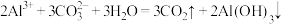 |
C.某主要成分为苛性钠、铝粉的管道疏通剂: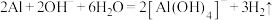 |
D.明矾净水原理: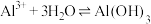 (胶体) (胶体)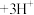 |
您最近一年使用:0次
2024-05-30更新
|
200次组卷
|
3卷引用:广东省部分学校2024届高三下学期5月份大联考化学试题
名校
解题方法
2 . Li2CO3可用于制备锂电池的正极材料LiCoO2,以某锂云母矿石(主要成分为Li2O,还有Al2O3、Fe2O3、MnO、MgF2等杂质)制备Li2CO3。
已知:①有关沉淀数据如下表(“完全沉淀”时金属离子浓度≤1.0×10-5mol·L-1)。
②部分物质的溶解度曲线见下图。
(1)酸浸,向锂云母矿石中加入50%硫酸,加热至90℃,装置如图所示。烧杯中试剂的作用是___________ 。___________ 。分两次调节pH的主要原因是___________ 。
(3)沉锂,将已经除杂的溶液蒸发浓缩,向浓缩后的滤液中加入稍过量饱和Na2CO3溶液,加热煮沸,趁热过滤,将滤渣洗涤烘干,得Li2CO3固体。浓缩液中离子浓度过大将在产品中引入___________ 杂质(填化学式)。
(4)Li2CO3和Co3O4混合后,在空气中高温加热可以制备锂电池的正极材料LiCoO2,写出反应方程式:___________ 。
(5)CoC2O4·2H2O热分解可制备Co3O4。请补充完整由含c(Co2+)=0.1mol·L-1的浸出液(含有杂质Al3+、Fe3+、Fe2+)制备纯净的CoC2O4·2H2O实验方案:___________ ,干燥,得到CoC2O4·2H2O晶体。(须使用的试剂:NaClO3,NaOH,AgNO3溶液,(NH4)2C2O4,蒸馏水)
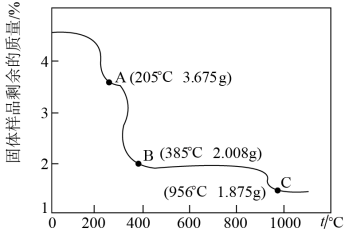
(6)为确定由CoC2O4·2H2O获得Co3O4的最佳煅烧温度,准确称取4.575g的CoC2O4·2H2O样品,在空气中加热,固体样品的剩余质量随温度的变化如图所示(已知385℃以上残留固体均为金属氧化物)经测定,205~385℃的煅烧过程中,产生的气体为CO2,计算AB段消耗O2在标准状况下的体积___________ 。(写出计算过程,结果保留2位有效数字)
已知:①有关沉淀数据如下表(“完全沉淀”时金属离子浓度≤1.0×10-5mol·L-1)。
| 沉淀 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Co(OH)2 | Mn(OH)2 | Mg(OH)2 |
| 恰好完全沉淀时pH | 5.2 | 8.8 | 3.2 | 9.4 | 9.8 | 11.1 |

(1)酸浸,向锂云母矿石中加入50%硫酸,加热至90℃,装置如图所示。烧杯中试剂的作用是

(3)沉锂,将已经除杂的溶液蒸发浓缩,向浓缩后的滤液中加入稍过量饱和Na2CO3溶液,加热煮沸,趁热过滤,将滤渣洗涤烘干,得Li2CO3固体。浓缩液中离子浓度过大将在产品中引入
(4)Li2CO3和Co3O4混合后,在空气中高温加热可以制备锂电池的正极材料LiCoO2,写出反应方程式:
(5)CoC2O4·2H2O热分解可制备Co3O4。请补充完整由含c(Co2+)=0.1mol·L-1的浸出液(含有杂质Al3+、Fe3+、Fe2+)制备纯净的CoC2O4·2H2O实验方案:
(6)为确定由CoC2O4·2H2O获得Co3O4的最佳煅烧温度,准确称取4.575g的CoC2O4·2H2O样品,在空气中加热,固体样品的剩余质量随温度的变化如图所示(已知385℃以上残留固体均为金属氧化物)经测定,205~385℃的煅烧过程中,产生的气体为CO2,计算AB段消耗O2在标准状况下的体积
您最近一年使用:0次
3 . “价类”二维图体现了元素的分类观、转化观,下图是 及其部分化合物的“价类”二维图。下列说法错误的是
及其部分化合物的“价类”二维图。下列说法错误的是
 及其部分化合物的“价类”二维图。下列说法错误的是
及其部分化合物的“价类”二维图。下列说法错误的是
| A.反应③④⑤⑥⑦均属于复分解反应 | B.反应①⑥所加试剂可能相同 |
C.物质的类别处“ ”代表偏铝酸盐 ”代表偏铝酸盐 | D.反应④⑤均可以通过加入盐酸实现转化 |
您最近一年使用:0次
名校
解题方法
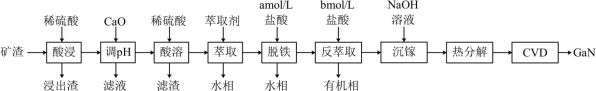
4 . 氮化镓(GaN)具有优异的光电性能。一种利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4、SiO2]制备GaN的工艺流程如下:
②常温下,Ksp[Zn(OH)2]=10-16.6,Ksp[Ga(OH)3]=10-35.1,Ksp[Fe(OH)3]=10-38.5。
③Ga3+、Fe3+在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
回答下列问题:
(1)“酸浸”时能提高反应速率的措施有____________ (答1条即可)
(2)“酸浸”所得浸出液中Ga3+、Zn2+浓度分别为0.21g/L、65g/L。常温下,为尽可能多地提取Ga3+并确保不混入Zn(OH)2,用CaO“调pH”时须不能大于___________ (假设调pH时溶液体积不变)
(3)“脱铁”和“反萃取”时,所用盐酸的浓度a=________ mol/L,b=______ mol/L(选填上表中盐酸的浓度)。
(4)“沉镓”时,若加入NaOH的量过多,会导致Ga3+的沉淀率降低,原因是___________ (用离子方程式表示)。
(5)利用CVD(化学气相沉积)技术,将热分解得到的Ga2O3与NH3在高温下反应可制得GaN,同时生成另一种产物,该反应化学方程式为_______________ 。
(6)GaN晶体的一种立方晶胞如图下所示。________ 种空间运动状态。
②该晶胞边长为anm,GaN的相对分子质量为Mr,则该晶体密度为_________ g/cm3(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
②常温下,Ksp[Zn(OH)2]=10-16.6,Ksp[Ga(OH)3]=10-35.1,Ksp[Fe(OH)3]=10-38.5。
③Ga3+、Fe3+在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
| 盐酸浓度/mol/L | 反萃取率/% | |
| Ga3+ | Fe3+ | |
| 2 | 86.9 | 9.4 |
| 4 | 69.1 | 52.1 |
| 6 | 17.5 | 71.3 |
(1)“酸浸”时能提高反应速率的措施有
(2)“酸浸”所得浸出液中Ga3+、Zn2+浓度分别为0.21g/L、65g/L。常温下,为尽可能多地提取Ga3+并确保不混入Zn(OH)2,用CaO“调pH”时须不能大于
(3)“脱铁”和“反萃取”时,所用盐酸的浓度a=
(4)“沉镓”时,若加入NaOH的量过多,会导致Ga3+的沉淀率降低,原因是
(5)利用CVD(化学气相沉积)技术,将热分解得到的Ga2O3与NH3在高温下反应可制得GaN,同时生成另一种产物,该反应化学方程式为
(6)GaN晶体的一种立方晶胞如图下所示。

②该晶胞边长为anm,GaN的相对分子质量为Mr,则该晶体密度为
 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解题方法
5 . 下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 用 | 氧化性: |
B |
|
|
C | 液氨可用作制冷剂 | 氨气极易溶于水 |
D | Na着火不能用水扑灭 | Na可与水反应产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 化学与生活密切相关。下列生活场景中有关化学知识的说法错误的是
选项 | 生活中的应用 | 化学知识 |
A |
|
|
B |
|
|
C |
|
|
D | 小苏打用制作食用碱 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 一定条件下,下列各项中的物质按如图所示的箭头不能实现一步转化的是
甲 丙
丙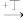 乙
乙
甲
 丙
丙 乙
乙| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | NaOH溶液 | CO2 | Na2CO3溶液 | NaHSO4溶液 |
| B | SiO2 | C | CO2 | Fe |
| C | H2S | SO2 | S | O2 |
| D | 氨水 | AlCl3 | Al(OH)3 | 盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 聚合硫酸铝铁(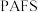 )是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为
)是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为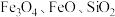 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为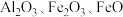 等),经过一系列的反应制得,具体流程如下:
等),经过一系列的反应制得,具体流程如下:___________ (填序号)。
A.降低温度 B.烧渣粉碎 C.适当提高硫酸浓度 D.加水稀释
“酸溶”后得到的溶液中,主要存在的金属阳离子有___________ (填化学符号)。
(2)检验“氧化”后溶液中金属阳离子的方法是___________ 。
(3)实验测得“氧化”过程中温度过高氧化效率会下降,原因可能是___________ 。
(4)“酸溶”过程中发生反应的离子方程式为___________ 。
(5)滤渣Ⅱ中可以循环利用的物质是___________ (填化学式)。
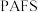 )是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为
)是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为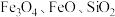 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为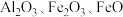 等),经过一系列的反应制得,具体流程如下:
等),经过一系列的反应制得,具体流程如下: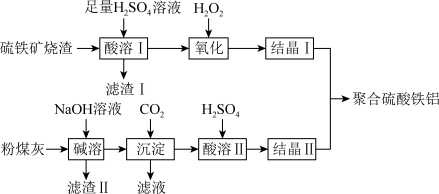
A.降低温度 B.烧渣粉碎 C.适当提高硫酸浓度 D.加水稀释
“酸溶”后得到的溶液中,主要存在的金属阳离子有
(2)检验“氧化”后溶液中金属阳离子的方法是
(3)实验测得“氧化”过程中温度过高氧化效率会下降,原因可能是
(4)“酸溶”过程中发生反应的离子方程式为
(5)滤渣Ⅱ中可以循环利用的物质是
您最近一年使用:0次
2024-04-24更新
|
195次组卷
|
2卷引用:江苏省盐城市五校联考2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
9 . 絮凝剂聚合氯化铝{ ,
, }广泛用于废水处理。由偏铝酸钙
}广泛用于废水处理。由偏铝酸钙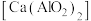 制备聚合氯化铝的一种工艺流程如下:
制备聚合氯化铝的一种工艺流程如下: 的絮凝效果可用盐基度(盐基度
的絮凝效果可用盐基度(盐基度 )衡量,当盐基度为0.60~0.85时,絮凝效果较好。
)衡量,当盐基度为0.60~0.85时,絮凝效果较好。
(1)“碱溶”时,化学反应方程式为___________ 。
(2)若滤液浓度较大,则通入过量 不利于减少
不利于减少 滤饼中的杂质,其原因是
滤饼中的杂质,其原因是___________ 。
(3)“酸化”时的装置如图所示,仪器A的名称为___________ ,若要使产品盐基度为 ,则
,则
___________ ;先将 滤饼分散在蒸馏水中,再向其中滴加一定量的盐酸,与直接向滤饼中加盐酸相比,优点是
滤饼分散在蒸馏水中,再向其中滴加一定量的盐酸,与直接向滤饼中加盐酸相比,优点是____________ 。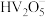 、
、 的碱性废水制取聚合氯化铝的实验方案:取适量废水,
的碱性废水制取聚合氯化铝的实验方案:取适量废水,___________ ,向其中滴加一定量的盐酸,得到聚合氯化铝。(实验中须使用的试剂有: 、5%的双氧水、蒸馏水、
、5%的双氧水、蒸馏水、 溶液)
溶液)
 ,
, }广泛用于废水处理。由偏铝酸钙
}广泛用于废水处理。由偏铝酸钙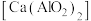 制备聚合氯化铝的一种工艺流程如下:
制备聚合氯化铝的一种工艺流程如下: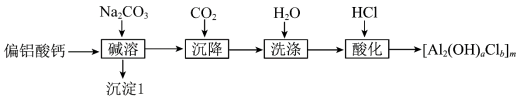
 的絮凝效果可用盐基度(盐基度
的絮凝效果可用盐基度(盐基度 )衡量,当盐基度为0.60~0.85时,絮凝效果较好。
)衡量,当盐基度为0.60~0.85时,絮凝效果较好。(1)“碱溶”时,化学反应方程式为
(2)若滤液浓度较大,则通入过量
 不利于减少
不利于减少 滤饼中的杂质,其原因是
滤饼中的杂质,其原因是(3)“酸化”时的装置如图所示,仪器A的名称为
 ,则
,则
 滤饼分散在蒸馏水中,再向其中滴加一定量的盐酸,与直接向滤饼中加盐酸相比,优点是
滤饼分散在蒸馏水中,再向其中滴加一定量的盐酸,与直接向滤饼中加盐酸相比,优点是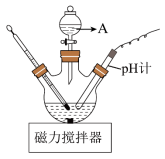
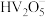 、
、 的碱性废水制取聚合氯化铝的实验方案:取适量废水,
的碱性废水制取聚合氯化铝的实验方案:取适量废水, 、5%的双氧水、蒸馏水、
、5%的双氧水、蒸馏水、 溶液)
溶液)| 化合价 |  |  |
| +4价V | 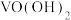 沉淀 沉淀 | 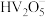 |
| +5价V |  |  |
| +3价Al |  沉淀 沉淀 |  |
您最近一年使用:0次
名校
10 . 下列叙述不正确的是
A.在稀硫酸中加入铜粉,铜粉不溶解;再加入 固体,铜粉不溶解 固体,铜粉不溶解 |
B.将 通入 通入 溶液中至饱和,无沉淀产生;再通入 溶液中至饱和,无沉淀产生;再通入 ,产生沉淀 ,产生沉淀 |
C.向 溶液中滴加氨水,产生白色沉淀;再加入 溶液中滴加氨水,产生白色沉淀;再加入 溶液,沉淀消失 溶液,沉淀消失 |
D.检验某白色固体是否为铵盐的方法:取少量固体于试管中,加浓 溶液,加热,将湿润的红色石蕊试纸放在试管口 溶液,加热,将湿润的红色石蕊试纸放在试管口 |
您最近一年使用:0次

 溶液刻蚀铜质电路板
溶液刻蚀铜质电路板
 可用于治疗胃酸过多
可用于治疗胃酸过多
 用于自来水的杀菌
用于自来水的杀菌 水溶液显碱性
水溶液显碱性

