名校
解题方法
1 . 物质的性质决定着反应的多样性。对于 与
与 的反应,Z同学就有着不同想法。为此,他设计了以下实验:
的反应,Z同学就有着不同想法。为此,他设计了以下实验:
(1)研究 溶液与KI溶液反应
溶液与KI溶液反应
实验Ⅰ:向盛有1 mL 1 mol/L 溶液的试管中加入1 mL 1 mol/L KI溶液,振荡试管,静置。取上层清液,向其中加入
溶液的试管中加入1 mL 1 mol/L KI溶液,振荡试管,静置。取上层清液,向其中加入___________ ,溶液无明显变化。
结论Ⅰ:二者混合只发生沉淀反应,无明显氧化还原反应。
(2)探究 的氧化性强弱
的氧化性强弱
实验Ⅱ:将打磨光亮的铁丝伸入1 mol/L 溶液中,一段时间后将铁丝取出。除去溶液中剩余的
溶液中,一段时间后将铁丝取出。除去溶液中剩余的 ,取1~2 mL溶液于试管中,加入试剂X,振荡,溶液变为红色,证明溶液中存在
,取1~2 mL溶液于试管中,加入试剂X,振荡,溶液变为红色,证明溶液中存在 。试剂X应为
。试剂X应为___________ 。
结论Ⅱ:___________ 。
已知 氧化性大于
氧化性大于 ,则证明
,则证明 可与
可与 发生氧化还原反应。
发生氧化还原反应。
(3)①X同学测得常温下该 溶液的pH为5.5,于是对结论Ⅱ提出质疑,认为可能是酸性条件下
溶液的pH为5.5,于是对结论Ⅱ提出质疑,认为可能是酸性条件下 体现了氧化性。
体现了氧化性。
为了验证其质疑是否正确,他设计了一个对比实验:将打磨光亮的铁丝伸入___________ 溶液中,一段时间后将铁丝取出。取1~2 mL溶液于试管中,加入试剂X,观察溶液是否呈红色。
②同时,X同学考虑到 溶液与KI溶液反应体系中存在竞争反应。所以,他设计了以下实验来探究
溶液与KI溶液反应体系中存在竞争反应。所以,他设计了以下实验来探究 与
与 的氧化还原反应
的氧化还原反应

根据此装置,盐桥中可选择___________ 作为电解质。
a.KCl b. c.
c.
在此实验中,可通过___________ (填实验现象)证明 与
与 一定发生了氧化还原反应。
一定发生了氧化还原反应。
(4)X同学查阅资料,得知常温下,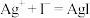
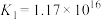 、
、

 ,试从速率和平衡两个方面解释
,试从速率和平衡两个方面解释 溶液与KI溶液混合只发生沉淀反应而无明显氧化还原反应的可能原因:
溶液与KI溶液混合只发生沉淀反应而无明显氧化还原反应的可能原因:___________ 。
 与
与 的反应,Z同学就有着不同想法。为此,他设计了以下实验:
的反应,Z同学就有着不同想法。为此,他设计了以下实验:(1)研究
 溶液与KI溶液反应
溶液与KI溶液反应实验Ⅰ:向盛有1 mL 1 mol/L
 溶液的试管中加入1 mL 1 mol/L KI溶液,振荡试管,静置。取上层清液,向其中加入
溶液的试管中加入1 mL 1 mol/L KI溶液,振荡试管,静置。取上层清液,向其中加入结论Ⅰ:二者混合只发生沉淀反应,无明显氧化还原反应。
(2)探究
 的氧化性强弱
的氧化性强弱实验Ⅱ:将打磨光亮的铁丝伸入1 mol/L
 溶液中,一段时间后将铁丝取出。除去溶液中剩余的
溶液中,一段时间后将铁丝取出。除去溶液中剩余的 ,取1~2 mL溶液于试管中,加入试剂X,振荡,溶液变为红色,证明溶液中存在
,取1~2 mL溶液于试管中,加入试剂X,振荡,溶液变为红色,证明溶液中存在 。试剂X应为
。试剂X应为结论Ⅱ:
已知
 氧化性大于
氧化性大于 ,则证明
,则证明 可与
可与 发生氧化还原反应。
发生氧化还原反应。(3)①X同学测得常温下该
 溶液的pH为5.5,于是对结论Ⅱ提出质疑,认为可能是酸性条件下
溶液的pH为5.5,于是对结论Ⅱ提出质疑,认为可能是酸性条件下 体现了氧化性。
体现了氧化性。为了验证其质疑是否正确,他设计了一个对比实验:将打磨光亮的铁丝伸入
②同时,X同学考虑到
 溶液与KI溶液反应体系中存在竞争反应。所以,他设计了以下实验来探究
溶液与KI溶液反应体系中存在竞争反应。所以,他设计了以下实验来探究 与
与 的氧化还原反应
的氧化还原反应
根据此装置,盐桥中可选择
a.KCl b.
 c.
c.
在此实验中,可通过
 与
与 一定发生了氧化还原反应。
一定发生了氧化还原反应。(4)X同学查阅资料,得知常温下,
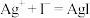
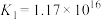 、
、

 ,试从速率和平衡两个方面解释
,试从速率和平衡两个方面解释 溶液与KI溶液混合只发生沉淀反应而无明显氧化还原反应的可能原因:
溶液与KI溶液混合只发生沉淀反应而无明显氧化还原反应的可能原因:
您最近一年使用:0次
解题方法
2 . 某化学小组探究酸性条件下 、
、 、
、 三种微粒的氧化性强弱,设计如下实验
三种微粒的氧化性强弱,设计如下实验 夹持仪器已略去;装置的气密性已检验;忽略氧气对反应的影响
夹持仪器已略去;装置的气密性已检验;忽略氧气对反应的影响 :
:

实验记录如下:
请回答下列问题:
(1)实验室制取 的化学方程式为
的化学方程式为________  。
。
(2)配制 溶液时,
溶液时,________ ,再加水稀释到所需浓度。
(3)资料表明, 能与
能与 结合形成深红棕色物质
结合形成深红棕色物质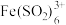 ,反应方程式为:
,反应方程式为: 。请用化学平衡移动原理解释实验Ⅰ中溶液颜色变化的原因
。请用化学平衡移动原理解释实验Ⅰ中溶液颜色变化的原因________ 。
(4)实验Ⅱ中发生反应的离子方程式是________ 。
(5)实验Ⅲ中,浅绿色溶液变为黄色的原因是________  用离子方程式表示
用离子方程式表示 。
。
(6)实验Ⅳ中液面上方有少量红棕色气体生成,发生反应的化学方程式是________ 。
(7)综合上述实验得出的结论是:在酸性条件下,氧化性强弱是: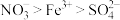 。
。________ ,说明氧化性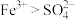 (填实验序号,下同);
(填实验序号,下同);________ ,说明氧化性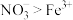 。
。
 、
、 、
、 三种微粒的氧化性强弱,设计如下实验
三种微粒的氧化性强弱,设计如下实验 夹持仪器已略去;装置的气密性已检验;忽略氧气对反应的影响
夹持仪器已略去;装置的气密性已检验;忽略氧气对反应的影响 :
:
实验记录如下:
实验序号 | 实验操作 | 实验现象 |
Ⅰ | 向A装置中通入段时间的 | A中黄色溶液迅速变成深红棕色,最终变为浅绿色 |
Ⅱ | 取出少量A装置中的溶液,先加入KSCN溶液,再加入 | 加入KSCN溶液后溶液不变色,再加入 |
Ⅲ | 打开活塞a,将过量稀 | A中浅绿色溶液最终变为黄色 |
Ⅳ | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中注入空气 | 溶液变为红色;液面上方有少量红棕色气体生成 |
请回答下列问题:
(1)实验室制取
 的化学方程式为
的化学方程式为 。
。(2)配制
 溶液时,
溶液时,(3)资料表明,
 能与
能与 结合形成深红棕色物质
结合形成深红棕色物质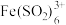 ,反应方程式为:
,反应方程式为: 。请用化学平衡移动原理解释实验Ⅰ中溶液颜色变化的原因
。请用化学平衡移动原理解释实验Ⅰ中溶液颜色变化的原因(4)实验Ⅱ中发生反应的离子方程式是
(5)实验Ⅲ中,浅绿色溶液变为黄色的原因是
 用离子方程式表示
用离子方程式表示 。
。(6)实验Ⅳ中液面上方有少量红棕色气体生成,发生反应的化学方程式是
(7)综合上述实验得出的结论是:在酸性条件下,氧化性强弱是:
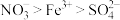 。
。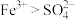 (填实验序号,下同);
(填实验序号,下同);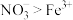 。
。
您最近一年使用:0次
3 . 绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得到各种铁的氧化物和硫的氧化物。已知SO3是一种无色晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红等。回答下列问题:
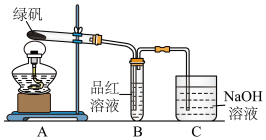
(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是____________ ,甲组由此得出绿矾的分解产物中含有SO2。装置C的作用是______________ 。
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中__________ (填字母)。
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解所得气态产物的装置:

①丙组同学的实验装置中,依次连接的合理顺序为___________ 。
②能证明绿矾分解产物中有O2的检验方法是____________ 。
(4)为证明绿矾分解产物中含有三价铁的操作及现象________ 。
(5)请用离子方程式表示下列化学反应
①向碳酸氢钠溶液中滴入三氯化铁溶液:_______
②硫酸亚铁溶液中逐滴加入酸性高锰酸钾溶液:_______

(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解所得气态产物的装置:

①丙组同学的实验装置中,依次连接的合理顺序为
②能证明绿矾分解产物中有O2的检验方法是
(4)为证明绿矾分解产物中含有三价铁的操作及现象
(5)请用离子方程式表示下列化学反应
①向碳酸氢钠溶液中滴入三氯化铁溶液:
②硫酸亚铁溶液中逐滴加入酸性高锰酸钾溶液:
您最近一年使用:0次
解题方法
4 . 某化学兴趣小组利用硫酸铁溶液与铜粉反应,又向反应后溶液中加入KSCN溶液以检验Fe3+是否有剩余,实验记录如下;
(1)写出实验1中第i步的离子方程式_______________ 。甲同学猜想第ii步出现的异常现象是由于溶液中的Cu2+干扰了检验Fe3+的现象。查阅相关资料如下
①2Cu2++4SCN- 2CuSCN↓(白色)+(SCN)2(黄色)
2CuSCN↓(白色)+(SCN)2(黄色)
②硫氰[(SCN)2]:是一种拟卤素,性质与卤素单质相似,其氧化性介于Br2和I2之间。
该同学又通过如下实验验证猜想
(2)经检测,实验2反应后的溶液pH值减小,可能的原因是___________________________________________ 。
(3)根据实验2、3的实验现象,甲同学推断实验3中溶液变红是由于Fe2+被(SCN)2氧化,写出溶液变红的离子方程式_______________________ 。继续将实验2中的浊液进一步处理,验证了这一结论的可能性。

补充实验4的目的是排除了溶液存在Cu2+的可能,对应的现象是____________________________________________ 。
(4)乙同学同时认为,根据氧化还原反应原理,在此条件下,Cu2+也能氧化Fe2+,他的判断依据是_______ 。
(5)为排除干扰,小组同学重新设计如下装置。
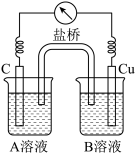
①A溶液为____________________________ 。
②“电流表指针偏转,说明Cu与Fe3+发生了反应”,你认为这种说法是否合理?__________________ (填合理或不合理),原因是__________________________________________ 。
③验证Fe3+是否参与反应的操作是________________________________________ 。
| 实验编号 | 操作 | 现象 |
| 实验1 |  | i.加入Cu粉后充分振荡,溶液逐渐变蓝; ii.取少量i中清液于试管中,滴加2滴 0.2mol/LKSCN溶液,溶液变为红色,但振荡后红色迅速褪去并有白色沉淀生成。 |
(1)写出实验1中第i步的离子方程式
①2Cu2++4SCN-
 2CuSCN↓(白色)+(SCN)2(黄色)
2CuSCN↓(白色)+(SCN)2(黄色)②硫氰[(SCN)2]:是一种拟卤素,性质与卤素单质相似,其氧化性介于Br2和I2之间。
该同学又通过如下实验验证猜想
| 实验编号 | 操作 | 现象 |
| 实验2 |  | 溶液呈绿色,一段时间后后开始出现白色沉淀,上层溶液变为黄色 |
| 实验3 | 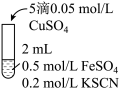 | 无色溶液立即变红,同时生成白色沉淀。 |
(2)经检测,实验2反应后的溶液pH值减小,可能的原因是
(3)根据实验2、3的实验现象,甲同学推断实验3中溶液变红是由于Fe2+被(SCN)2氧化,写出溶液变红的离子方程式

补充实验4的目的是排除了溶液存在Cu2+的可能,对应的现象是
(4)乙同学同时认为,根据氧化还原反应原理,在此条件下,Cu2+也能氧化Fe2+,他的判断依据是
(5)为排除干扰,小组同学重新设计如下装置。

①A溶液为
②“电流表指针偏转,说明Cu与Fe3+发生了反应”,你认为这种说法是否合理?
③验证Fe3+是否参与反应的操作是
您最近一年使用:0次
2020-03-28更新
|
692次组卷
|
6卷引用:重庆市江津中学、实验中学等七校2020届高三下学期6月联考(三诊)理科综合化学试题
重庆市江津中学、实验中学等七校2020届高三下学期6月联考(三诊)理科综合化学试题北京市平谷区2020届高三第一次模拟考试化学试题北京市平谷区2020届高三3月质量监控(一模)化学试题(已下线)考点15 金属元素及其化合物-2020年高考化学命题预测与模拟试题分类精编(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编:科学探究(已下线)专题讲座(三)“铁三角”综合实验题解题策略(精练)——2021年高考化学一轮复习讲练测
名校
5 . 下列物质的性质与用途不具有对应关系是
| A.CO具有还原性,可用于冶炼铁 | B.KNO3具有氧化性,可用于制黑火药 |
| C.Na2CO3溶液显碱性,可用于除油污 | D.FeCl3溶液显酸性,可用于刻蚀电路板上的铜 |
您最近一年使用:0次
6 . 为了探究铁及其化合物的氧化性或还原性,某同学设计如下实验操作,对应的实验现象、实验结论及离子方程式均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 | 离子方程式 |
| A | 向 溶液中加入 溶液中加入 片 片 | 浅绿色溶液变为无色,溶液中有黑色固体生成 |  具有还原性 具有还原性 |  |
| B | 向 溶液中滴加新制氯水 溶液中滴加新制氯水 | 浅绿色溶液变为棕黄色 |  具有还原性 具有还原性 | 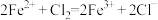 |
| C | 向 溶液中加入铁粉 溶液中加入铁粉 | 棕黄色溶液变为浅绿色 |  具有还原性 具有还原性 | 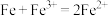 |
| D | 向 溶液中加入铜粉 溶液中加入铜粉 | 蓝色溶液变为棕黄色 |  具有氧化性 具有氧化性 | 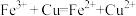 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-05更新
|
1073次组卷
|
8卷引用:重庆市万州第二高级中学2022-2023学年高一上学期12月线上考试化学试题
重庆市万州第二高级中学2022-2023学年高一上学期12月线上考试化学试题(苏教版2019)必修第二册专题9 金属与人类文明 第二单元 探究铁及其化合物的转化(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2022年高考化学考点微专题(已下线)3.1.2 铁盐和亚铁盐-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)第三章 铁 金属材料(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)内蒙古巴彦淖尔市第一中学2022-2023学年高一上学期1月期末考试化学试题湖南省泸溪县第一中学等多校联考2023-2024学年高二上学期8月月考化学试题云南省保山市腾冲市第八中学2023--2024学年高一上学期期末化学强化训练
7 . 已知: K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。某实验小组制备高铁酸钾(K2FeO4)并探究其性质。
(1)制备K2FeO4 (夹持装置图略)
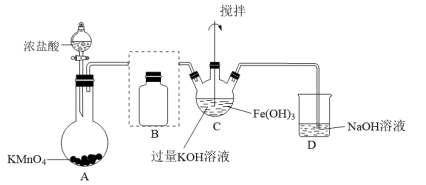
①A为氯气发生装置。A中反应的离子方程式是___________ (锰被还原为Mn2+)。
②将除杂装置图补充完整并标明所用试剂___________ 。
③C中得到紫色固体和溶液。C中Cl2发生的反应有① ,②(写离子方程式)
,②(写离子方程式)___________ 。
(2)探究K2FeO4的性质
首先,取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
①由方案I中溶液变红可知a中含有___________ 离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由___________ 产生。(用离子方程式表示)
②方案II可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是___________
③用高铁酸钠代替氯气作净水消毒剂的优点是___________ 。(答出两点即可)。
(1)制备K2FeO4 (夹持装置图略)

①A为氯气发生装置。A中反应的离子方程式是
②将除杂装置图补充完整并标明所用试剂

③C中得到紫色固体和溶液。C中Cl2发生的反应有①
 ,②(写离子方程式)
,②(写离子方程式)(2)探究K2FeO4的性质
首先,取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案I | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案II | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量,滴加盐酸,有Cl2产生。 |
②方案II可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是
③用高铁酸钠代替氯气作净水消毒剂的优点是
您最近一年使用:0次
名校
解题方法
8 . K2FeO4是一种高效水处理剂,紫色固体。实验小组制备高铁酸钾(K2FeO4)并探究其性质。已知K2FeO4具有下列性质:
①可溶于水、微溶于浓KOH溶液;②在0℃~5℃、强碱性溶液中比较稳定;③在酸性或中性条件下,能反应生成Fe(OH)3和O2。
(1)制备K2FeO4(夹持装置略)
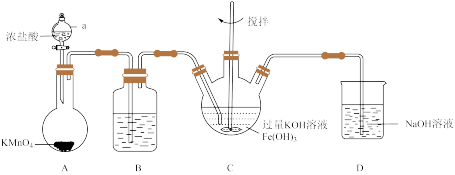
①A为氯气发生装置。其中,盛放KMnO4的仪器名称是_____ ;将Cl2通过装置B可除去杂质,以免影响实验,B中的试剂是_____ 。
②根据K2FeO4的制备实验得出:氧化性Cl2_____ FeO (填“>”或“<”),D装置的作用是
(填“>”或“<”),D装置的作用是_____ 。
③在不改变KOH溶液的浓度和体积的条件下,为了减少副反应,并提高K2FeO4产率,实验中可采取的措施是_____ 。
④C中得到紫色固体和溶液的化学方程式为_____ 。
(2)探究K2FeO4的性质
取C中紫色溶液,加入过量稀硫酸,产生黄绿色气体,得溶液X,经检验气体中含有Cl2。证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
①由方案Ⅰ中溶液变红可知X中含有Fe3+,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能因为_____ (请用离子方程式表示)。
②方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是_____ 。
①可溶于水、微溶于浓KOH溶液;②在0℃~5℃、强碱性溶液中比较稳定;③在酸性或中性条件下,能反应生成Fe(OH)3和O2。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置。其中,盛放KMnO4的仪器名称是
②根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),D装置的作用是
(填“>”或“<”),D装置的作用是③在不改变KOH溶液的浓度和体积的条件下,为了减少副反应,并提高K2FeO4产率,实验中可采取的措施是
④C中得到紫色固体和溶液的化学方程式为
(2)探究K2FeO4的性质
取C中紫色溶液,加入过量稀硫酸,产生黄绿色气体,得溶液X,经检验气体中含有Cl2。证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量X,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液Y。取少量Y,滴加盐酸,有Cl2产生。 |
②方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是
您最近一年使用:0次
名校
9 . 某兴趣小组,用如图所示实验方案探究 与
与 的相互转化,在控制其它试剂用量相同的条件下,改变KSCN溶液的用量,出现了异常现象。实验结果如下表所示。
的相互转化,在控制其它试剂用量相同的条件下,改变KSCN溶液的用量,出现了异常现象。实验结果如下表所示。
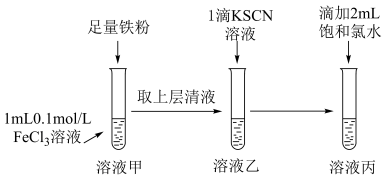
回答下列问题:
(1)试管1中发生反应的离子方程式为___________ 。
(2)编号①试管3中发生反应的离子方程式为___________ 和 。
。
(3)进一步探究编号②试管3中溶液褪色的原因,同学甲提出如下假设并设计了实验。
假设1:溶液褪色的原因是KSCN被转化。
假设2:溶液褪色的原因是___________ 。
同学乙查阅资料发现 可以被氧化成
可以被氧化成 ,请设计实验证明:
,请设计实验证明:
(4)编号③中未观察到溶液变红,可能的原因是___________ 。
 与
与 的相互转化,在控制其它试剂用量相同的条件下,改变KSCN溶液的用量,出现了异常现象。实验结果如下表所示。
的相互转化,在控制其它试剂用量相同的条件下,改变KSCN溶液的用量,出现了异常现象。实验结果如下表所示。
| 实验编号 |  /( /( ) ) | 试管1 | 试管2 | 试管3 |
| ① | 1 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色 |
| ② | 0.1 | 溶液变为红色,而后红色褪去 | ||
| ③ | 0.01 | 溶液变为棕黄色,未见红色 |
(1)试管1中发生反应的离子方程式为
(2)编号①试管3中发生反应的离子方程式为
 。
。(3)进一步探究编号②试管3中溶液褪色的原因,同学甲提出如下假设并设计了实验。
假设1:溶液褪色的原因是KSCN被转化。
假设2:溶液褪色的原因是
| 实验操作 | 实验现象 | 实验结论 |
| 取两份褪色后的溶液1mL于试管A、B中, | ||
| 往试管A中滴加 | 溶液恢复红色 | 假设1成立 |
| 往试管B中滴加 | 溶液未恢复红色 | 假设2不成立 |
 可以被氧化成
可以被氧化成 ,请设计实验证明:
,请设计实验证明:(4)编号③中未观察到溶液变红,可能的原因是
您最近一年使用:0次
2023-12-08更新
|
193次组卷
|
2卷引用:重庆市长寿区八校联考2023-2024学年高一上学期1月期末化学试题
名校
10 . 长期放置的 溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶
溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶 溶液进行了如表实验。
溶液进行了如表实验。
I.分别取2mL新制的 溶液于三支试管中,进行如图实验。
溶液于三支试管中,进行如图实验。
(1)方案ii中,紫色褪去发生的离子方程式是_______ 。
(2)方案iii的实验现象是_______ ,写出氯水参与反应的离子方程式:__ 。
II.久置的 溶液。
溶液。
(3)将上述实验iv__ 和实验v中的实验现象__ ;操作__ 补充完整。
(4)小组同学查阅资料得知,“维生素C可将 转化为
转化为 ”。为了验证维生素C的作用,设计了如表实验vi。
”。为了验证维生素C的作用,设计了如表实验vi。
由实验vi能否得出“维生素C可将 转化为
转化为 ”的结论?请说明理由
”的结论?请说明理由_______ 。
 溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶
溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶 溶液进行了如表实验。
溶液进行了如表实验。I.分别取2mL新制的
 溶液于三支试管中,进行如图实验。
溶液于三支试管中,进行如图实验。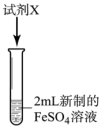 | 实验 | 试剂X | 实验现象 |
| 实验i | 1mL1mol/L NaOH溶液 | 现象a | |
| 实验ii | 5滴酸性 溶液 溶液 | 现象b:紫色褪去 | |
| 实验iii | 依次加入5滴KSCN溶液、5滴氯水 | 现象c |
(2)方案iii的实验现象是
II.久置的
 溶液。
溶液。| 实验操作 | 实验现象 | 实验结论 | |
| 实验iv | 取少量久置的 溶液于试管中,向其中滴加5滴KSCN溶液 溶液于试管中,向其中滴加5滴KSCN溶液 | _______ |  溶液部分变质 溶液部分变质 |
| 实验v | _______ | _______ | |
(4)小组同学查阅资料得知,“维生素C可将
 转化为
转化为 ”。为了验证维生素C的作用,设计了如表实验vi。
”。为了验证维生素C的作用,设计了如表实验vi。| 实验操作 | 实验现象 | |
| 实验vi | 取一定量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性 溶液 溶液 | 紫色褪去 |
 转化为
转化为 ”的结论?请说明理由
”的结论?请说明理由
您最近一年使用:0次
2022-12-29更新
|
300次组卷
|
2卷引用:重庆市南开中学2022-2023学年高一上学期12月定时练习化学试题

 溶液
溶液 加入装置A中,关闭活塞a
加入装置A中,关闭活塞a

