解题方法
1 . 阅读下列材料后,回答相应问题。
一个体重50kg的健康人大约含铁2g,这2g铁在人体中不是以单质金属形式存在,而是以 和
和 的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁(
的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁( )。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。
)。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。
(1)人体中经常进行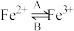 的相互转化,在A过程中,
的相互转化,在A过程中, 做
做_______ 剂;在B过程中, 做
做_______ 剂。
(2)“服用维生素C,可使食物中三价铁离子还原成二价铁离子。”这句话指出,维生素C具有_______ 性。
(3)向沸水中滴加饱和的 溶液制备
溶液制备 胶体,则其离子方程式为:
胶体,则其离子方程式为:_______ 。
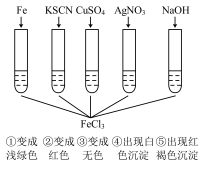
(4)为了验证 的性质,某化学兴趣小组设计了如下图所示的一组实验,其中实验结果一定错误的是_______(填字母)
的性质,某化学兴趣小组设计了如下图所示的一组实验,其中实验结果一定错误的是_______(填字母)
(5)已知:氧化性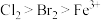 ,还原性
,还原性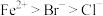 ,则向
,则向 1L
1L 溶液中通入标准状况下氯气2.24L,被氧化的粒子是
溶液中通入标准状况下氯气2.24L,被氧化的粒子是_______ 。
一个体重50kg的健康人大约含铁2g,这2g铁在人体中不是以单质金属形式存在,而是以
 和
和 的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁(
的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁( )。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。
)。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。(1)人体中经常进行
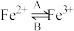 的相互转化,在A过程中,
的相互转化,在A过程中, 做
做 做
做(2)“服用维生素C,可使食物中三价铁离子还原成二价铁离子。”这句话指出,维生素C具有
(3)向沸水中滴加饱和的
 溶液制备
溶液制备 胶体,则其离子方程式为:
胶体,则其离子方程式为:(4)为了验证
 的性质,某化学兴趣小组设计了如下图所示的一组实验,其中实验结果一定错误的是_______(填字母)
的性质,某化学兴趣小组设计了如下图所示的一组实验,其中实验结果一定错误的是_______(填字母)
| A.④和⑤ | B.只有③ | C.③和④ | D.①②③ |
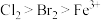 ,还原性
,还原性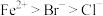 ,则向
,则向 1L
1L 溶液中通入标准状况下氯气2.24L,被氧化的粒子是
溶液中通入标准状况下氯气2.24L,被氧化的粒子是
您最近一年使用:0次
名校
解题方法
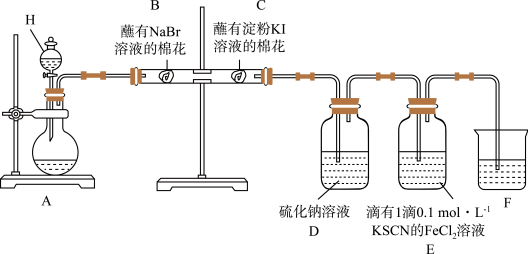
2 . 某同学利用以下装置探究非金属元素性质的递变规律,并验证氯气的性质。
回答下列问题:
(1)仪器H的名称为_______ 。
(2)能说明氯气的氧化性强于溴的实验现象为_______ 。
(3)氯气进入D中,反应的离子方程式为_______ 。
(4)E中溶液先变为红色,后红色褪去,为探究E中溶液褪色的原因,该同学提出两种假设:a. 被氧化:b.
被氧化:b._______ ,设计实验方案验证以上假设,向褪色后的溶液中滴加_______ ,若观察到_______ ,可验证假设b成立。
(5)实验结束后,取出B处的棉花与另一个蘸有淀粉 溶液的棉花G接触,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填标号)。
溶液的棉花G接触,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填标号)。

回答下列问题:
(1)仪器H的名称为
(2)能说明氯气的氧化性强于溴的实验现象为
(3)氯气进入D中,反应的离子方程式为
(4)E中溶液先变为红色,后红色褪去,为探究E中溶液褪色的原因,该同学提出两种假设:a.
 被氧化:b.
被氧化:b.(5)实验结束后,取出B处的棉花与另一个蘸有淀粉
 溶液的棉花G接触,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填标号)。
溶液的棉花G接触,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填标号)。A.氧化性: | B.同主族元素从上到下非金属性减弱 |
| C.同周期元素从左到右非金属性减弱 | D. 对应含氧酸酸性逐渐减弱 对应含氧酸酸性逐渐减弱 |
您最近一年使用:0次
2023-04-21更新
|
286次组卷
|
2卷引用:海南省琼海市嘉积中学2023-2024学年高一下学期开学化学试题
解题方法
3 . A、B、C、D四种物质都含有一种共同的元素,A是常见的金属,C的溶液呈现黄色,A、B、C、D之间有如图所示转化关系。
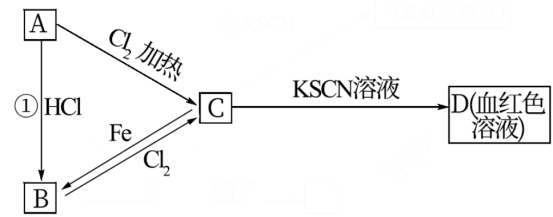
试回答下列问题:
(1)A是___________ ,C是_________________ 。
(2)C的溶液与NaOH溶液混合后产生的现象是______________________________ 。
(3)反应①的反应类型是___________________ 。
(4)从A、B、C三种物质中任选一种,从它们所含共同元素的价态上预测所选物质具有氧化性或还原性,并设计实验验证。
预测性质___________________________________________
主要操作___________________________________________
可能的现象__________________________________________

试回答下列问题:
(1)A是
(2)C的溶液与NaOH溶液混合后产生的现象是
(3)反应①的反应类型是
(4)从A、B、C三种物质中任选一种,从它们所含共同元素的价态上预测所选物质具有氧化性或还原性,并设计实验验证。
预测性质
主要操作
可能的现象
您最近一年使用:0次
4 . 实验室中利用如图所示装置(夹持装置略)制备 并进行实验探究。
并进行实验探究。
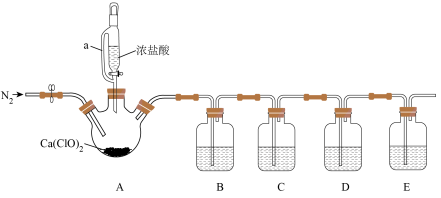
已知:C中试剂为滴有KSCN溶液的 溶液;D中试剂为
溶液;D中试剂为 的饱和溶液。
的饱和溶液。
回答下列问题:
(1)仪器a的名称为___________ 。
(2)写出装置A中生成 的化学方程式:
的化学方程式:___________ 。
(3)实验中观察到C中溶液先变红后褪色。
①溶液变红的原因为___________ 。
②溶液褪色的原因可能是___________ ,设计实验验证该猜想:___________ 。
(4)反应一段时间后,取D中适量溶液,加入 溶液,有白色沉淀生成。该实验能否证明氯气具有氧化性
溶液,有白色沉淀生成。该实验能否证明氯气具有氧化性___________ (填“能”或“不能”),若能,说明理由;若不能,请设计实验证明:___________ 。
 并进行实验探究。
并进行实验探究。
已知:C中试剂为滴有KSCN溶液的
 溶液;D中试剂为
溶液;D中试剂为 的饱和溶液。
的饱和溶液。回答下列问题:
(1)仪器a的名称为
(2)写出装置A中生成
 的化学方程式:
的化学方程式:(3)实验中观察到C中溶液先变红后褪色。
①溶液变红的原因为
②溶液褪色的原因可能是
(4)反应一段时间后,取D中适量溶液,加入
 溶液,有白色沉淀生成。该实验能否证明氯气具有氧化性
溶液,有白色沉淀生成。该实验能否证明氯气具有氧化性
您最近一年使用:0次
5 . 硫酸亚铁是一种重要的工业原料,同时可以用于制造补血药物,但其具有毒性,故严禁在食品中滥用硫酸亚铁。某同学为探究富含硫酸亚铁且保存时间较长的糕点的情况,设计了如下实验方案:

(1)试剂1的化学式是______________________ 。
(2)加入新制氯水后溶液红色加深的原因是____________ (用离子方程式表示)。
(3)该同学在实验中加入了过量的新制氯水,放置一段时间后,发现红色褪去,现对褪色原因进行探究(已知SCN-有还原性)。
[提出假设]
假设1:溶液中的+3价铁被氧化为更高的价态;
假设2:____________________________________________ 。
[设计方案]
(4)对提出的假设2进行验证,实验方案是________ 。
[应用拓展]
(5)FeSO4固体应________ 保存。

(1)试剂1的化学式是
(2)加入新制氯水后溶液红色加深的原因是
(3)该同学在实验中加入了过量的新制氯水,放置一段时间后,发现红色褪去,现对褪色原因进行探究(已知SCN-有还原性)。
[提出假设]
假设1:溶液中的+3价铁被氧化为更高的价态;
假设2:
[设计方案]
(4)对提出的假设2进行验证,实验方案是
[应用拓展]
(5)FeSO4固体应
您最近一年使用:0次
名校
6 . 已知下述三个实验均能发生化学反应,下列判断正确的是( )
①将铁钉放入硫酸铜溶液中②向硫酸亚铁溶液中滴入几滴浓硝酸③将铜丝放入氯化铁溶液中.
①将铁钉放入硫酸铜溶液中②向硫酸亚铁溶液中滴入几滴浓硝酸③将铜丝放入氯化铁溶液中.
| A.实验①中铁钉只做还原剂 | B.实验②中Fe2+既显氧化性有显还原性 |
| C.实验③中发生的是置换反应 | D.上述实验证明氧化性Fe3+>Fe2+>Cu2+ |
您最近一年使用:0次
2019-12-23更新
|
76次组卷
|
4卷引用:海南省农垦中学2023-2024学年上学期高三期末考试化学试题(B卷)
海南省农垦中学2023-2024学年上学期高三期末考试化学试题(B卷)(已下线)2012年人教版高中化学必修一3.2 几种重要的金属化合物练习卷江西省南昌市新建县第一中学2019-2020学年高一上学期第二次月考化学试题(已下线)【南昌新东方】2019 新建一中高一上第二次月考
名校
7 . 下列有关物质性质与用途具有对应关系的是
| A.SO2具有氧化性,可用于漂白纸浆 |
| B.Si的熔点高,可用作半导体材料 |
| C.FeCl3溶液显酸性,可用于蚀刻铜制的电路板 |
| D.漂白液中含有强氧化性物质,可作漂白剂和消毒剂 |
您最近一年使用:0次
2019-11-19更新
|
323次组卷
|
4卷引用:海南省琼海市嘉积第三中学2021-2022学年高三下学期第二次月考化学科试题
名校
解题方法
8 . 某小组同学探究FeCl3溶液显黄色的原因。
资料:i.FeCl3溶液中存在平衡:[Fe(H2O)6]3++H2O⇌[Fe(H2O)5]2++H3O+
ii.Fe3+与 不能形成配位键。
不能形成配位键。
(1)Fe3+的核外电子排布式为___________ 。
[猜想与预测]
小组同学认为可能是Fe3+与其他微粒配位形成的配离子导致溶液显黄色,进而提出以下猜想:
Ⅰ.Fe3+与OH-配位 Ⅱ.Fe3+与H2O配位 Ⅲ.Fe3+与Cl-配位
(2)解释Fe3+可与这些微粒形成配合物的原因:___________ 。
[实验与分析]
为验证猜想I,小组同学设计并完成了以下实验。
(3)实验a的作用是___________ 。
(4)①甲同学认为实验c可以证明猜想Ⅰ成立,而猜想Ⅱ不成立,理由是___________ 。小组同学为了证明猜想Ⅲ成立,将实验c所得溶液分为两份进行了如下实验:
②实验d的实验现象为___________ ,证明猜想Ⅲ成立
[结论与反思]
(5)依据上述现象解释FeCl3溶液显黄色的原因是___________ 。
(6)已知EDTA与Fe3+配位能力比SCN-更强,设计实验证明Fe3+与EDTA形成的配合物为浅黄色(EDTA通常配成溶液使用):___________ 。
资料:i.FeCl3溶液中存在平衡:[Fe(H2O)6]3++H2O⇌[Fe(H2O)5]2++H3O+
ii.Fe3+与
 不能形成配位键。
不能形成配位键。(1)Fe3+的核外电子排布式为
[猜想与预测]
小组同学认为可能是Fe3+与其他微粒配位形成的配离子导致溶液显黄色,进而提出以下猜想:
Ⅰ.Fe3+与OH-配位 Ⅱ.Fe3+与H2O配位 Ⅲ.Fe3+与Cl-配位
(2)解释Fe3+可与这些微粒形成配合物的原因:
[实验与分析]
为验证猜想I,小组同学设计并完成了以下实验。
| 实验 | a | b | c |
| 实验操作 | 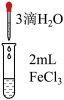 |  | 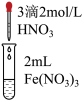 |
| 实验现象 | 溶液黄色略变浅 | 溶液黄色略变浅 | 黄色褪去 |
(4)①甲同学认为实验c可以证明猜想Ⅰ成立,而猜想Ⅱ不成立,理由是
| 实验 | d | e |
| 实验操作 | 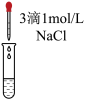 |  |
| 实验现象 | _______ | 溶液仍为无色 |
[结论与反思]
(5)依据上述现象解释FeCl3溶液显黄色的原因是
(6)已知EDTA与Fe3+配位能力比SCN-更强,设计实验证明Fe3+与EDTA形成的配合物为浅黄色(EDTA通常配成溶液使用):
您最近一年使用:0次
9 . FeCl3能用于金属蚀刻、污水处理、印染工业,易潮解,加热易升华。某化学研究性学习小组模拟工业生产流程制备氯化铁并对产物做如下探究实验(部分夹持装置省略)。

(1)盛放MnO2的仪器名称为___________
(2)装置A中制氯气反应的离子方程式为___________ 。
(3)若缺少装置E,对本实验造成的影响是___________ 。
(4)将铁粉分散到石棉绒中的优点是___________ ,当硬质玻璃管中___________ 时,开始点燃D处的酒精灯。
(5)实验结束并冷却后,将收集器中的固体物质转移至锥形瓶中,进行如下实验:

查阅资料可知:SCN-能被氧化剂氧化。该小组对红色褪去的原因进行探究:
假设1:O2将SCN-氧化。
假设2:H2O2将SCN-氧化
通过设计如下实验得出假设2成立,请在下表空格中填写现象:

(1)盛放MnO2的仪器名称为
(2)装置A中制氯气反应的离子方程式为
(3)若缺少装置E,对本实验造成的影响是
(4)将铁粉分散到石棉绒中的优点是
(5)实验结束并冷却后,将收集器中的固体物质转移至锥形瓶中,进行如下实验:

查阅资料可知:SCN-能被氧化剂氧化。该小组对红色褪去的原因进行探究:
假设1:O2将SCN-氧化。
假设2:H2O2将SCN-氧化
通过设计如下实验得出假设2成立,请在下表空格中填写现象:
| 实验 | 操作 | 现象 | |
| 实验I(取褪色后的溶液2等份) | 第1份 | 滴加FeCl3溶液 | 无明显变化 |
| 第2份 | 滴加过量KSCN溶液 | ||
| 实验Ⅱ | 向实验Ⅰ的第2份溶液中再通入O2 | ||
您最近一年使用:0次
解题方法
10 . 下列实验操作与预期实验目的或所得实验结论一致的是( )
| 选项 | 实验操作和现象 | 预期实验目的或结论 |
| A | 向Fe(NO3)2溶液中滴加盐酸,溶液转为黄色 | 说明盐酸具有氧化性 |
| B | 向一定浓度的Na2SiO3溶液中通入适量的CO2气 体,有白色沉淀 | 说明H2CO3的酸性比H2SiO3的酸性强 |
| C | 某气体通入澄清石灰水溶液中,没有沉淀 | 说明该气体中肯定没有CO2 |
| D | 室温下向CuCl2和少量FeCl3的混合溶液中,加入 铜屑,充分搅拌,过滤,得蓝绿色溶液 | 除去杂质FeCl3得纯净物CuCl2溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
203次组卷
|
2卷引用:2016届海南中学高三考前高考模拟十化学试卷



