解题方法
1 . 下列实验操作及现象均正确,不能得出相应结论的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 将氯气与铁反应后的剩余固体加入盐酸中,固体全部溶解,滴加 溶液后无现象 溶液后无现象 | 氯气与铁反应生成 |
| B | 将足量锌粉分别加入等体积、等 的 的 和 和 弱酸溶液中,反应结束后, 弱酸溶液中,反应结束后, 溶液产生更多的氢气 溶液产生更多的氢气 |  |
| C | 将葡萄糖溶液加入酸性 溶液中,溶液紫红色褪去 溶液中,溶液紫红色褪去 | 葡萄糖具有还原性 |
| D | 将 通入 通入 气体中,瓶壁上产生黄色固体 气体中,瓶壁上产生黄色固体 |  具有氧化性 具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 比较 与 与 结合 结合 的能力 的能力 | 室温下,用pH计测相同物质的量浓度的 溶液和NaClO溶液的pH 溶液和NaClO溶液的pH | NaClO溶液的pH大 |  结合 结合 的能力比 的能力比 强 强 |
| B | 验证 消去生成乙烯 消去生成乙烯 | 乙醇与浓硫酸混合迅速加热至170℃,产生的气体通入酸性 溶液中 溶液中 |  溶液褪色 溶液褪色 | 生成了乙烯 |
| C | 探究CO还原 的固体产物 的固体产物 | 往 还原 还原 所得固体产物中先加稀盐酸,再滴加KSCN溶液 所得固体产物中先加稀盐酸,再滴加KSCN溶液 | 溶液不变红 | 固体产物为Fe |
| D | 探究反应物浓度和反应速率的关系 | 往各盛有4mL  酸性 酸性 溶液的a、b两试管中分别加入2mL 溶液的a、b两试管中分别加入2mL  、 、 的草酸溶液 的草酸溶液 | b试管溶液颜色比a浅 | 反应物浓度越大,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 硫代硫酸钠 是重要的化工原料,易溶于水。实验室中探究
是重要的化工原料,易溶于水。实验室中探究 与某些金属阳离子的氧化还原反应情况。
与某些金属阳离子的氧化还原反应情况。
资料:i.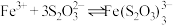 (紫黑色)
(紫黑色) 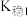 ;
;
ii. 为白色沉淀,
为白色沉淀,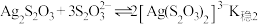 ;
;
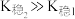 。
。
回答下列问题:
探究一
(1)根据实验①的现象,初步判断最终 被
被 还原为
还原为 ,通过
,通过_____ (填操作、试剂和现象),进一步证实生成了 。进一步实验证明
。进一步实验证明 最终被氧化为
最终被氧化为 ,该过程总反应的化学方程式为
,该过程总反应的化学方程式为_____ 。
(2)氧化性: (同浓度)。但实验②中
(同浓度)。但实验②中 未发生氧化还原反应的原因是
未发生氧化还原反应的原因是_____ 。
探究二
(3)实验③中黑色沉淀可能为 或
或 。通过
。通过_____ (填操作、试剂和现象),进一步证实生成了 。白色絮状沉淀变为黑色沉淀的化学方程式为
。白色絮状沉淀变为黑色沉淀的化学方程式为_____ 。
(4)将 溶液逐滴滴入
溶液逐滴滴入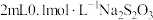 溶液中至过量,该过程可观察到的实验现象为
溶液中至过量,该过程可观察到的实验现象为_____ 。
 是重要的化工原料,易溶于水。实验室中探究
是重要的化工原料,易溶于水。实验室中探究 与某些金属阳离子的氧化还原反应情况。
与某些金属阳离子的氧化还原反应情况。资料:i.
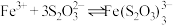 (紫黑色)
(紫黑色) 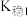 ;
;ii.
 为白色沉淀,
为白色沉淀,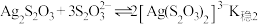 ;
;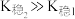 。
。回答下列问题:
探究一
| 装置 | 编号 | 试剂X | 实验现象 |
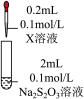 | ① | 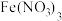 溶液 溶液 | 混合后溶液先变成紫黑色,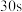 后溶液几乎变为无色 后溶液几乎变为无色 |
| ② |  溶液 溶液 | 一段时间后,生成白色沉淀,振荡后,沉淀溶解,得到无色溶液 |
 被
被 还原为
还原为 ,通过
,通过 。进一步实验证明
。进一步实验证明 最终被氧化为
最终被氧化为 ,该过程总反应的化学方程式为
,该过程总反应的化学方程式为(2)氧化性:
 (同浓度)。但实验②中
(同浓度)。但实验②中 未发生氧化还原反应的原因是
未发生氧化还原反应的原因是探究二
| 装置 | 编号 | 试剂X | 实验现象 |
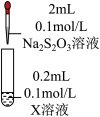 | ③ |  溶液 溶液 | 立即生成白色絮状沉淀,沉淀很快变为黑色沉淀。 |
 或
或 。通过
。通过 。白色絮状沉淀变为黑色沉淀的化学方程式为
。白色絮状沉淀变为黑色沉淀的化学方程式为(4)将
 溶液逐滴滴入
溶液逐滴滴入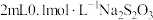 溶液中至过量,该过程可观察到的实验现象为
溶液中至过量,该过程可观察到的实验现象为
您最近一年使用:0次
名校
解题方法
4 . 下列实验探究方案不能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 将二氧化硫气体通入碘和淀粉的混合溶液中,观察溶液颜色的变化 | 探究还原性: |
| B | 向盛有 溶液的试管中滴加几滴 溶液的试管中滴加几滴 溶液。振荡,观察颜色的变化 溶液。振荡,观察颜色的变化 | 探究 是否变质 是否变质 |
| C | 加热溴乙烷和氢氧化钠-乙醇混合溶液,将产生的气体通入高锰酸钾溶液中。观察溶液颜色的变化 | 探究溴乙烷在此条件下发生的是取代反应还是消去反应 |
| D | 向盛有等浓度的NaCl和KI混合溶液的试管中滴加几滴 溶液,振荡,观察沉淀颜色 溶液,振荡,观察沉淀颜色 | 证明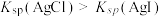 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-06更新
|
419次组卷
|
3卷引用:河北省秦皇岛市2022-2023学年高二下学期期末考试化学试题
5 . 工业上常用碳酸锰矿为主要原料来生产干电池的材料 ,为了去除碳酸锰矿中含有的少量金属离子(
,为了去除碳酸锰矿中含有的少量金属离子( 、
、 、
、 、
、 、
、 等)而获得
等)而获得 ,设计了如图所示的工艺流程:
,设计了如图所示的工艺流程:
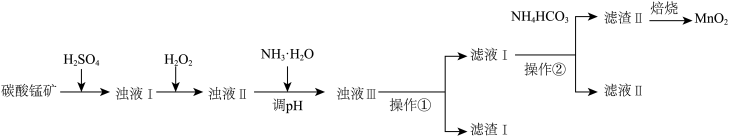
有关金属阳离子开始沉淀和沉淀完全的pH如下表:
回答下列问题:
(1)操作①和②的名称为___________ ,此操作需用到的玻璃仪器有___________ 。
(2)“滤渣I”中含有的物质是___________ 。
(3)加入 的作用为
的作用为___________ ,写出其发生反应的离子方程式:________ 。检验“浊液III”中是否含有 的方法:取少许浊液于试管中,静置;再取少许上层清液,滴入
的方法:取少许浊液于试管中,静置;再取少许上层清液,滴入_______ (填化学式)溶液,观察清液现象。
(4)写出加入 生成气体时发生反应的化学方程式:
生成气体时发生反应的化学方程式:___________ 。
(5)“滤液II”中可回收的物质为___________ (填化学式),其在农业上常用作___________ 。
 ,为了去除碳酸锰矿中含有的少量金属离子(
,为了去除碳酸锰矿中含有的少量金属离子( 、
、 、
、 、
、 、
、 等)而获得
等)而获得 ,设计了如图所示的工艺流程:
,设计了如图所示的工艺流程:
有关金属阳离子开始沉淀和沉淀完全的pH如下表:
| 金属阳离子 |  |  |  |  |  |  |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 8.0 | 8.3 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.8 | 9.8 |
(1)操作①和②的名称为
(2)“滤渣I”中含有的物质是
(3)加入
 的作用为
的作用为 的方法:取少许浊液于试管中,静置;再取少许上层清液,滴入
的方法:取少许浊液于试管中,静置;再取少许上层清液,滴入(4)写出加入
 生成气体时发生反应的化学方程式:
生成气体时发生反应的化学方程式:(5)“滤液II”中可回收的物质为
您最近一年使用:0次
名校
6 . 下列实验目的、实验操作及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 验证肉桂醛中含碳碳双键 | 向肉桂醛(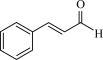 )中加入酸性KMnO4溶液 )中加入酸性KMnO4溶液 | 肉桂醛中含有碳碳双键 |
| B | 比较CuSO4和KMnO4的催化效果 | 向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4溶液和KMnO4溶液,CuSO4溶液产生气泡速率快 | CuSO4催化H2O2溶液分解效果更好 |
| C | 验证菠菜中含有铁元素 | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入几滴KSCN溶液,溶液不变红 | 说明菠菜中不含铁元素 |
| D | 判断强酸和弱酸 | NaHCO3溶液显碱性,NaHSO3溶液显酸性 | 可以确定H2CO3是弱酸,无法判断H2SO3是否为弱酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-19更新
|
807次组卷
|
2卷引用:江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题
7 . 高铁酸钾( )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。它可通过干法和湿法等途径来制备。已知它的相关性质:
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。它可通过干法和湿法等途径来制备。已知它的相关性质:
①不溶于乙醚、醇和氯仿等有机溶剂。
②极易溶于水。
③热稳定性差,在低温、强碱性溶液中相当稳定。
请结合其制备方法,回答下列问题:
I.干法制备:将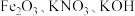 混合加热共熔,发生的反应为:
混合加热共熔,发生的反应为: (未配平)
(未配平)
(1)上述反应中作氧化剂的物质为_______ (填化学式),制备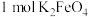 理论上需
理论上需 的物质的量为
的物质的量为_______ 。
Ⅱ.湿法制备:利用 、
、 和
和 等为原料制备,其生产流程如下:
等为原料制备,其生产流程如下:
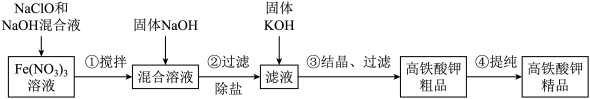
(2) 溶液的浓度和配比对产品的产率有较大的影响,现要配制
溶液的浓度和配比对产品的产率有较大的影响,现要配制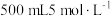 的
的 溶液,需要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和
溶液,需要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和_______ ,若 加入过量,在碱性介质中
加入过量,在碱性介质中 与
与 发生氧化还原反应生成
发生氧化还原反应生成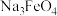 ,此反应的离子方程式为
,此反应的离子方程式为_______ 。
(3)将固体 加入混合液中是为了除去高铁酸钠中混有的钠盐杂质(除盐),钠盐杂质除
加入混合液中是为了除去高铁酸钠中混有的钠盐杂质(除盐),钠盐杂质除 外,主要是指
外,主要是指 和
和_______ (填化学式),此操作是利用了钠盐杂质在强碱溶液中溶解度_______ (填“大”或“小”)的性质从而实现与高铁酸钠分离。
(4)将固体 加入到滤液中发生了物质的转化,写出该反应的化学方程式
加入到滤液中发生了物质的转化,写出该反应的化学方程式_______ 。
(5)关于高铁酸钾的制备,下列说法错误的是_______(填字母)。
 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。它可通过干法和湿法等途径来制备。已知它的相关性质:
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。它可通过干法和湿法等途径来制备。已知它的相关性质:①不溶于乙醚、醇和氯仿等有机溶剂。
②极易溶于水。
③热稳定性差,在低温、强碱性溶液中相当稳定。
请结合其制备方法,回答下列问题:
I.干法制备:将
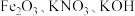 混合加热共熔,发生的反应为:
混合加热共熔,发生的反应为: (未配平)
(未配平)(1)上述反应中作氧化剂的物质为
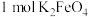 理论上需
理论上需 的物质的量为
的物质的量为Ⅱ.湿法制备:利用
 、
、 和
和 等为原料制备,其生产流程如下:
等为原料制备,其生产流程如下:
(2)
 溶液的浓度和配比对产品的产率有较大的影响,现要配制
溶液的浓度和配比对产品的产率有较大的影响,现要配制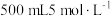 的
的 溶液,需要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和
溶液,需要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和 加入过量,在碱性介质中
加入过量,在碱性介质中 与
与 发生氧化还原反应生成
发生氧化还原反应生成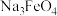 ,此反应的离子方程式为
,此反应的离子方程式为(3)将固体
 加入混合液中是为了除去高铁酸钠中混有的钠盐杂质(除盐),钠盐杂质除
加入混合液中是为了除去高铁酸钠中混有的钠盐杂质(除盐),钠盐杂质除 外,主要是指
外,主要是指 和
和(4)将固体
 加入到滤液中发生了物质的转化,写出该反应的化学方程式
加入到滤液中发生了物质的转化,写出该反应的化学方程式(5)关于高铁酸钾的制备,下列说法错误的是_______(填字母)。
| A.干法制备的优点是步骤简单,但反应温度难以控制,熔融态的强碱存在严重腐蚀反应容器;湿法制备的优点是工艺成熟,但步骤多、操作较困难。 |
B.在湿法制备中,往滤液中加入固体 时,要在冰水浴中缓慢分多次加入。 时,要在冰水浴中缓慢分多次加入。 |
| C.在湿法制备中,第④步提纯需要采用重结晶操作,该操作第一步是将粗产品加水溶解。 |
| D.在湿法制备中,第④步提纯需将结晶的高铁酸钾过滤、洗涤、干燥,洗涤、干燥的目的是脱碱、脱水,洗涤时可用异丙醇洗涤。 |
您最近一年使用:0次
名校
8 . 在分析化学上,测定含 酸性溶液中钛元素的含量通常涉及两个反应:
酸性溶液中钛元素的含量通常涉及两个反应:
I.用 粉还原
粉还原 得到
得到 ;
;
II.用 溶液滴定,反应的离子方程式为
溶液滴定,反应的离子方程式为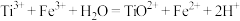 。
。
下列说法错误的是
 酸性溶液中钛元素的含量通常涉及两个反应:
酸性溶液中钛元素的含量通常涉及两个反应:I.用
 粉还原
粉还原 得到
得到 ;
;II.用
 溶液滴定,反应的离子方程式为
溶液滴定,反应的离子方程式为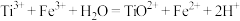 。
。下列说法错误的是
A.还原性: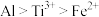 |
B.反应I中氧化产物和还原产物的物质的量之比为 |
C.反应II的滴定实验可选用 溶液作指示剂 溶液作指示剂 |
D.反应I中生成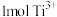 时消耗的 时消耗的 和反应Ⅱ中消耗 和反应Ⅱ中消耗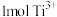 时生成的 时生成的 的量相同 的量相同 |
您最近一年使用:0次
2023-02-14更新
|
653次组卷
|
4卷引用:湖南省新高考教学教研联盟(长郡十八校联盟)2022-2023学年高二下学期5月联考化学试题
名校
解题方法
9 . 草酸亚铁晶体是生产感光材料的原料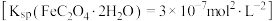 ,制备流程如下:
,制备流程如下:
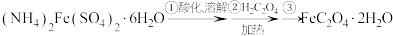
下列说法错误的是
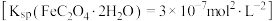 ,制备流程如下:
,制备流程如下: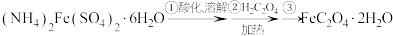
下列说法错误的是
A.可用 溶液检验 溶液检验 是否变质 是否变质 |
B.步骤①酸化的目的是抑制 的水解 的水解 |
C.步骤②反应为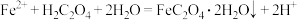 |
| D.步骤③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
您最近一年使用:0次
2022-05-15更新
|
924次组卷
|
4卷引用:吉林省吉林市第一中学2021-2022学年高二下学期6月月考化学试题(理科创新班)
吉林省吉林市第一中学2021-2022学年高二下学期6月月考化学试题(理科创新班)山东省青岛市2021-2022学年高三下学期高考模拟检测(二)化学试题(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
10 . 铁粉可用于处理水中污染物。铁粉的氧化物层可以导电。
(1)富铁矿石经破碎、筛分到微米级后,在氢气氛围下 高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:
高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:___________ 。
(2)采用 溶液还原铁盐,可以制备纳米级的铁粉,并生成
溶液还原铁盐,可以制备纳米级的铁粉,并生成 。
。
① 中
中 离子的空间构型为
离子的空间构型为___________ 。
②由 每生成
每生成 ,需要
,需要 物质的量是
物质的量是___________  。
。
(3)利用纳米铁粉可以有效处理废水中的 和
和 ,去除机理如图1所示。
,去除机理如图1所示。
①纳米铁粉去除污水中 和
和 机理不同,请解释原因并简述两者的区别
机理不同,请解释原因并简述两者的区别___________ 。


②由图2可知,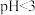 时,随
时,随 减小,
减小, 和
和 去除率减小的原因是
去除率减小的原因是___________ 。
(1)富铁矿石经破碎、筛分到微米级后,在氢气氛围下
 高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:
高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:(2)采用
 溶液还原铁盐,可以制备纳米级的铁粉,并生成
溶液还原铁盐,可以制备纳米级的铁粉,并生成 。
。①
 中
中 离子的空间构型为
离子的空间构型为②由
 每生成
每生成 ,需要
,需要 物质的量是
物质的量是 。
。(3)利用纳米铁粉可以有效处理废水中的
 和
和 ,去除机理如图1所示。
,去除机理如图1所示。①纳米铁粉去除污水中
 和
和 机理不同,请解释原因并简述两者的区别
机理不同,请解释原因并简述两者的区别

②由图2可知,
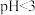 时,随
时,随 减小,
减小, 和
和 去除率减小的原因是
去除率减小的原因是
您最近一年使用:0次
2022-01-24更新
|
472次组卷
|
2卷引用:江苏省扬州中学2021-2022学年高二下学期3月月考高二化学试题



