名校
1 . 高纯MgO具有优良的电绝缘性、高导热性等,常被用作绝缘材料填料、高温耐热材料。由白云石[主要成分为 ,含少量
,含少量 、
、 、
、 等杂质]制备高纯MgO和副产品
等杂质]制备高纯MgO和副产品 的一种流程如下:
的一种流程如下:
(1)请写出基态Ca原子的价电子排布式___________ 。
(2)步骤“煅烧1”中, 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(3)“铵浸”时,含钙化合物被浸取,含镁化合物部分水化生成 (
(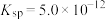 )。若铵浸液中
)。若铵浸液中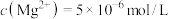 ,则其pH=
,则其pH=___________ ;滤饼“水化反应”后,将体系冷却到与铵浸液相同温度,得到主要含有 的悬浊液,其中
的悬浊液,其中
___________ 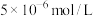 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(4)“沉钙”时主要发生反应的离子方程式为___________ 。
(5)“碳化反应”时,镁化合物转化为可溶于水的___________ (填化学式,下同),滤渣的主要成分为___________ 。
(6)“热解”时生成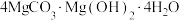 (碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是
(碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是___________ 。
 ,含少量
,含少量 、
、 、
、 等杂质]制备高纯MgO和副产品
等杂质]制备高纯MgO和副产品 的一种流程如下:
的一种流程如下: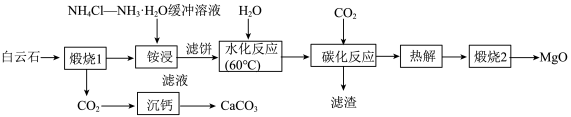
(1)请写出基态Ca原子的价电子排布式
(2)步骤“煅烧1”中,
 发生反应的化学方程式为
发生反应的化学方程式为(3)“铵浸”时,含钙化合物被浸取,含镁化合物部分水化生成
 (
(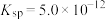 )。若铵浸液中
)。若铵浸液中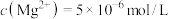 ,则其pH=
,则其pH= 的悬浊液,其中
的悬浊液,其中
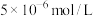 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(4)“沉钙”时主要发生反应的离子方程式为
(5)“碳化反应”时,镁化合物转化为可溶于水的
(6)“热解”时生成
 (碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是
(碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是
您最近一年使用:0次
名校
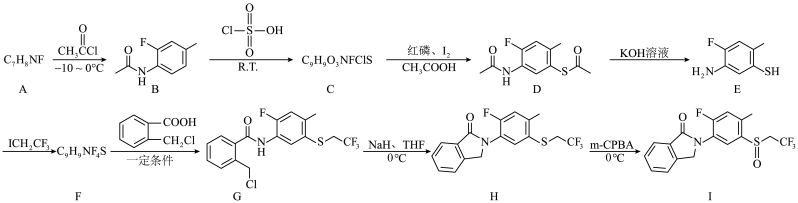
2 . 化合物I是一种高活性杀螨剂,通过抑制螨的脂肪合成从而阻断其能量代谢来发挥作用。以下为其合成路线之一。
(1)A中官能团名称是_______ 。
(2)B的分子式为_______ 。
(3)C的结构简式为_______ 。
(4)E→F的反应类型为_______ 。
(5)F→G的化学方程式为_______ 。
(6)在B的同分异构体中,同时满足下列条件的共有_______ 种(不考虑立体异构)。
①含有苯环
②能发生银镜反应
③苯环上有两个取代基,其中一个取代基为氨基( )与苯环直接相连
)与苯环直接相连
其中,核磁共振氢谱显示为5组峰,且峰面积之比为3∶2∶2∶2∶1的同分异构体的结构简式为
_______ 。
(1)A中官能团名称是
(2)B的分子式为
(3)C的结构简式为
(4)E→F的反应类型为
(5)F→G的化学方程式为
(6)在B的同分异构体中,同时满足下列条件的共有
①含有苯环
②能发生银镜反应
③苯环上有两个取代基,其中一个取代基为氨基(
 )与苯环直接相连
)与苯环直接相连其中,核磁共振氢谱显示为5组峰,且峰面积之比为3∶2∶2∶2∶1的同分异构体的结构简式为
您最近一年使用:0次
名校
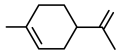
3 . Ⅰ 重庆奉节的脐橙闻名遐迩,从脐橙果皮中提取的橙油具有抗菌抑菌、抗氧化、祛痰平喘等多种作用,常用于医药、食品加工、日化等多个领域。橙油的主要成分是柠檬烯,其结构简式如下。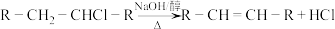 R为烃基或H
R为烃基或H
(1)柠檬烯的分子式______ ,官能团名称______ 。
(2)柠檬烯的一氯代物:______ 种。
(3)写出A→B的化学方程式:______ 。
(4)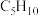 不属于烯烃的同分异构体有
不属于烯烃的同分异构体有______ 种。
(5)E的结构简式:______ 。
Ⅱ 高分子的循环利用过程如下图所示。______ 。
(7)b与 发生加成反应最多可生成
发生加成反应最多可生成______ 种二溴代物。

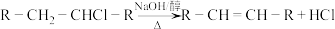 R为烃基或H
R为烃基或H(2)
(1)柠檬烯的分子式
(2)柠檬烯的一氯代物:
(3)写出A→B的化学方程式:
(4)
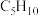 不属于烯烃的同分异构体有
不属于烯烃的同分异构体有(5)E的结构简式:
Ⅱ 高分子的循环利用过程如下图所示。
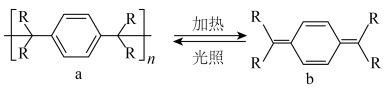 (R为
(R为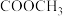 )
)
(7)b与
 发生加成反应最多可生成
发生加成反应最多可生成
您最近一年使用:0次
名校
4 . 肼( )是一种强还原性的高能物质,在航天、能源等领域有广泛应用。
)是一种强还原性的高能物质,在航天、能源等领域有广泛应用。
(1)火箭发射可以用肼(液态)作燃料, 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。
已知:
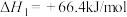
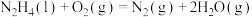
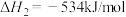
请写出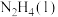 与
与 反应的热化学方程式
反应的热化学方程式______ 。
(2)向恒容密闭容器内加入一定量 ,一定条件下体系中存在以下平衡:
,一定条件下体系中存在以下平衡:
Ⅰ.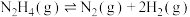
Ⅱ.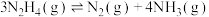
在较高温度肼几乎分解完全,分解产物的物质的量随温度变化如图:______ 。
②在较高温度肼几乎分解完全的原因可能是______ 。
③N点时,体系内 为
为______ 。
(3) 是二元弱碱,
是二元弱碱, 在水溶液中存在如下两步电离:
在水溶液中存在如下两步电离:
①
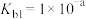 ;
;
②__________________________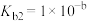 。
。
①写出 在水溶液中的第②步电离方程式:
在水溶液中的第②步电离方程式:______ 。
②25℃时,向 的水溶液中加入稀硫酸,欲使
的水溶液中加入稀硫酸,欲使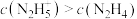 ,同时
,同时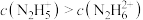 ,应控制溶液的
,应控制溶液的 范围为
范围为______ (用含a、b的式子表示)。
(4)利用 燃料电池电解
燃料电池电解 溶液并制备
溶液并制备 ,装置如图所示(
,装置如图所示(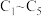 均为石墨电极,假设各装置在工作过程中溶液体积不变)。
均为石墨电极,假设各装置在工作过程中溶液体积不变)。 电极反应式为
电极反应式为______ 。
②若甲装置 电极上消耗标准状况下1.12L的
电极上消耗标准状况下1.12L的 ,理论上丙装置阳极室溶液质量减少
,理论上丙装置阳极室溶液质量减少______ g。
 )是一种强还原性的高能物质,在航天、能源等领域有广泛应用。
)是一种强还原性的高能物质,在航天、能源等领域有广泛应用。(1)火箭发射可以用肼(液态)作燃料,
 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。已知:

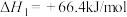
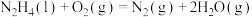
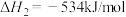
请写出
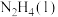 与
与 反应的热化学方程式
反应的热化学方程式(2)向恒容密闭容器内加入一定量
 ,一定条件下体系中存在以下平衡:
,一定条件下体系中存在以下平衡:Ⅰ.
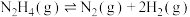
Ⅱ.
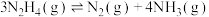
在较高温度肼几乎分解完全,分解产物的物质的量随温度变化如图:
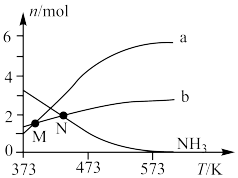
②在较高温度肼几乎分解完全的原因可能是
③N点时,体系内
 为
为(3)
 是二元弱碱,
是二元弱碱, 在水溶液中存在如下两步电离:
在水溶液中存在如下两步电离:①

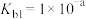 ;
;②__________________________
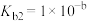 。
。①写出
 在水溶液中的第②步电离方程式:
在水溶液中的第②步电离方程式:②25℃时,向
 的水溶液中加入稀硫酸,欲使
的水溶液中加入稀硫酸,欲使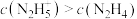 ,同时
,同时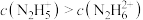 ,应控制溶液的
,应控制溶液的 范围为
范围为(4)利用
 燃料电池电解
燃料电池电解 溶液并制备
溶液并制备 ,装置如图所示(
,装置如图所示(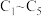 均为石墨电极,假设各装置在工作过程中溶液体积不变)。
均为石墨电极,假设各装置在工作过程中溶液体积不变)。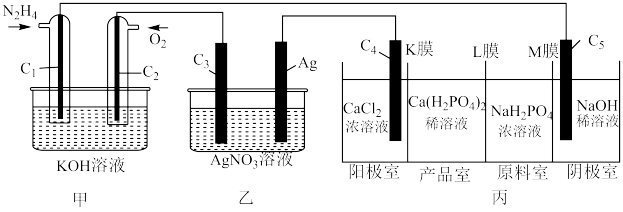
 电极反应式为
电极反应式为②若甲装置
 电极上消耗标准状况下1.12L的
电极上消耗标准状况下1.12L的 ,理论上丙装置阳极室溶液质量减少
,理论上丙装置阳极室溶液质量减少
您最近一年使用:0次
解题方法
5 . 我国承诺2030年前,二氧化碳的排放不再增长。为更早实现“碳达峰”“碳中和”,彰显中国作为大国的责任与担当。诸多科学家都在大力研究将 甲烷化、
甲烷化、 甲醇化、
甲醇化、 碳酸二甲酯(DMC)化从而减少碳的排放。
碳酸二甲酯(DMC)化从而减少碳的排放。
(1) 甲烷化其相关反应的热化学方程式如下:
甲烷化其相关反应的热化学方程式如下:
ⅰ. ;
;
ⅱ. ;
;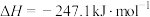
①写出 甲烷化的热化学方程式:
甲烷化的热化学方程式:___________ 。
②实际生产中,为提高 甲烷化时生产效率,反应适宜在
甲烷化时生产效率,反应适宜在___________ 条件下进行。
a.高温低压 b.高温高压 c.低温高压
③已知反应ⅰ的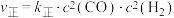 ,
,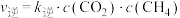 ,
, 、
、 为速率常数,若反应达平衡后升高温度,则
为速率常数,若反应达平衡后升高温度,则 值
值___________ 。(填“增大”“不变”或“减小”)。
(2) 甲醇化其中涉及的主要反应:
甲醇化其中涉及的主要反应:
ⅰ. ;
;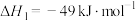
ⅱ. ;
;
①某研究小组利用 催化剂将
催化剂将 转化为甲醇的机理如图所示。在该历程中,优先与催化剂反应的物质是
转化为甲醇的机理如图所示。在该历程中,优先与催化剂反应的物质是___________ :生成的甲醇分子的氧原子来自___________ 。(填化学式) ,保持压强为p MPa合成甲醇。达到平衡时,
,保持压强为p MPa合成甲醇。达到平衡时, 的转化率、
的转化率、 和CO的选择性随温度变化关系如图。
和CO的选择性随温度变化关系如图。
 的选择性=
的选择性=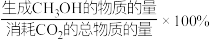 ;
;
CO的选择性=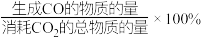 。
。
270℃反应达到平衡,水蒸气的分压为___________ p MPa,反应ⅱ的 为
为___________ 。(均保留2位有效数字)
 甲烷化、
甲烷化、 甲醇化、
甲醇化、 碳酸二甲酯(DMC)化从而减少碳的排放。
碳酸二甲酯(DMC)化从而减少碳的排放。(1)
 甲烷化其相关反应的热化学方程式如下:
甲烷化其相关反应的热化学方程式如下:ⅰ.
 ;
;
ⅱ.
 ;
;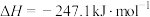
①写出
 甲烷化的热化学方程式:
甲烷化的热化学方程式:②实际生产中,为提高
 甲烷化时生产效率,反应适宜在
甲烷化时生产效率,反应适宜在a.高温低压 b.高温高压 c.低温高压
③已知反应ⅰ的
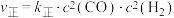 ,
,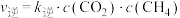 ,
, 、
、 为速率常数,若反应达平衡后升高温度,则
为速率常数,若反应达平衡后升高温度,则 值
值(2)
 甲醇化其中涉及的主要反应:
甲醇化其中涉及的主要反应:ⅰ.
 ;
;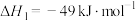
ⅱ.
 ;
;
①某研究小组利用
 催化剂将
催化剂将 转化为甲醇的机理如图所示。在该历程中,优先与催化剂反应的物质是
转化为甲醇的机理如图所示。在该历程中,优先与催化剂反应的物质是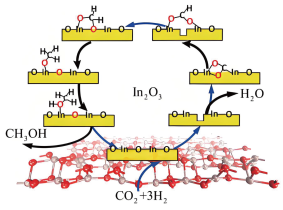
 ,保持压强为p MPa合成甲醇。达到平衡时,
,保持压强为p MPa合成甲醇。达到平衡时, 的转化率、
的转化率、 和CO的选择性随温度变化关系如图。
和CO的选择性随温度变化关系如图。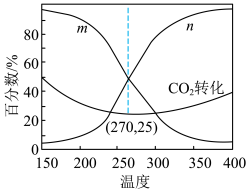
 的选择性=
的选择性=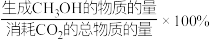 ;
;CO的选择性=
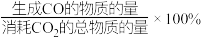 。
。270℃反应达到平衡,水蒸气的分压为
 为
为
您最近一年使用:0次
名校
解题方法
6 . 有机化合物A在生产生活中具有重要的价值, 研究其结构及性质具有非常重要的意义。
Ⅰ.测定分子组成
取4.6g有机化合物A在足量氧气中完全燃烧,生成0.3 mol H2O和0.2 mol CO2
(1)该有机化合物的实验式是___________ 。
Ⅱ.确定分子式
该有机化合物的质谱信息如图。___________ 。
Ⅲ.确定结构简式
有机化合物A的核磁共振氢谱有3组峰,峰面积之比为1:2:3。
(3)A的结构简式是___ 。
Ⅳ.解释性质
(4)有机化合物A能与水互溶的原因是A与水形成分子间氢键。在方框中画出1个A分子中两个不同的原子分别与H2O形成的氢键________ (氢键用“…”表示)。
① 酸性条件下,向V mL A溶液中加入 V1 mL c1 mol·L-1 K2Cr2O7溶液。A被氧化为B(B比A少2个氢原子,多1个氧原子),Cr2O 被还原为Cr3+
被还原为Cr3+
② 充分反应后,向①中加入过量KI溶液。
( )
)
③ 向②反应后的溶液中滴加c2 mol·L-1 Na2S2O3溶液,达到滴定终点时,消耗的体积为V2 mL( )。
)。
(5)①中参与反应的A与K2Cr2O7的物质的量之比是___________ 。
(6)结合实验数据,得cA =___________ mol·L-1(用代数式表示)。
Ⅰ.测定分子组成
取4.6g有机化合物A在足量氧气中完全燃烧,生成0.3 mol H2O和0.2 mol CO2
(1)该有机化合物的实验式是
Ⅱ.确定分子式
该有机化合物的质谱信息如图。
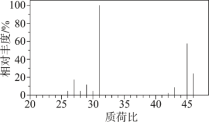
Ⅲ.确定结构简式
有机化合物A的核磁共振氢谱有3组峰,峰面积之比为1:2:3。
(3)A的结构简式是
Ⅳ.解释性质
(4)有机化合物A能与水互溶的原因是A与水形成分子间氢键。在方框中画出1个A分子中两个不同的原子分别与H2O形成的氢键

① 酸性条件下,向V mL A溶液中加入 V1 mL c1 mol·L-1 K2Cr2O7溶液。A被氧化为B(B比A少2个氢原子,多1个氧原子),Cr2O
 被还原为Cr3+
被还原为Cr3+② 充分反应后,向①中加入过量KI溶液。
(
 )
)③ 向②反应后的溶液中滴加c2 mol·L-1 Na2S2O3溶液,达到滴定终点时,消耗的体积为V2 mL(
 )。
)。(5)①中参与反应的A与K2Cr2O7的物质的量之比是
(6)结合实验数据,得cA =
您最近一年使用:0次
名校
解题方法
7 . CaMnO3是一种热电材料,立方CaMnO3的晶胞结构如图所示,晶胞参数为anm。下列说法错误的是
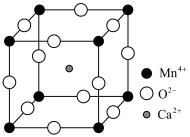
A. 与 与 之间的最近距离为 之间的最近距离为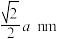 |
B.距离每个 最近的 最近的 原子有8个 原子有8个 |
| C.基态锰原子的第三电离能大于基态铬原子的第三电离能 |
D.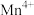 填充在由 填充在由 形成的八面体空隙中 形成的八面体空隙中 |
您最近一年使用:0次
名校
解题方法
8 . 硅元素及其化合物在生产生活中应用广泛。
回答下列问题:
(1)基态硅原子核外电子有___________ 种空间运动状态,价电子的电子排布图为___________ 。
(2)硅与碳同主族,但硅烷(SiH4)稳定性弱于甲烷,其原因是___________ 。
(3)高纯四氯化硅为无色透明液体,四氯化硅的空间构型为___________ ,四氯化硅易溶于苯,其原因是___________ ,四氯化硅熔点远低于氯化镁,其原因是___________ 。
(4)硅酸盐是地壳的主要成分。硅酸盐的最简单阴离子为 ,为硅氧四面体,结构如图1所示:
,为硅氧四面体,结构如图1所示:___________ 。
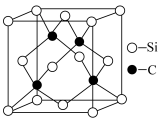
(5)碳化硅俗名金刚砂,其硬度大、熔点高,是良好的耐磨材料,其晶胞结构如图所示。晶体中碳原子位于硅原子组成的___________ (填“正方体”、“正四面体”或“正八面体”)中心;与碳原子距离最近且相等的碳原子有___________ 个,晶胞参数为anm,则碳化硅晶体的密度为___________ 。g·cm-3(列出计算式即可)。
回答下列问题:
(1)基态硅原子核外电子有
(2)硅与碳同主族,但硅烷(SiH4)稳定性弱于甲烷,其原因是
(3)高纯四氯化硅为无色透明液体,四氯化硅的空间构型为
(4)硅酸盐是地壳的主要成分。硅酸盐的最简单阴离子为
 ,为硅氧四面体,结构如图1所示:
,为硅氧四面体,结构如图1所示: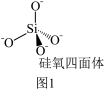

(5)碳化硅俗名金刚砂,其硬度大、熔点高,是良好的耐磨材料,其晶胞结构如图所示。晶体中碳原子位于硅原子组成的
您最近一年使用:0次
名校
解题方法
9 . 肉桂酸苄酯又名苯丙烯酸苄酯,常作为定香剂,也可用于香皂及食品香精的调香原料。以下是一种合成肉桂酸苄酯的路线。
Ⅱ.反应①、反应②的原子利用率均为100%
(1)A的名称为_____ 。
(2)反应③的试剂及条件为_____ 。
(3)上述合成路线涉及的反应中,属于取代反应的有_____ (填编号)。
(4)写出反应D→E的化学方程式_____ 。
(5)写出G在一定条件下生成的高分子化合物的结构简式_____ 。
(6)F同时满足下列条件的同分异构体共有_____ (不考虑立体异构)。
①苯环上有2个取代基
②能发生银镜反应和水解反应
③能与 溶液发生显色反应
溶液发生显色反应
其中核磁共振氢谱显示6组峰,且峰面积比为3:2:2:1:1:1的是_____ (填结构简式)。
(7)参照上述合成路线,以 为原料,设计制备
为原料,设计制备 的合成线路(无机试剂及溶剂任选)
的合成线路(无机试剂及溶剂任选)_____ 。

Ⅱ.反应①、反应②的原子利用率均为100%
Ⅲ.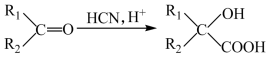
(1)A的名称为
(2)反应③的试剂及条件为
(3)上述合成路线涉及的反应中,属于取代反应的有
(4)写出反应D→E的化学方程式
(5)写出G在一定条件下生成的高分子化合物的结构简式
(6)F同时满足下列条件的同分异构体共有
①苯环上有2个取代基
②能发生银镜反应和水解反应
③能与
 溶液发生显色反应
溶液发生显色反应其中核磁共振氢谱显示6组峰,且峰面积比为3:2:2:1:1:1的是
(7)参照上述合成路线,以
 为原料,设计制备
为原料,设计制备 的合成线路(无机试剂及溶剂任选)
的合成线路(无机试剂及溶剂任选)
您最近一年使用:0次
名校
解题方法
10 . 下图所示的配合物离子,其中铁的一个配体为茂环阴离子( ),该配体以
),该配体以 电子参与配位,其结构如图。下列说法不正确的是
电子参与配位,其结构如图。下列说法不正确的是
 ),该配体以
),该配体以 电子参与配位,其结构如图。下列说法不正确的是
电子参与配位,其结构如图。下列说法不正确的是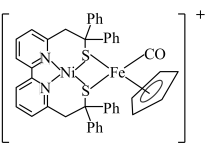
| A.该结构中共有3个配位体,其中镍的配位数为4 |
B.已知其中的镍为 ,则铁的化合价为+2 ,则铁的化合价为+2 |
| C.中心铁原子周围的价层电子数共有18个 |
D.S的杂化方式为 |
您最近一年使用:0次



